
- •Методические указания занятия № 1 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Вопросы для самоподготовки:
- •Контрольные вопросы и задачи
- •Методические указания занятия № 2 для студентов I курса фармацевтического факультета
- •Лабораторная работа Материальное обеспечение:
- •Опыт№ 1. Получение и свойства гидроксида магния
- •Опыт № 2. Свойства солей магния
- •1. Реакции с раствором серной кислоты
- •2. Реакции с карбонатами
- •1. Реакция с гидрофосфатом натрия (фармакопейная)
- •2. Реакция с оксихинолином (с9h6onh)
- •3. Окрашивание пламени (фармакопейная)
- •Методические указания занятия № 3 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Лабораторная работа Материальное обеспечение:
- •1. Реакция с раствором гидроксида аммония
- •2. Реакция с пероксидом водорода
- •3. Реакция с персульфатом аммония
- •Методические указания занятия № 4 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •К занятию повторить:
- •Лабораторная работа
- •1. Реакция с гидроксидом аммония
- •3. Реакция окисления персульфатом аммония (фармакопейная)
- •4. Микрокристаллоскопическая реакция со щавелевой кислотой
- •5. Реакция с пероксидом водорода на ион MnO4- (фармакопейная)
- •Методические указания занятия № 5 для студентов I курса фармацевтического факультета
- •Лабораторная работа
- •1. Реакция с гексацианоферратом (III) калия (фармакопейная)
- •2. Реакция с диметилглиоксимом (реактивом Чугаева)
- •1. Реакция с гексацианоферратом (II) калия (фармакопейная)
- •2. Реакция с тиоцианатом аммония
- •1. Реакция с тиоцианатом аммония
- •2. Реакция с нитрозо-р-солью (фармакопейная)
- •1. Реакция с диметилглиоксимом
- •Методические указания занятия № 6 для студентов I курса фармацевтического факультета
- •Методические указания занятия № 7 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Вопросы для самоподготовки:
- •Лабораторная работа Материальное обеспечение:
- •1. Реакция с гидроксидом аммония (фармакопейная)
- •2. Реакция восстановления катиона меди (II) до металлической меди (фармакопейная)
- •3. Реакция с рубеановодородной кислотой
- •Методические указания занятия № 8 для студентов I курса фармацевтического факультета
- •1.Реакция с сульфидом натрия.
- •2.Реакция с тиомочевиной.
- •4.Реакция с иодидом калия.
- •1.Восстановление до металлической ртути хлоридом олова(II).
- •2. Восстановление до металлической ртути медью.
- •3.Реакция с иодидом калия.
- •4.Реакция с хроматом калия.
- •2.Реакция с иодидом калия.
- •3.Реакция восстановления катионов ртути(II) до металлической.
- •4.Реакция с дифенилкарбазидом.
- •Контрольные вопросы и задачи
- •Методические указания занятия № 9 для студентов I курса фармацевтического факультета
- •Лабораторная работа:
- •1. Реакция с ализарином.
- •Аналитические реакции на анион b4o72-
- •1. Реакция с хлоридом бария.
- •2.Окрашивание пламени сложных эфиров борной кислоты (фармакапейная).
- •3.Реакция с куркумином (фармакапейная).
- •Контрольные вопросы
- •Методические указания занятия № 11 для студентов I курса фармацевтического факультета
- •Лабораторная работа
- •Аналитические реакции на ион (co32-):
- •1. Реакция с хлоридом бария.
- •2. Реакция с сильными кислотами (фармакопейная).
- •Аналитические реакции на ион scn-:
- •1. Реакция с нитратом серебра.
- •2. Реакция с солями железа (III).
- •1. Реакция с серной кислотой или растворимыми сульфатами.
- •2. Реакция с хроматом калия.
- •3. Реакция с иодидом калия или натрия (реакция «золотого дождя», фармакопейная).
- •2. Реакция с сульфидом натрия.
- •3. Реакция с водой.
- •Контрольные вопросы:
- •Лабораторная работа
- •Аналитические реакции на ион no2-
- •Аналитические реакции на ион no3-
- •1. Реакция с металлическим цинком или алюминием.
- •2. Реакция с медью и серной кислотой (фармакопейная).
- •3. Реакция с дифениламином (фармакопейная).
- •4. Реакция с хлоридом железа (II).
- •Аналитические реакции на ион no3-
- •1. Реакция разложения солей аммония щелочами (фармакопейная).
- •2. Реакция с реактивом Несслера.
- •Методические указания занятия № 13 для студентов I курса фармацевтического факультета
- •Вопросы для самоподготовки
- •Лабораторная работа
- •Аналитические реакции на анион po43-
- •1. Реакция с нитратом серебра (фармакопейная).
- •2. Реакция с молибдатом аммония.
- •3. Реакция с магнезиальной смесью (фармакопейная).
- •1. Реакция гидролиза.
- •2. Реакция с метиловым фиолетовым.
- •Реакция гидролиза.
- •Методические указания занятия № 14 для студентов I курса фармацевтического факультета
- •Методические указания занятия № 15 для студентов I курса фармацевтического факультета
- •2. Изучить окислительно-восстановительные свойства пероксида водорода.
- •Лабораторная работа
- •2. Реакция с нитратом серебра.
- •3. Реакция с сильными минеральными кислотами.
- •4. Реакция с иодом.
- •Методические указания занятия № 16 для студентов I курса фармацевтического факультета
- •1. Реакция с нитратом серебра (фармакопейная).
- •2. Реакция с сильными окислителями.
- •Список литературы
- •Методические указания занятия № 17 для студентов I курса фармацевтического факультета
3. Окрашивание пламени (фармакопейная)
Летучие соли бария окрашивают пламя в желто-зеленый цвет.
КОНТРОЛЬНЫЕ ВОПРОСЫ И ЗАДАЧИ
1. Каким образом и почему изменяются основные свойства гидроксидов металлов IIА группы в ряду Be(OH)2 – Ba(OH)2?
2. Напишите реакцию растворения бериллия в растворе хлороводородной кислоты и гидроксида натрия.
3. Допишите уравнения реакций, расставьте коэффициенты:
а) Mg + HCl →
в) Mg + HNO3 (Р.) →
г) Мg + HNO3 (к.) →
4. Объясните, почему при пропускании оксида углерода (IV) через раствор хлорида кальция осадок СаСО3 не выпадает, а при пропускании через раствор гидроксида кальция – выпадает?
5. Устранение постоянной жесткости воды можно проводить с помощью Na2CO3 и Na3PO4. Почему добавление Na3PO4 наиболее эффективно?
6. Напишите уравнения гидролиза следующих соединений:
а) ВаS ; б) Са(НСО3)2 ; в) [Be(H2O)4]Cl2 ; г) СаС2 .
7. Укажите, какие свойства элементов II А группы можно использовать для разделения пар катионов: а) Ве2+ и Мg2+; б) Ba2+ и Sr2+ .
8. Дайте рациональные названия следующим веществам: Ba(OH)2 ; Ca(OH)2 ; CaSO4 x 2H2O; MgSO4 x 7H2O; CaO.
9. Напишите предполагаемый химизм реакции образования внутрикомплексного соединения ионов Са2+ с эриохромом черным Т, имеющим структурную формулу:
 ОН HO
ОН HO
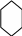
 H3OS
N=N
H3OS
N=N
NO2
10. Для качественного определения ионов бария по реакции с дихроматом калия в присутствии ацетата натрия образуется желтый осадок хромата бария. Объясните наблюдающееся явление. Ответ подтвердите уравнениями реакций.
11. При прокаливании 30 г кристаллогидрата сульфата кальция выделяется 6,28 г воды. Какова формула кристаллогидрата?
Методические указания занятия № 3 для студентов I курса фармацевтического факультета
ТЕМА: d-элементы VI В группы периодической системы Д. И. Менделеева. Хром и свойства его соединений. Аналитические реакции на ион Cr3+ .
ЦЕЛЬ: Изучить химические и аналитические свойства соединений хрома.
Хром – микроэлемент, входит в состав крови, головного мозга, участвует в углеводном обмене.
Целевые задачи:
1. Изучить условия существования в растворе хроматов и дихроматов.
2. Изучить окислительные свойства соединений хрома (VI).
3. Выполнить аналитические реакции на ион Cr3+.
ВОПРОСЫ ДЛЯ САМОПОДГОТОВКИ:
1. Общая характеристика элементов VI B группы.
2. Хром. Простое вещество и его химическая активность.
3. Хром(II). Свойства оксида и гидроксида хрома (II). Гидролиз солей. Восстановительные свойства соединений хрома (II).
4. Соединения хрома (III). Амфотерность оксида и гидроксида. Растворимость и гидролиз солей. Окислительно-восстановительные свойства соединений хрома (III). Комплексные соединения.
5. Соединения хрома(VI). Оксиды, хромовые и дихромовые кислоты, хроматы и дихроматы. Равновесие в растворе между хромат- и дихромат–ионами.
6. Окислительные свойства соединений хрома (VI), зависимость от рН среды.
7. Пероксид хрома и его структура. Надхромовая кислота.
8. Закономерность изменения кислотно–основных и окислительно-восстановительных свойств соединений хрома при переходе от низших к высшим степеням окисления.
9. Биологическое значение хрома и молибдена в организме. Химические основы применения соединений хрома в фармацевтическом анализе.
10. Аналитические реакции на катион Cr3+.
