
- •Методические указания занятия № 1 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Вопросы для самоподготовки:
- •Контрольные вопросы и задачи
- •Методические указания занятия № 2 для студентов I курса фармацевтического факультета
- •Лабораторная работа Материальное обеспечение:
- •Опыт№ 1. Получение и свойства гидроксида магния
- •Опыт № 2. Свойства солей магния
- •1. Реакции с раствором серной кислоты
- •2. Реакции с карбонатами
- •1. Реакция с гидрофосфатом натрия (фармакопейная)
- •2. Реакция с оксихинолином (с9h6onh)
- •3. Окрашивание пламени (фармакопейная)
- •Методические указания занятия № 3 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Лабораторная работа Материальное обеспечение:
- •1. Реакция с раствором гидроксида аммония
- •2. Реакция с пероксидом водорода
- •3. Реакция с персульфатом аммония
- •Методические указания занятия № 4 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •К занятию повторить:
- •Лабораторная работа
- •1. Реакция с гидроксидом аммония
- •3. Реакция окисления персульфатом аммония (фармакопейная)
- •4. Микрокристаллоскопическая реакция со щавелевой кислотой
- •5. Реакция с пероксидом водорода на ион MnO4- (фармакопейная)
- •Методические указания занятия № 5 для студентов I курса фармацевтического факультета
- •Лабораторная работа
- •1. Реакция с гексацианоферратом (III) калия (фармакопейная)
- •2. Реакция с диметилглиоксимом (реактивом Чугаева)
- •1. Реакция с гексацианоферратом (II) калия (фармакопейная)
- •2. Реакция с тиоцианатом аммония
- •1. Реакция с тиоцианатом аммония
- •2. Реакция с нитрозо-р-солью (фармакопейная)
- •1. Реакция с диметилглиоксимом
- •Методические указания занятия № 6 для студентов I курса фармацевтического факультета
- •Методические указания занятия № 7 для студентов I курса фармацевтического факультета
- •Целевые задачи:
- •Вопросы для самоподготовки:
- •Лабораторная работа Материальное обеспечение:
- •1. Реакция с гидроксидом аммония (фармакопейная)
- •2. Реакция восстановления катиона меди (II) до металлической меди (фармакопейная)
- •3. Реакция с рубеановодородной кислотой
- •Методические указания занятия № 8 для студентов I курса фармацевтического факультета
- •1.Реакция с сульфидом натрия.
- •2.Реакция с тиомочевиной.
- •4.Реакция с иодидом калия.
- •1.Восстановление до металлической ртути хлоридом олова(II).
- •2. Восстановление до металлической ртути медью.
- •3.Реакция с иодидом калия.
- •4.Реакция с хроматом калия.
- •2.Реакция с иодидом калия.
- •3.Реакция восстановления катионов ртути(II) до металлической.
- •4.Реакция с дифенилкарбазидом.
- •Контрольные вопросы и задачи
- •Методические указания занятия № 9 для студентов I курса фармацевтического факультета
- •Лабораторная работа:
- •1. Реакция с ализарином.
- •Аналитические реакции на анион b4o72-
- •1. Реакция с хлоридом бария.
- •2.Окрашивание пламени сложных эфиров борной кислоты (фармакапейная).
- •3.Реакция с куркумином (фармакапейная).
- •Контрольные вопросы
- •Методические указания занятия № 11 для студентов I курса фармацевтического факультета
- •Лабораторная работа
- •Аналитические реакции на ион (co32-):
- •1. Реакция с хлоридом бария.
- •2. Реакция с сильными кислотами (фармакопейная).
- •Аналитические реакции на ион scn-:
- •1. Реакция с нитратом серебра.
- •2. Реакция с солями железа (III).
- •1. Реакция с серной кислотой или растворимыми сульфатами.
- •2. Реакция с хроматом калия.
- •3. Реакция с иодидом калия или натрия (реакция «золотого дождя», фармакопейная).
- •2. Реакция с сульфидом натрия.
- •3. Реакция с водой.
- •Контрольные вопросы:
- •Лабораторная работа
- •Аналитические реакции на ион no2-
- •Аналитические реакции на ион no3-
- •1. Реакция с металлическим цинком или алюминием.
- •2. Реакция с медью и серной кислотой (фармакопейная).
- •3. Реакция с дифениламином (фармакопейная).
- •4. Реакция с хлоридом железа (II).
- •Аналитические реакции на ион no3-
- •1. Реакция разложения солей аммония щелочами (фармакопейная).
- •2. Реакция с реактивом Несслера.
- •Методические указания занятия № 13 для студентов I курса фармацевтического факультета
- •Вопросы для самоподготовки
- •Лабораторная работа
- •Аналитические реакции на анион po43-
- •1. Реакция с нитратом серебра (фармакопейная).
- •2. Реакция с молибдатом аммония.
- •3. Реакция с магнезиальной смесью (фармакопейная).
- •1. Реакция гидролиза.
- •2. Реакция с метиловым фиолетовым.
- •Реакция гидролиза.
- •Методические указания занятия № 14 для студентов I курса фармацевтического факультета
- •Методические указания занятия № 15 для студентов I курса фармацевтического факультета
- •2. Изучить окислительно-восстановительные свойства пероксида водорода.
- •Лабораторная работа
- •2. Реакция с нитратом серебра.
- •3. Реакция с сильными минеральными кислотами.
- •4. Реакция с иодом.
- •Методические указания занятия № 16 для студентов I курса фармацевтического факультета
- •1. Реакция с нитратом серебра (фармакопейная).
- •2. Реакция с сильными окислителями.
- •Список литературы
- •Методические указания занятия № 17 для студентов I курса фармацевтического факультета
1. Реакция с нитратом серебра (фармакопейная).
В пробирку помещают 2-3 капли раствора бромида калия, добавляют 3-5 капель раствора нитрата серебра, наблюдают образование бледно-желтого осадка. Осадок испытывают на растворимость в концентрированном растворе аммиака и карбоната аммония.
Br-+Ag+AgBr
2. Реакция с сильными окислителями.
В пробирку помещают 2-3 капли раствора бромида калия, добавляют 2-3 капли 2 моль/л раствора серной кислоты и 1-2 капли хлорной воды. Вследствие выделения свободного брома, раствор буреет. Добавляют 5-6 капель бензола и встряхивают. Бензол окрашивается в красновато-бурый цвет (бензольное кольцо), а при избытке хлорной воды становится лимонно-желтым, вследствие образования хлорида брома BrCl.
2Br-+Cl2Br2+2Cl-
Аналитические реакции на I-:
1. Реакция с нитратом серебра.
В пробирку помещают 2-3 капли раствор иодида калия, добавляют 2-3 капли раствора нитрата серебра. Наблюдают образование желтого осадка. Испытывают растворимость осадка в растворах азотной кислоты, аммиака, иодида калия и тиосульфата натрия.
I-+Ag+AgI
2. Реакция с хлорной водой и другими окислителями.
В пробирку помещают 2-3 капли раствора иодида калия и добавляют по каплям хлорную воду. Наблюдают выделение свободного иода. Прибавляют хлороформ, встряхивают и наблюдают появление фиолетовой окраски органического слоя. Затем добавляют избыток хлорной воды. Наблюдают исчезновение окраски.
2I-+Cl2I2+2Cl-
I2+5Cl2+6H2O2HIO3+10HCl
3. Реакция с солями свинца.
В пробирку помещают 3-5 капель раствора иодида калия, добавляют 2-3 капли соли свинца. Наблюдают образование желтого осадка иодида свинца. Испытывают растворимость осадка в растворах щелочей, иодида калия, при нагревании.
2I-+Pb2+PbI2
PbI2+2KIK2[PbI4]
4. Реакция с нитратом калия.
К 2-3 каплям иодида калия добавляют 3-4 капли 2 моль/л раствора серной кислоты, 6-8 капель бензола или хлороформа и 3-4 капли раствора нитрата калия. Смесь встряхивают. Наблюдают окрашивание органического растворителя в фиолетовый цвет.
2I-+2NO2-+4H+I2+2H2O+2NO
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА ОРГАНИЧЕСКИЕ ИОНЫ:
Оксалат-ион:
1. Реакция с хлоридом бария.
В пробирку помещают 2-3 капли раствора оксалата аммония и прибавляют 3-5 капель раствора хлорида бария. Наблюдают образование белого осадка. В одну пробирку прибавляют 2 моль/л раствор хлороводородной кислоты, а в другую 2 моль/л раствор уксусной кислоты. Наблюдают изменение осадков.
C2O42-+Ba2+BaC2O4
2. Реакция с хлоридом кальция.
В пробирку помещают 2-3 капли раствора оксалата аммония и прибавляют 3-5 капель раствора хлорида кальция. Наблюдают образование белого осадка. В одну пробирку прибавляют 2 моль/л раствор хлороводородной кислоты, а в другую 2 моль/л раствор уксусной кислоты. Наблюдают изменение осадков.
C2O42-+Ca2+CaC2O4
3. Реакция с перманганатом калия в кислой среде.
В пробирку помещают 2-3 капли раствора оксалата аммония, прибавляют 3-5 капель 2 моль/л раствора серной кислоты, нагревают на водяной бане до 70-80С и по каплям добавляют раствор перманганата калия. Наблюдают обесцвечивание раствора и выделение бесцветного газа.
5 C2O42-+2MnO4-+16H+2Mn2++10CO2+8H2O
CO2+Ca(OH)2CaCO3+H2O
Ацетат-ион:
1. Реакция с хлоридом железа (III) (фармакопейная)
В пробирку помещают 5-7 капель раствора, содержащего ацетат-ионы, добавляют 2-3 капли раствора хлорида железа (III). Наблюдают появление темно-красного окрашивания раствора. После этого содержимое пробирки нагревают до кипения. Наблюдают выпадение красно- бурого осадка основной соли.
3CH3COO-+Fe3+Fe(CH3COO)3
Fe(CH3COO)3+2HOHFe(OH)2CH3COO+2CH3COOH
2. Реакция с серной кислотой.
В пробирку помещают 2-3 капли раствора ацетата натрия, прибавляют 2-3 капли разбавленной серной кислоты и раствор осторожно нагревают. Обнаруживают выделяющуюся уксусную кислоту по запаху. Определению мешают анионы, образующие в этих условиях газообразнве продукты с резких запахом.
СH3COO-+H+CH3COOH
3. Реакция образования этилацетата (фармакопейная).
5-6 капель нагревают с равным количеством концентрированной серной кислоты и добавляют 4-5 капель эталового спирта. Ощущается запах этилацетата.
CH3COO-+C2H5OHCH3OOC2H5+OH-
Тартрат-ион:
1. Реакция с хлоридом калия (фармакопейная).
К 3-4 каплям раствора тартрата прибавляют 7-10 капель раствора хлорида калия и потирают стеклянной палочкой внутренние стенки пробирки. Наблюдают образование белого кристаллического осадка. Испытывают растворение осадка в минеральных кислотах и щелочах.
HC4H4O6-+K+KHC4H4O6
2. Реакция с резорцином (фармакопейная).
3
 -5
капель раствора тартрата нагревают с
2-3 каплями концентрированной серной
кислотой и с несколькими кристаллами
резосцина. Наблюдают появление
вишнево-красного окрашивания.
-5
капель раствора тартрата нагревают с
2-3 каплями концентрированной серной
кислотой и с несколькими кристаллами
резосцина. Наблюдают появление
вишнево-красного окрашивания.

 O
O



 C O OH
C O OH




 OH + C
О
OH + C
О

 H
C OH 2H
OH + 2 H C
H
C OH 2H
OH + 2 H C







 2HC
OH OH HO СH2
2HC
OH OH HO СH2
 H
C OH
гликолевый
HO
CH
H
C OH
гликолевый
HO
CH
 O
альдегид
OH
O
альдегид
OH
C
 OH
OH
Салицилат-ион:
1. К 2-3 каплям нейтрального раствора салицилата прибавляют 2 капли раствора хлорида железа (III), появляется сине-фиоелтовое или красно- фиолетовое окрашивание.



 COO
COO
 OH
OH
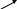
 +
FeCl3
FeCl + NaCl + HCl
+
FeCl3
FeCl + NaCl + HCl
COONa O
Бензоат-ион:
1. Реакция с хлоридом железа (III).
В пробирку помещают 3-5 капель нейтрального раствора бензоата и прибавляют 3-5 капель раствора хлорида железа(III). Наблюдают образование осадка. Испытывают растворимость полученного осадка в минеральных кислотах.

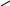

 O
O
O
O






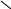 C
_ C 3+
C
_ C 3+
6
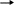 O + 2
FeCl3
+ 10
H2O O-
Fe
х
Fe(OH)3
+ 7H2O
O + 2
FeCl3
+ 10
H2O O-
Fe
х
Fe(OH)3
+ 7H2O


 O
3
O
3


 C
C
+ 3 OH
+ 6
Cl -
3 OH
+ 6
Cl -
2. Реакция с 5% раствором сульфата меди (II).
К 2-3 каплям раствора, содержащего бензоат-ионы добавляют по каплям 5% раствор сульфата меди (II), наблюдают образование осадка бирюзового цвета.

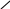

 O O
O O
2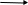


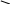 C _ +
CuSO4
C
Cu
+
SO4
2-
C _ +
CuSO4
C
Cu
+
SO4
2-
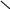
 O O
O O
2
Цитрат-ион:
1. Реакция с хлоридом кальция.
К 3-5 каплям нейтрального раствора, содержащего цитрат- ионы прибавляют 5-6 капель раствора хлорида кальция, раствор остается прозрачным, при кипячении образуется белый осадок цитрата кальция. Испытывают растворимость цитрата кальция в хлороводородной кислоте.
 _ _
_ _
C H2
- COO 3-
CH2
COO
H2
- COO 3-
CH2
COO

OH OH
2



 C _
+
3 Ca2+ C _
Ca3
C _
+
3 Ca2+ C _
Ca3
COO COO
_ _
 CH2
COO CH2
COO 2
CH2
COO CH2
COO 2
2. Реакция с сульфатом ртути (II).
К 3-5 каплям раствора, содержащего цитрат- ионы, прибавляют 1-2 капли 2 моль/л раствора хлороводородной кислоты, 1-2 капли перманганата калия и раствор слегка нагревают. К полученному раствору добавляют по каплям раствор соли ртути (II). Наблюдают образование белого осадка.
_ _

 _
3 2
_
3 2
CH2 COO CH2 COO
 OH
CH2
COO- 2+
OH
CH2
COO- 2+
 C _ MnO4- Hg C
O Hg
C _ MnO4- Hg C
O Hg
 COO C O
COO C O
_ _ CH2 COO
CH2 COO CH2 COO
