
- •10. Связь периодич-го з. Со строением эл-ных оболочек атомов. Пр. Клечковского. Энергетич. Ячейки. Правило Хунда.
- •8. Волновые свойства электрона. Квантовые числа,s-, p-,d-,f-состояния электронов. Электронные орбитали.
- •9. Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •16.Ионная (электронная связь).
- •15.Направленность ковалентной связи ᵹ- и π-связи. Гибридизация атомных орбиталей.
- •19.Донорно-акцепторный механизм ков.Св.. Комплексные соединения.
- •17. Представление о методе молекулярных орбиталей.
- •14. Ков.(атомная) св.. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •13.Образование химической связи. Энергия и длина связи.
- •11. Периодич.З.Д.И.Менделеева и периодич.Сист. Эл-ов: ряды, периоды, группы, подгруппы, порядковый номер эл-та.
- •7. З.Хим.Экв-ов. Молярные экв-ные массы сложных в-в.
- •3. Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •6. Основные стехиометрические законы.
- •5. Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •21. Система. Фаза. Компонент. Параметры. Функции состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •22. Первое начало термодинамики. Закон Гесса как следствие первого начала термодинамики. Термохимические расчеты.
- •27. Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.Первый закон.
- •29.Условия самопроизвольного протекания химических реакций.
- •34.Скорость химической реакции. Закон действующих масс. Константа скорости.
- •36. .Кинетическая классификация по степени сложности. Обратимые и необратимые реакции.
- •41. Дисперсные системы. Коллоидные растворы.
- •37 .Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса
- •44. Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •50.Произведение растворимости.
- •12. Периодическое изменение свойств химических элементов. Радиус атомов, сродство электрону,
- •57.Электролиз. Последовательность разряда ионов на катоде и аноде.
- •3) Ме,стоящие в ряду напр-я посла водорода
- •59.Классификация химических источников тока.
- •60. Коррозия металлов. Химическая и электрохимическая коррозия.
- •61. Основные методы борьбы с коррозией.
- •62. Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •64.Сущн-ть физико-химич.Анализа.Пр-ло фаз.Диаграмма состояния воды.
- •67.Адсорбция и абсорбция.
- •64. Основные принципы построения диаграммы плавкости бинарных систем.
- •1. Принцип непрерывности.
- •2. Принцип соответствия.
- •65. Эвтектическая диаграмма плавкости (без образования твердых растворов).
17. Представление о методе молекулярных орбиталей.
Основаны на том, что для каждого из электронных состояний молекулы как многоэлектронной системы полная волновая ф-ция составляется из произведений волновых ф-ций электронов (мол. орбита-лей) в соответствии с электронной конфигурацией системы, т. е. с учетом чисел заполнения (1 или 2). Числа заполнения при этом показывают, сколько электронов-один или два-занимают данную орбиталь, так что данная орбиталь входит в произведение один или два раза. Поскольку, согласно Паули принципу. полная волновая ф-ция системы электронов должна быть антисимметрична относительно перестановок индексов (номеров) электронов, ее представляют в виде определителя (или линейной комбинации неск. определителей), построенного из мол. спин-орбиталей и называемого о п р е д е л и т е л е м С л е й т е р а (Слэтера).
14. Ков.(атомная) св.. Метод валентных связей. Возбужденные состояния атомов. Валентность.
К.с.
возникает м/у элементами с одинаковым
или близким знач-ми эн.сродства к
электрону. Валентность атомов в
соединениях с к.св.опр.по числу электронных
пар(1пара–1ед.валентности).Для оценки
отн.зарядности элемента в ков.соед-х
(на самом деле никаких зарядов в этих
соед-х нет) прибегают к приему: мысленно
связь разорвать ,при разрыве связи в
пределах периода электрон смещается
от левее стоящего элемента к правее
стоящего, а в пределах гл.подгр.от ниже
стоящему к выше.2
метода
объяснения механизма возн-ния ков.св.:
метод валентных связей (МВС) и метод
молекулярных орбиталей (МО).В основе
МВС лежит 3 положения: 1. Химическая связь
образуется двумя электронами с
противоположно направленными спинами.
При этом имеет место взаимное перекрытие
электронных орбиталей. М/у атомами
возникает зона повышенной электронной
плотности, к которой притягиваются ядра
с остальными электронами.

2. Связь имеет ориентацию в направлении, обеспечивающем макс.возможное перекрывание орбиталей.3.Чем больше взаимное перекрывание эл-ных орбиталей, тем прочнее связь.Валентными являются неспаренные электроны. Их число можно изобр.c помощью эл-ной конфигурации атомов.При возб-и атомов (за счет притока эн.извне) имеет место «распаривание» электронов и переход электрона на более удалённый подуровень в пределах одного уровня. Распаривание одной электронной пары может увеличить валентность на 2 единицы.
13.Образование химической связи. Энергия и длина связи.
При взаимодействии атомов между ними может возникнуть химическая связь, приводящая к образованию молекулы/иона/кристалла. Чем прочнее связь, тем больше требуется затратить энергии на ее разрыв.
При возникновении связи энергия выделяется, следовательно уменьшается потенциальная энергия системы электронов и ядер.
Потенциальная
эн. образующейся молекулы меньше
суммарной потенциальной эн.исходных
свободных атомов.Для характеристики
химической связи используются следующие
термины:Длина
связи
- межъядерное расстояние в невозбуждённой
молекуле (обычно 1-2 Ангстрема, 1А=
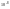 см).Эн.связи
– энергия, выделяющаяся при образовании
данного вида связи (150-1000 кДж/моль).
см).Эн.связи
– энергия, выделяющаяся при образовании
данного вида связи (150-1000 кДж/моль).
