
- •10. Связь периодич-го з. Со строением эл-ных оболочек атомов. Пр. Клечковского. Энергетич. Ячейки. Правило Хунда.
- •8. Волновые свойства электрона. Квантовые числа,s-, p-,d-,f-состояния электронов. Электронные орбитали.
- •9. Принцип Паули. Емкость энергетических уровней и подуровней атомов элементов.
- •16.Ионная (электронная связь).
- •15.Направленность ковалентной связи ᵹ- и π-связи. Гибридизация атомных орбиталей.
- •19.Донорно-акцепторный механизм ков.Св.. Комплексные соединения.
- •17. Представление о методе молекулярных орбиталей.
- •14. Ков.(атомная) св.. Метод валентных связей. Возбужденные состояния атомов. Валентность.
- •13.Образование химической связи. Энергия и длина связи.
- •11. Периодич.З.Д.И.Менделеева и периодич.Сист. Эл-ов: ряды, периоды, группы, подгруппы, порядковый номер эл-та.
- •7. З.Хим.Экв-ов. Молярные экв-ные массы сложных в-в.
- •3. Понятие о химическом эквиваленте и эквивалентной массе простых и сложных веществ. Закон химических эквивалентов.
- •6. Основные стехиометрические законы.
- •5. Основные газовые законы. Определение молекулярных масс газообразных веществ.
- •21. Система. Фаза. Компонент. Параметры. Функции состояния: внутренняя энергия и энтальпия. Стандартные условия.
- •22. Первое начало термодинамики. Закон Гесса как следствие первого начала термодинамики. Термохимические расчеты.
- •27. Объединенная формула первого и второго начала термодинамики. Свободная энергия Гиббса и Гельмгольца.Первый закон.
- •29.Условия самопроизвольного протекания химических реакций.
- •34.Скорость химической реакции. Закон действующих масс. Константа скорости.
- •36. .Кинетическая классификация по степени сложности. Обратимые и необратимые реакции.
- •41. Дисперсные системы. Коллоидные растворы.
- •37 .Зависимость скорости реакции от температуры. Правило Вант-Гоффа. Уравнение Аррениуса
- •44. Растворимость газов в жидкостях. Закон Генри-Дальтона. Закон распределения.
- •50.Произведение растворимости.
- •12. Периодическое изменение свойств химических элементов. Радиус атомов, сродство электрону,
- •57.Электролиз. Последовательность разряда ионов на катоде и аноде.
- •3) Ме,стоящие в ряду напр-я посла водорода
- •59.Классификация химических источников тока.
- •60. Коррозия металлов. Химическая и электрохимическая коррозия.
- •61. Основные методы борьбы с коррозией.
- •62. Кристаллическое состояние вещества. Химическая связь в кристаллах.
- •64.Сущн-ть физико-химич.Анализа.Пр-ло фаз.Диаграмма состояния воды.
- •67.Адсорбция и абсорбция.
- •64. Основные принципы построения диаграммы плавкости бинарных систем.
- •1. Принцип непрерывности.
- •2. Принцип соответствия.
- •65. Эвтектическая диаграмма плавкости (без образования твердых растворов).
65. Эвтектическая диаграмма плавкости (без образования твердых растворов).
Диаграмма состояния системы - диаграмма, указывающая, в каких фазовых состояниях находится система в зависимости от условий: температура, давление и состав.
Диаграммы плавкости – частный вид диаграмм состояния.
Для систем, дающих диаграмму плавкости такого типа, характерна полная взаимная растворимость компонентов в жидком состоянии и нерастворимость – в твердом.
Пример. Системы Pb-Ag, Cd-Bi, Tl-Au, KCl-LiCl и т.д.
Чтобы
построить диаграмму плавкости системы
А-В, необходимо приготовить несколько
сплавов – от 100% А, через каждые
![]() - до 100%В.
- до 100%В.
Далее снимаются кривые охлаждения и характерные точки переносятся на диаграмму плавкости бинарной системы А-В. Температуры плавления чистых компонентов -tА и tВ.
Температура начала первичной кристаллизации сплава 4 – t4, окончание – tE. Подобным же образом переносят характерные точки для всех сплавов и соединяют их на диаграмме плавными линиями, получая в итоге диаграмму плавкости системы A-B.
Ломанная линия tАЕtВ - “линия ликвидуса”, выше нее возможно существование лишь жидкой фазы.
Линия MEN – “линия солидуса”, ниже нее – лишь твердая фаза.
Между солидусом и ликвидусом область сосуществования двух фаз – твердой и жидкой.
На линии Ликвидуса нах-ся 2 компонента 2 фазы, число ст.своб.=1,в точке эвтептики три фазы.
66.Поверхностные
явления. Понятие поверхностного
натяжения.Поверхностное натяжение
– избыток свободной энергии в поверхностном
слое, отнесенный к
 поверхности поглощающего тела.
поверхности поглощающего тела.
 Поверхностное
растяжение растворов зависит от природы
растворителя и растворенного вещества,
от концентрации последнего и от
температуры. Поверхностное натяжение
как функция концентрации растворенного
вещества при Т-const
- изотерма
поверхностного натяжения.
Поверхностное
растяжение растворов зависит от природы
растворителя и растворенного вещества,
от концентрации последнего и от
температуры. Поверхностное натяжение
как функция концентрации растворенного
вещества при Т-const
- изотерма
поверхностного натяжения.
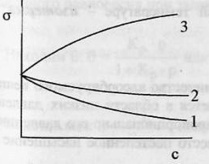 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные вещества
(ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.
1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные вещества
(ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.
66-67.Поверхностное
натяжение растворов. Изотерма
адсорбции.Поверхностное натяжение
– избыток свободной энергии в поверхностном
слое, отнесенный к
поверхности поглощающего тела.
 Поверхностное
растяжение растворов зависит от природы
растворителя и растворенного вещества,
от концентрации последнего и от
температуры. Поверхностное натяжение
как функция концентрации растворенного
вещества при Т-const
- изотерма
поверхностного натяжения.
Поверхностное
растяжение растворов зависит от природы
растворителя и растворенного вещества,
от концентрации последнего и от
температуры. Поверхностное натяжение
как функция концентрации растворенного
вещества при Т-const
- изотерма
поверхностного натяжения.
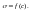 1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные вещества
(ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции.
1
и 2 – поверхностно-активные вещества
(ПАВ).3 – поверхностно-инактивные вещества
(ПИАВ).Разность
с в поверхностном слое – поверхностный
избыток вещества Г (гамма).Для
ПАВ Г>0, для ПИАВ Г<0.Поверхность
твердых тел, как и жидкостей, обладает
избыточной свободной
энергией Гиббса.
Твердые тела не могут (в отличие от
жидкостей) самопроизвольно изменять
площадь поверхности.Величина адсорбции
зависит
от природы адсорбента и адсорбата, от
давления газа, температуры.Зависимость
адсорбируемого количества газа от
давления адсорбата при постоянной
температуре – изотерма адсорбции.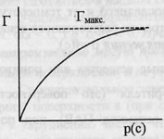 С
ростом давления увеличивается количество
адсорбируемого вещества.Лэнгмюр при
выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало. 3.
адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения адсорбента
адсорбатом:
С
ростом давления увеличивается количество
адсорбируемого вещества.Лэнгмюр при
выводе уравнения изотермы сделал
следующие допущения: 1. все места
адсорбента одинаковы. 2. взаимодействие
между частицами пренебрежимо мало. 3.
адсорбционный слой состоит из одного
слоя молекул, адсорбция локализованная
– нет перемещения адсорбционного
комплекса вдоль поверхности
адсорбента.Степень заполнения адсорбента
адсорбатом:
 Скорость
адсорбции:
Скорость
адсорбции:
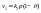
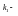 константа скорости адсорбции.Скорость
десорбции:
константа скорости адсорбции.Скорость
десорбции:
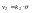
 константа скорости десорбции.Адсорбционное
равновесие наступает при вается в
промежуточной области.Процесс адсорбции
экзотермичен: поглощение вещества
протекает с выделением теплоты, десорбция
– с поглощением теплоты.Если адсорбируются
несколько
газов:
константа скорости десорбции.Адсорбционное
равновесие наступает при вается в
промежуточной области.Процесс адсорбции
экзотермичен: поглощение вещества
протекает с выделением теплоты, десорбция
– с поглощением теплоты.Если адсорбируются
несколько
газов:
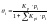 Для
адсорбции на неоднородной поверхностибыло
предложено эмпирическое уравнение
Фрейндлиха.
Для
адсорбции на неоднородной поверхностибыло
предложено эмпирическое уравнение
Фрейндлиха.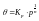
 к
и n
– коэффициенты, постоянные для данного
адсорбента и газа при данной
температуре.Уравнение Фрейндлиха,
наоборот, не отражает особенностей
изотермы в области высоких и низких
давлений, но для области промежуточных
давлений согласуются с опытными
данными.
к
и n
– коэффициенты, постоянные для данного
адсорбента и газа при данной
температуре.Уравнение Фрейндлиха,
наоборот, не отражает особенностей
изотермы в области высоких и низких
давлений, но для области промежуточных
давлений согласуются с опытными
данными. Уравнение
изотермы хорошо передает зависимости
в области низких и области высоких
давлений, но не всегда оправды
Уравнение
изотермы хорошо передает зависимости
в области низких и области высоких
давлений, но не всегда оправды
