
- •Введение
- •1. Строение и свойства материалов
- •1.1. Классификация материалов
- •Плазма газ жидкость твердое тело
- •1.2. Кристаллическое строение материалов
- •1.3. Дефекты кристаллического строения
- •1.3.1. Точечные дефекты
- •1.3.2. Линейные дефекты
- •1.3.3. Поверхностные и объемные дефекты
- •1.4. Свойства материалов и методы их испытаний
- •2. Кристаллизация металлов и сплавов
- •2.1. Гомогенная и гетерогенная кристаллизация
- •2.2. Строение металлического слитка
- •2.3. Выращивание монокристаллов
- •2.3.1. Получение монокристаллов из расплава
- •2.3.2. Получение монокристаллов из раствора
- •2.3.2. Получение монокристаллов из паровой фазы
- •2.4. Аморфные металлические сплавы
- •3. Деформация и разрушение металлов
- •3.1. Упругая и пластическая деформация
- •3.2 Деформация моно- и поликристаллов
- •3.3. Влияние температуры на структуру деформированного металла
- •4. Основы теории двойных сплавов
- •4.1. Строение сплавов
- •4.2. Диаграммы состояния двойных сплавов
- •4.3. Диаграмма состояния железоуглеродистых сплавов
- •4.4. Углеродистые стали
- •4.5. Чугуны
- •5. Основы термической обработки стали
- •5.1. Основные превращения в стали
- •5.2. Отжиг стали
- •5.3. Закалка и отпуск
- •6. Поверхностное упрочнение деталей
- •6.1. Упрочнение методом пластической деформации
- •6.2. Упрочнение методом поверхностной закалки
- •6.3. Химико-термическая обработка
- •7. Легированные стали
- •7.1. Влияние легирующих элементов на структуру и свойства
- •7.2. Маркировка и классификация легированных сталей
- •7.3. Конструкционные стали
- •7.4. Инструментальные стали
- •7.5. Стали с особыми свойствами
- •8. Цветные металлы и сплавы
- •8.1. Титан и его сплавы
- •8.2. Алюминий и его сплавы
- •8.3. Магний и его сплавы
- •8.4. Медь и ее сплавы
- •8.5. Другие цветные металлы и сплавы
- •8.6. Материалы с памятью формы
- •9. Неметаллические и композиционные материалы
- •9.1. Полимеры
- •9.2. Пластмассы
- •9.3. Композиционные материалы
- •9.4. Керамические материалы
- •10. Материалы с особыми электрическими свойствами
- •10.1. Физическая природа электропроводности
- •10.2. Факторы, влияющие на удельное сопротивление
- •10.3. Материалы высокой проводимости
- •10.4. Сверхпроводящие металлы и сплавы
- •10.5. Материалы с высоким сопротивлением
- •10.6. Металлы и сплавы различного назначения
- •10.7. Материалы для припоев
- •11. Материалы с особыми магнитными свойствами
- •11.1. Классификация веществ по магнитным свойствам
- •11.2. Природа ферромагнитного состояния
- •11.3. Процессы намагничивания ферромагнетиков
- •Магнитная проницаемость, определяемая по формуле
- •11.4. Классификация магнитных материалов
- •11.4.1. Магнитомягкне материалы
- •Высокочастотные магнитомягкие материалы.
- •11.4.2. Магнитотвердые материалы
- •Заключение
- •Литература
- •Оглавление
2. Кристаллизация металлов и сплавов
Переход металла из жидкого или парообразного состояния в твердое (кристаллическое) называется первичной кристаллизацией. Образование новых кристаллов в твердом теле называют вторичной кристаллизацией. Процесс кристаллизации, как установил Д.К. Чернов, осуществляется в два этапа: возникновение зародыша и рост из него кристалла. Различают гомогенное (в объеме жидкой фазы) и гетерогенное (на поверхности твердых частиц, неметаллических включений, стенок изложниц и др.) зарождение кристаллов.
2.1. Гомогенная и гетерогенная кристаллизация
Г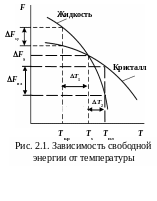 омогенная
кристаллизация.
Состояние системы характеризуется
внутренней энергией, которая складывается
из энергии движения атомов (ионов),
электронов, энергии упругих искажений
кристаллической решетки и т. д.
Часть энергии, которая при изотермических
условиях может быть превращена в работу,
называется свободной:
омогенная
кристаллизация.
Состояние системы характеризуется
внутренней энергией, которая складывается
из энергии движения атомов (ионов),
электронов, энергии упругих искажений
кристаллической решетки и т. д.
Часть энергии, которая при изотермических
условиях может быть превращена в работу,
называется свободной:
F = U – T S,
где F – свободная энергия, U – полная внутренняя энергия, T – температура; S – энтропия. Вещество может находиться в твердом, жидком или газообразном агрегатных состояниях. Переход в новое состояние возможен, если оно обладает меньшим запасом свободной энергии.
С ростом температуры свободная энергия F металла в жидком и твердом состояниях уменьшается (рис. 2.1):
![]() .
.
При равновесной температуре кристаллизации Тs свободные энергии жидкой и твердой фаз одинаковы, обе фазы сосуществуют одновременно, изменение энергии не происходит:
Fs = Fж – Fт = 0.
Процесс кристаллизации должен быть термодинамически выгоден, и сопровождаться уменьшением свободной энергии системы. Это возможно тогда, когда жидкая фаза будет охлаждена ниже Тs до практической температуры кристаллизации Ткр. Переход из жидкого состояния в твердое сопровождается выделением энергии:
Fкр = Fж – Fт > 0.
Охлаждение расплава ниже равновесной температуры называют переохлаждением и характеризуют степенью переохлаждения:
T1 = Тs – Ткр.
Плавление – процесс обратный кристаллизации – происходит при перегреве выше равновесной температуры. Переход из твердого состояния в жидкое сопровождается поглощением энергии:
Fпл = Fж – Fт < 0.
Нагревание расплава выше равновесной температуры называют перегревом и характеризуют степенью перегрева: T2 = Тпл – Тs.
Разница между реальными температурами плавления и кристаллизации – температурный гистерезис.
М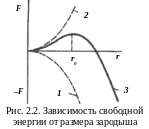 еханизм
процесса кристаллизации.
При переходе жидкого металла в твердое
состояние выигрыш в свободной энергии
(рис. 2.2, кривая
1)
должен
быть больше
затрат энергии на образование поверхности
раздела жидкость-кристалл
(кривая
2).
Изменение
свободной энергии системы F
определяется алгебраической суммой
поверхностной S
и объемной Vf
энергий
зародыша:
еханизм
процесса кристаллизации.
При переходе жидкого металла в твердое
состояние выигрыш в свободной энергии
(рис. 2.2, кривая
1)
должен
быть больше
затрат энергии на образование поверхности
раздела жидкость-кристалл
(кривая
2).
Изменение
свободной энергии системы F
определяется алгебраической суммой
поверхностной S
и объемной Vf
энергий
зародыша:
F = – V f + S ,
где S – поверхность зародыша; – удельное поверхностное натяжение на границе раздела; V – объем зародыша; f – разность свободных энергий жидкого и кристаллического состояний, приходящаяся на единицу объема. Увеличение размера зародыша сначала приводит к росту свободной энергии (объем зародыша мал, поверхность велика), при некотором критическом значении r0 – к уменьшению (рис. 2.2, кривая 3). Минимальный размер способного к росту зародыша называется критическим, зародыш – устойчивым. Зародыши образуются независимо друг от друга, растущие кристаллы имеют правильную форму (см. рис. 2.3). При срастании с другими кристаллами форма нарушается, кристаллы называют зернами. Их рост продолжается в направлениях оставшихся участков жидкого металла.
Д
 ля
образования и роста зародышей требуется
диффузионное перемещение атомов в
жидком металле. Каждой температуре
кристаллизации (степени переохлаждения)
отвечает определенный размер устойчивого
зародыша: мелкие растворяются в жидкости,
крупные растут. Чем ниже температура
(больше степень переохлаждения), тем
меньше размер устойчивого зародыша,
тем больше центров кристаллизации
образуется в единицу времени, тем быстрее
идет процесс кристаллизации.
ля
образования и роста зародышей требуется
диффузионное перемещение атомов в
жидком металле. Каждой температуре
кристаллизации (степени переохлаждения)
отвечает определенный размер устойчивого
зародыша: мелкие растворяются в жидкости,
крупные растут. Чем ниже температура
(больше степень переохлаждения), тем
меньше размер устойчивого зародыша,
тем больше центров кристаллизации
образуется в единицу времени, тем быстрее
идет процесс кристаллизации.
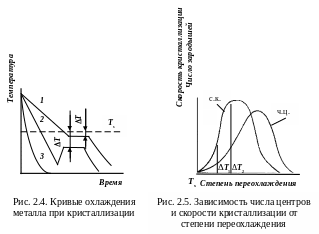
При медленном охлаждении (рис. 2.4, кривая 1) степень переохлаждения T1 мала (рис. 2.5), кристаллизация протекает при высокой температуре, близкой к равновесной. На кривой температура-время появляется горизонтальная площадка, так как отвод тепла компенсируется выделяющейся при кристаллизации скрытой теплотой кристаллизации. В расплаве за единицу времени в единице объема образуется мало зародышей (размерность – мм-3∙с-1) из которых вырастают крупные кристаллы. Новые зародыши, как правило, не образуются.
С увеличением скорости охлаждения (рис. 2.4, кривая 2) кристаллизация протекает при более низкой температуре. Число зародышей увеличивается, из них вырастает много мелких кристаллов. Скорость кристаллизации – скорость увеличения линейных размеров кристалла –имеет размерность мм∙с-1. При большой степени переохлаждения скрытая теплота выделяется в начальный момент кристаллизации бурно, температура резко повышается.
С увеличением степени переохлаждения скорость диффузии атомов уменьшается, образование зародышей и их рост затрудняется.
При максимальной скорости охлаждения (кривая 3) диффузия атомов мала, число центров кристаллизации и скорость роста кристаллов равны нулю, образуется аморфная структура – металлическое стекло.
Степень переохлаждения зависит от объема жидкого металла и его чистоты. При большом объеме жидкого металла выделяющаяся при кристаллизации теплота повышает температуру практически до равновесной; при малом объеме – выделяющейся теплоты недостаточно, кристаллизация происходит с большей степенью переохлаждения. Значительное переохлаждение достигается только при затвердевании очень чистых металлов. У технически чистых металлов и сплавов степень переохлаждения невелика: 10–30 °С. Соли, силикаты, органические вещества, наоборот, склонны к переохлаждению.
Гетерогенная кристаллизация. Самопроизвольное образование зародышей происходит только в чистом жидком металле. Образование зародышей часто происходит на инородных включениях (примесях), которые всегда присутствуют в расплаве.
Если атомы примеси и затвердевающего металла имеют одинаковые кристаллические решетки (структурный фактор) и размеры атомов не отличаются более чем на 5–7 % (размерный фактор), то такие изоморфные примеси играют роль готовых центров кристаллизации. Структурное сходство между поверхностями сопряжения зародыша и включения приводит к уменьшению критического размера зародыша. Затвердевание начинается при меньшем переохлаждении, чем при самопроизвольной кристаллизации. Чем больше примесей, тем больше центров кристаллизации и мельче зерно. Такое образование зародышей называют гетерогенным. Кристаллизация обычно начинается от стенок формы, которые играют ту же роль, что и включения.
Если неизоморфные примеси имеют контакт с затвердевающим металлом, то строение их поверхностного слоя изменяется, приспосабливаясь к строению кристаллов металла – активация примесей. На активированной примеси осаждаются атомы затвердевающего металла.
Растворенные в жидком металле поверхностно-активные примеси могут измельчать зерно и изменять форму растущего кристалла, осаждаясь тонким слоем на его поверхности. Это приводит к уменьшению поверхностной энергии на границе раздела.
модифицирование – введение в расплав различных веществ (модификаторов) с целью повышения механических, технологических и эксплуатационных свойств отливок путем измельчения структуры. Кроме модифицирования, применяют физические воздействия на структуру кристаллизующегося металла: регулирование температуры расплава и его охлаждение при переливе, вибрацию, ультразвук, электромагнитное перемешивание и др. Есть и комбинированные способы: ввод модификаторов и наложение колебаний с ультразвуковой частотой.
Установлено два типа воздействия модификаторов на структуру.
Монотонное измельчение зерна с повышением содержания модификатора. При содержании более 0,2–0,6 % оно стабилизируется.
Немонотонное измельчение зерна с областью оптимальной концентрации 0,01–0,1 %. Превышение приводит к увеличению размера зерна.
Монотонное уменьшение размера зерна с повышением концентрации модификатора характерно для нерастворимых примесей (титан в алюминии), немонотонное – для поверхностно-активных растворимых примесей (например, магний в цинке).
При модифицировании алюминиевых сплавов применяют Ti, V, Zr; стали – Al, V, Ti. Бор используют в качестве поверхностно-активного модификатора для никелевых и железных сплавов, магний – для чугуна.
Демодификаторы – добавки, повышающие размер зерна. Они увеличивают работу образования зародыша, задерживают его образование и понижают вероятность возникновения центра кристаллизации.
