
- •Ответы к государственному экзамену по хирургии
- •Физическая антисептика
- •Подготовка операционного поля
- •1. Гемодинамические или противошоковые: полиглюкин (макродекс, реополиглюкин (реомакродекс), желатиноль.)
- •2. Дезинтоксикационные: гемодез, неогемодез, полидез (компенсан, «I окомпенсан).
- •3. Препараты для парентерального питания:
- •4. Регуляторы водно-солевого и кислотно-щелочного состояния:
- •5. Растворы осмодиуритического действия: маннитол, сорбитол.
- •6. Клиническая картина.
- •I По источнику воспалительного процесса:
- •II По характеру клинических и паталогоанатомических проявлений:
- •III По локализации очага поражения:
- •IV По этиологии.
- •1. Серозно-инфильтративная.
- •2. Гнойно-некротическая.
- •1. Местное лечение.
- •2. Общее лечение.
- •I. Местное лечение.
- •II. Общее лечение.
- •1. Микробные ассоциации
- •2. Местные факторы, способствующие развитию гангрены
- •3. Снижение устойчивости организма:
- •Профилактика анаэробной гангрены
- •Лечение
- •Осложнения оперативного лечения
- •Строение отростка
- •Клиника.
- •2. По клиническим формам.
- •3. Варианты течения:
- •Физиология билирубинового обмена
- •Дифференциальная диагностика желтухи.
- •I этап: есть ли и было ли кровотечение у данного больного?
- •II этап: возникло ли кровотечение из гастродуо-денальной зоны или из других анатомических областей с последующим заглатыванием крови.
- •Компенсированный стеноз
- •Субкомпенсированный стеноз
- •Декомпенсированный стеноз
- •1. Срочные торакотомий: выполняются сразу при поступлении пострадавшего.
- •2. Ранние торакотомий: выполняются в течение первых суток после травмы
- •1. В зависимости от направления выхождения внутренностей:
- •II этап. Эпоха видеоскопической эндохирургии
- •Функциональные методы исследования
- •До прорыва абсцесса в бронх.
- •Прорыв абсцесса в бронх
- •По состоянию клапанов:
- •Синдром портальной гипертензии
- •1. Стеноз подвздошных артерий – трансилюминальная ангиопластика.
- •2. Стенозы - шунтирующие операции - аорто-бедренное (абш), бедренно-подколенное (бпш), бедренно-тибиальное (бтш).
- •3. Дистальная форма поражения - артериализация венозного кровотока.
- •2. Инородные тела пищевода
- •3. Химические ожоги пищевода
- •Терминальная стадия хпн по н. А. Лопаткину, и. Н. Кучинскому
- •Аномалии положения почек
- •Аномалии взаимоотношения почек
- •Асимметричные формы сращения
- •Аплазия почки - Тяжелая степень недоразвития паренхимы, нередко сочетающее с отсутствием мочеточника. Порок формируется в раннем эмбриональном периоде до образования нефронов.
- •Кистозные аномалии почек Поликистоз почек
- •* Оценка производится в соответствии с критериями Kruger и Menkfeld.
- •1. Обеспечить проходимость дыхательных путей, оценить степень дыхательной недостаточности.
- •7. Транспортная иммобилизация.
- •8. Проведение инфузионной терапии.
Терминальная стадия хпн по н. А. Лопаткину, и. Н. Кучинскому
Форма клинического течения |
Клиническая характеристика |
Виды лечения |
0 |
по своему течению напоминает интермиттирующую стадию; водовыделительная функция сохранена, азотемия без тенденции к быстрому росту (мочевина до 25 ммоль/л, клубочковая фильтрация – 10 – 15 мл/мин, СМ – до 0,6 ед.), изогипостенурия, водные и электролитные нарушения не выражены |
консервативное |
I |
водовыделительная функция сохранена; клубочковая фильтрация менее 10 мл/мин, значительная азотемия (мочевина – 25 – 35 ммоль/л, креатинин – до 1,0 ммоль/л, СМ – до 0,75 ед.); умеренный метаболический ацидоз и электролитные нарушения |
консервативное, подготовка к гемодиализу, пересадка почки без диализо-терапии |
IIа |
олигурия, задержка жидкости в тканях, дисэлектролитемия, гиперазотемия (мочевина – свыше 35 ммоль/л, креатинин – свыше 1,1ммоль/л, фильтрация – ниже 5 мл/мин); обратимые изменения сердечно-сосудистой системы; гипертензия не выше 200/120 мм рт. ст.; недостаточность кровообращения II степени |
хронический гемодиализ и трансплантация почки |
IIб |
те же данные, что и при IIa, но более тяжелая сердечная недостаточность с нарушениями кровообращения в большом и малом кругах; злокачественная гипертензия, полисерозиты |
гемодиализ по индивидуальным показаниям; пересадка почки рискованна |
III |
тяжелая уремия, гиперазотемия (мочевина крови - 60 ммоль/л и выше, креатинин – 2,0 ммоль/л и выше, СМ – 1,75 ед. и выше), гиперкалиемия, декомпенсированный метаболический ацидоз, дисфункция внутренних органов |
симптоматическое лечение |
В практике используют также классификацию ХПН, разработанную М.Я. Ратнер с соавт. (1973, 1980), согласно которой выделяются четыре стадии: в I стадии уровень креатинина в плазме крови составляет 0,18 – 0,44 ммоль/л; во II – 0,44 – 0,88; в III – 0,88 – 1,3 и в IV стадии – более 1,3 ммоль/л. К синдромам, частично зависящим от стадии ХПН, авторы относят ацидоз, анемию, азотемическую интоксикацию; к синдромам, не зависящим от стадии ХПН, гипертензию, сердечную недостаточность, гипо- и гиперкалиемию.
Клиника. Течение ХПН чаще медленно прогрессирующее, иногда с многолетним периодом относительной компенсации. За это время у больных наблюдаются периоды ухудшения и ремиссии. Ускоряет развитие и прогрессирование ХПН – обострение основного заболевания, интеркуррентные инфекции, пищевые интоксикации, хирургические вмешательства, травматизация, беременность, гемотрансфузионная реакция, психическая травма.
Обострение характеризуется резким нарушением функции почек, снижением диуреза, бурным нарастанием азотемии, нарушением электролитного состава крови и кислотно-щелочного равновесия, прогрессированием анемии.
В начальной стадии ХПН клиническая картина, как правило, определяется основным заболеванием. При этом на первый план выступают общая слабость, повышенная утомляемость, снижение трудоспособности. При последующих стадиях жалобы больных и клиническая картина обычно объяснимы интоксикацией, свойственной азотемии, и зависят от поражения различных органов и систем.
В начальной стадии ХПН при объективном обследовании выявляется бледность кожных покровов, желтоватый оттенок кожи (задержка урохромов), «синяки». В терминальной стадии частым симптомом является кожный зуд, связанный с выделением через кожу кристаллов мочевины, которая иногда видна в виде своеобразного «инея». Из-за раздражения кожи и слизистых оболочек часто возникают гнойничковые заболевания. Вследствие указанных причин на коже нередко отмечаются следы расчесов. С задержкой «уремических токсинов» связаны парастезии, носовые кровотечения, кровотечения из десен, желудочно-кишечные, маточные, подкожные геморрагии.
С нарушением фосфорно-кальциевого обмена связывают появление остеомаляции, остеосклероза, что клинически проявляется болями в костях. Нарушение экскреции мочевой кислоты со временем может приводить к возникновению вторичной подагры с типичными подагрическими приступами артрита.
Изменения со стороны нервной системы: больные угнетены, характерна частая смена настроения, могут быть подергивания мышц, иногда болезненные судороги икроножных мышц. Со временем усиливаются слабость, сонливость, утомляемость, апатия (уремическая энцефалопатия). В терминальной стадии могут быть тяжелые полинейропатии с болевым и дистрофическим синдромами. На фоне злокачественной гипертензии могут развиваться церебральные инсульты.
Симптоматика со стороны системы дыхания может быть обусловлена как патологией со стороны сердечно-сосудистой системы (сердечная астма), так и раздражением слизистых оболочек верхних и нижних дыхательных путей вследствие викарного выделения мочевины, что приводит к развитию ларингитов, трахеитов, бронхитов, пневмоний. Могут развиваться уремический пневмонит и плеврит, нефрогенный отек легких (вследствие гипергидратации, повышенной проницаемости капилляров и артерий бронхов). Характерны одышка, приступы удушья (острая левожелудочковая недостаточность). Больные при этом занимают вынужденное сидячее положение. В таких случаях рентгенологически выявляется «уремический отек легких» – в виде бабочки. Важным диагностическим моментом является также увеличение массы тела на 3,5 – 5 кг.
Со стороны сердечно-сосудистой системы в начальные стадии ХПН могут отмечаться различные проявления гипертензивного синдрома (неприятные ощущения в области сердца, головная боль, головокружение, признаки левожелудочковой недостаточности от одышки до кардиальной астмы). В дальнейшем поражение системы кровообращения обусловлено развитием уремической интоксикации (уремические миокардиты, перикардиты, болевой синдром, типичный для стенокардии, вплоть до развития инфаркта миокарда). При осмотре определяются приглушенность сердечных тонов, ритм галопа, систолический шум, расширение границ сердца, различные нарушения ритма и проводимости. За счет активации ренин – ангиотензин - альдостероновой системы отмечается повышение артериального давления, причем частота и степень его увеличиваются с нарастанием тяжести уремии. Развитие гипертонии ускоряет темп прогрессирования почечной недостаточности. При злокачественной гипертензии развиваются типичные для нее осложнения (ретинопатия, церебральные инсульты, сердечная астма и др.). В терминальной стадии ХПН развивается перикардит, фибринозный или выпотной, проявляющийся выраженными загрудинными болями, одышкой. Шум трения перикарда выслушивается лучше всего в области нижней трети грудины. До развития методов лечения программным гемодиализом появление шума трения перикарда считалось крайне плохим прогностическим признаком («похоронный звон уремиков»).
Желудочно-кишечные расстройства при ХПН нарастают с повышением уровня азотемии и проявляются извращением вкуса, отвращением к пище, тошнотой, рвотой, икотой, желудочно-кишечными кровотечениями, поносами (реже запорами), стоматитом, глосситом, хейлитом.. Таким образом, поражение желудочно-кишечного тракта при ХПН сопровождается выделительным гастритом, дуоденитом, энтероколитом. В терминальной стадии характерны аммиачный запах изо рта, повышенное слюноотделение, изъязвления слизистой рта.
Суточный диурез в начальных стадиях ХПН (латентной и компенсированной) нормальный или несколько повышен, в интермиттирующей стадии имеется полиурия (2,5 литра в сутки и выше). В терминальной стадии развивается олиго- и анурия.
Характерны множественные эндокринные нарушения, в том числе импотенция, аменорея, гинекомастия и др., связанные с задержкой пролактина.
В терминальной стадии ХПН нарастает неврологическая симптоматика, появляются судорожные подергивания, усиливается энцефалопатия, вплоть до развития уремической комы, с большим шумным ацидотическим дыханием (дыхание Куссмауля). Иногда развивается тяжелая миопатия.
Лабораторные данные: В общем анализе крови при ХПН обнаруживается постепенно нарастающая анемия, токсический лейкоцитоз, достигающий иногда 80 000 – 100 000 со сдвигом лейкоцитарной формулы влево, снижение числа тромбоцитов и их способности к агрегации.
В моче в начале ХПН изменения определяются основным заболеванием, однако, по мере прогрессирования они нивелируются. Ранним симптомом развития почечной недостаточности является снижение относительной плотности мочи до 1,004 – 1,011 независимо от величины диуреза. Часто имеет место никтурия. Прогрессивно снижается скорость клубочковой фильтрации.
В крови повышается уровень мочевины, креатинина, средних молекул, магния, фосфора и калия (в терминальной стадии), снижается уровень кальция. При полиурии отмечается гипокалиемия, метаболический ацидоз. В терминальной стадии ХПН, если развивается олиго- или анурия (что может быть и при обострении основного заболевания в более ранних стадиях) отмечается гиперкалиемия с соответствующей клинической симптоматикой и изменениями на ЭКГ (высокий зубец Т и уширение комплекса QRS).
В диагностике ХПН существенное значение придается установлению размеров почек, которые в подавляющем большинстве случаев уменьшены. Для этого используют методы рентгеновского (обзорная рентгенография почек) и ультразвукового исследования почек. Весьма чувствительным методом раннего выявления снижения функции почек является радиоизотопная ренография. При ХПН ренографические кривые выглядят плоскими и вытянутыми.
Лечение. Начальные стадии ХПН (латентная и компенсированная) – III группа инвалидности, интермиттирующая – II группа, терминальная – I группа инвалидности.
Лечение больных с ХПН является одновременно патогенетическим и симптоматическим и включает мероприятия, направленные на нормализацию артериального давления, коррекцию анемии, водно-электролитных расстройств, предупреждение накопления в организме токсических продуктов обмена. Важнейший компонент комплексного лечения больных с ХПН – диета.
Основная цель диетического питания состоит в снижении содержания мочевины в крови больных. Количество белка в рационе больных, с одной стороны, не должно вызывать прироста азотистых шлаков в крови, с другой – не приводить к распаду собственных белков вследствие белкового голодания. При ХПН применяется диета, разработанная S. Giovanetti и соавт. (1964) несколько модифицированная в последующем. Количества белка с пищей в зависимости от стадии ХПН колеблется от 0,9-1 г до 0,5-0,6 г/кг веса тела. Вместе с тем должен быть обеспечен необходимый калораж питания с достаточным количеством витаминов. С этой целью разработан целый ряд специальных диет: «картофельная», «яблочная», овощная и др.
Количество потребляемой жидкости должно равняться диурезу за предыдущие сутки плюс дополнительно 300 мл (при отсутствии выраженных отеков).
– коррекция ионов калия, ограничение поваренной соли, регуляция белка.
В начальных стадиях ХПН необходимо лечение основного заболевания. Далее – симптоматическая терапия: гипотензивная, витаминотерапия, дезинтоксикационные растворы, натрия гидрокарбонат, сердечные гликозиды.
Лечение анемии: тестостерона пропионат 5%-1,0, препараты железа, с осторожностью – эритропоэтин.
Противоазотемическая терапия: леспенефрил, кофитол, сорбенты, анаболические стероиды, промывание кишечника, слабительные средства, «интестинальный диализ» и др.
В терминальной стадии ХПН применяют экстракорпоральные методы лечения: хронический гемодиализ, перитонеальный диализ, трансплантация почки.
Острая задержка мочеиспускания: первая помощь. Виды катетеров, правила катетеризации мочевого пузыря у мужчин и женщин.
Острая задержка мочеиспускания (ОЗМ) - скопление мочи в мочевом пузыре из-за невозможности самостоятельного мочеиспускания.
Этиология и патогенез
Причины ОЗМ:
Механические:
доброкачественная гиперплазия и рак предстательной железы;
острый простатит;
склероз шейки мочевого пузыря;
инородное тело;
камень и разрыв уретры;
новообразование нижних мочевых путей;
выпадение матки.
Заболевания и повреждения центральной нервной системы - ЦНС (опухоль, травма и т.д.).
Рефлекторные нарушения функции мочевого пузыря.
Отравления психоактивными веществами (снотворные средства, наркотические анальгетики).
В патогенезе ОЗМ участвуют механический и динамический механизмы.
У пожилых мужчин в ответ на постепенно нарастающую инфравезикальную обструкцию (механический фактор) изменяется нервная регуляция - тонус гладкомышечных клеток детрузора повышается, и детрузор гипертрофируется. Гистоморфологическая структура стенки мочевого пузыря постепенно изменяется: мышечные элементы замещаются соединительной тканью, развивается трабекулярность. Объем мочевого пузыря увеличивается. Процесс переходит в стадию декомпенсации - развивается гипотония гладкомышечных клеток детрузора (динамический фактор).
В такой ситуации любой провоцирующий фактор (переохлаждение, прием алкоголя, острой пищи, длительное сидячее положение, запор) вызывает венозный застой в малом тазе, вены шейки мочевого пузыря расширяются, возникает отек предстательной железы, что в свою очередь приводит к деформации, сдавлению простатической части уретры (механический компонент). На фоне уже имеющихся патологических изменений детрузора развивается ОЗМ.
Нередко ОЗМ у пожилых людей возникает после инъекции атропина или его дериватов вследствие снижения тонуса детрузора, чаще при уже имеющемся урологическом заболевании (например, аденома предстательной железы).
Рефлекторная ОЗМ чаще наблюдается после операций, особенно у детей, в связи с нарушением нервной регуляции детрузора и поперечно-полосатого сфинктера мочевого пузыря. Кроме того, она может возникнуть при травме промежности, таза и нижних конечностей, сильных эмоциональных потрясениях, алкогольном опьянении, испуге, истерии.
Часто встречающиеся ошибки терапии
Самолечение, прием диуретиков.
Неправильная, неумелая катетеризация и образование ложных ходов уретры.
На догоспитальном этапе не следует использовать металлический катетер.
Показания к госпитализации
Срочная госпитализация в урологическое отделение показана в случаях:
затрудненной первой катетеризации;
уретроррагии, острого воспаления уретры, органов мошонки и предстательной
железы, травмы уретры;
невозможности проведения катетера (нельзя делать больше 2 попыток);
не увенчавшихся успехом повторных катетеризаций мочевого пузыря.
Алгоритм неотложной помощи при ОЗМ
Причины ОЗМ |
Тактика ведения |
Механические |
Катетеризация мочевого пузыря (при отсутствии противопоказаний), восстановление нормального анатомического положения внутренних половых органов при выпадении матки |
Заболевания ЦНС |
Катетеризация мочевого пузыря |
Рефлекторная ОЗМ при неэффективности - пилокарпин 1 мл 1% раствора или неостигмина метилсульфат (прозерин) 1 мл 0,05% раствора подкожно; при неэффективности - катетеризация мочевого пузыря |
Рефлекторная стимуляция мочеиспускания (орошение наружных половых органов водой, переливание воды из одного сосуда в другой для создания соответствующего звукового эффекта), |
Отравление психоактивными веществами |
Катетеризация мочевого пузыря |
Клиническая картина
Больной беспокоен, испытывает сильные боли в надлобковой области, мучительные позывы к мочеиспусканию, ощущение распирания внизу живота.
Возможные осложнения
У пожилых мужчин ОЗМ часто переходит в хроническую форму и вызывает:
воспаление в мочевых путях (инфекционные агенты могут быть привнесены при катетеризации мочевого пузыря);
хронические цистит и пиелонефрит;
камнеобразование.
При гипотрофированной стенке мочевого пузыря развиваются пузырно-мочеточниково-лоханочные рефлюксы, приводящие к билатеральному уретерогидронефрозу и хронической почечной недостаточности.
Диагностика
Опрос и осмотр
При опросе выясняют:
как пациент мочился до ОЗМ;
какого цвета была моча;
принимал ли он препараты, способствующие ОЗМ.
При осмотре у больных астенического телосложения определяют симптом "шара" в надлобковой области. Перкуторно - над мочевым пузырем тупой звук. Пальпация болезненная из-за сильного позыва к мочеиспусканию.
Дифференциальная диагностика
Острую задержку мочи дифференцируют с анурией: при анурии нет позывов к мочеиспусканию, пальпация надлобковой области не болезненна.
При парадоксальной ишурии мочевой пузырь переполнен, больной не может самостоятельно мочиться, но при этом моча непроизвольно выделяется каплями. После выпускания мочи уретральным катетером ее подтекание прекращается, пока мочевой пузырь снова не переполнится.
Основные направления терапии
Срочное опорожнение мочевого пузыря путем введения эластичного катетера.
Противопоказания к катетеризации мочевого пузыря:
острый уретрит и эпидидимит (орхит);
острый простатит и/или абсцесс предстательной железы;
травма уретры.
В этом случае необходимо прибегнуть к пункции мочевого пузыря, которую выполняют только в урологическом или хирургическом стационаре.
Назначают антибиотики с целью профилактики воспалительных заболеваний органов мошонки и препараты группы b-адреноблокаторов.
Катетеризация мочевого пузыря - Введение катетера (полой резиновой, пластмассовой или металлической трубки) в мочеиспускательный канал и мочевой пузырь с лечебной или диагностической целью. Применяется для отведения мочи при острой (внезапной) и хронической (развившейся постепенно и длительно существующей) задержке мочеиспускания, для введения в мочевые пути лекарств, определения емкости мочевого пузыря, получения мочи для лабораторного исследования, выявления непроходимости мочевых путей и локализации препятствия и т.д. Процедура противопоказана при острых воспалительных процессах в мочеспускательном канале и мочевом пузыре, т.к. способствует распространению инфекции.
Применяют различные виды катетеров:

Виды катетеров:
а) конический с одним отверстием, Нелатона;
б) катетер Робинсона;
в) Whistle-tipуретральный катетер.
г) Катетер Coudé с оливообразным наконечником.
д) Катетер Малекота, самофиксирующийся, 4х «крылый».
е) катетер Малекота, самофиксирующийся, 2х «крылый».
ж) Катетер Пеццера, самофиксирующийся, используется для эпицистостомии.
з) 2х ходовой катетер Фолея, вход для раздутия баллончика в полости мочевого пузыря (i), канал для оттока мочи (ii).
и) 3х ходовой катетер Фолея, вход для раздутия баллончика в полости мочевого пузыря (i), канал для оттока мочи (ii), канал для подключения промывной системы мочевого пузыря (iii).
Процедуру проводят при строгом соблюдении асептики. Руки моют с мылом и протирают спиртом. Наружное отверстие мочеиспускательного канала обрабатывают раствором фурацилина.
У мужчин процедуру выполняют в положении больного на спине со слегка разведенными ногами. Катетер предварительно смазывают стерильным глицерином или вазелиновым (подсолнечным) маслом. Половой член берут левой рукой вблизи головки так, чтобы было удобно раскрыть наружное отверстие мочеиспускательного канала. Катетер вводят правой рукой очень плавно, половой член при этом как бы натягивают на катетер. Больному предлагают сделать несколько глубоких вдохов, на высоте вдоха, когда расслабляются мышцы, закрывающие вход в мочеиспускательный канал, продолжая оказывать мягкое давление, вводят катетер. О его нахождении в мочевом пузыре свидетельствует выделение мочи. Если катетер ввести не удается, то при ощущении сопротивления не следует применять усилий, т.к. это может привести к серьезным травмам.
Катетеризация мочевого пузыря у женщин, как правило, затруднений не вызывает. Наружные половые органы дезинфицируют раствором фурацилина, руки перед процедурой должны быть вымыты с мылом и обработаны спиртом. Пальцами левой руки осторожно раздвигают половые губы, при этом становится видно 2 отверстия: верхнее из них - отверстие мочеиспускательного канала, нижнее - вход во влагалище. Катетер, смазанный стерильным глицерином или вазелиновым маслом, очень плавно, без усилия, вводят правой рукой. Появление мочи - признак того, что катетер находится в мочевом пузыре. При невозможности ввести катетер следует сказать об этом врачу.
Некоторые больные урологическими заболеваниями требуют постоянной катетеризации, иногда несколько раз в день, поэтому родственникам таких больных следует уметь производить катетеризацию. Иногда катетер находится в мочевом пузыре в течение нескольких дней (после операций). В этом случае для предупреждения развития инфекции несколько раз в течение дня следует промывать мочевой пузырь через катетер дезинфицирующим раствором (например, фурацилина). Вначале следует вымыть руки с мылом и протереть их спиртом. Чистыми руками взять стерильный шприц (о стерилизации шприцев см. раздел Инъекции). Не вводя поршень в стеклянный цилиндр, взять цилиндр, снизу плотно закрыть отверстие канюли кусочком стерильной ваты или марли, из флакона с фурацилином налить немного раствора в цилиндр до последней метки на нем, взять поршень и немного ввести его в цилиндр, затем, держа правой рукой поршень, а левой - цилиндр, перевернуть наполненный шприц канюлей вверх и осторожно, вытесняя воздух, ввести поршень. Предварительно обработанный фурацилином катетер берут пальцами левой руки, в правой держат наполненный раствором фурацилина шприц. Канюлю его осторожно продвигают внутрь катетера (если катетер тонкий) или же плотно прижимают к катетеру (если катетер толще, чем диаметр канюли), раствор медленно вводят в мочевой пузырь. Затем шприц отсоединяют, дают введенному раствору вытечь и повторяют процедуру снова. В случае, если длительное нахождение катетера приводит к воспалению мочеиспускательного канала, промывание катетера можетбыть болезненным. Тогда перед введением дезинфицирующего раствора можно ввести в мочевой пузырь немного (5-10 миллилитров) 0,25-0,5 % раствора новокаина (в аптеках можно приобрести препарат в ампулах), катетер на 1-2 минуты пережимают, а затем производят промывание.
После длительного нахождения катетера практически всегда имеется воспаление мочеиспускательного канала (раздражение его резиной, пластмассой, микроцарапины на слизистой). Для профилактики возникновения осложнений перед удалением катетера в мочевой пузырь вводят раствор фурацилина и, не отсоединяя шприца, удаляют катетер. После удаления катетера полезно также в течение нескольких дней делать противовоспалительные ванночки со слабым раствором калия перманганата (марганцовки): кристаллики его разводят в кипяченой воде в банке, наливают теплую кипяченую воду в тазик, добавляют раствор калия перманганата (следить, чтобы не попали кристаллики!) до светло-розового цвета и на несколько минут садятся в тазик. Можно также делать аналогичные ванночки с отваром ромашки, зверобоя, шалфея (способ приготовления растворов: 1 столовая ложка травы на 1 стакан воды, довести до кипения, но не кипятить, дать настояться в течение 5 минут). Ванночки делают несколько раз в день, чем чаще, тем лучше.
Гематурия: виды гематурии, причины возникновения, диагностическая и лечебная тактика врача.
Гематурия - это примесь крови или эритроцитов в моче в микроскопическом или значительном количестве. Гематурия, как правило, является симптомом серьезных заболеваний мочеполовой системы.
Нормальный показатель эритроцитов в моче до 1,2 • 106. При гематурии количество эритроцитов до 3 и более в поле зрения.
При макроскопической гематурии моча внешне окрашена кровью, а если просто повышено содержание эритроцитов, которые можно увидеть только при микроскопическом исследовании, то это - микроскопическая гематурия (эритроцитурия).
Макрогематурия связана с наличием патологии. Следует учитывать, что красный цвет мочи не обязательно обусловлен наличием в ее составе крови, это также может быть воздействие пищевых продуктов или лекарственных препаратов, поэтому до диагностики микроскопией осадка мочи нельзя сделать однозначный вывод.
Симптомы гематурии
При гематурии наблюдается раздражительное нарушение мочеиспускания, учащение мочеиспускания, воспалительный процесс в мочевом пузыре, предстательной железе или мочеиспускательном канале. В этом случае назначается, бактериологические исследования мочи и устранение инфекции антибиотиками. При боли в боковых отделах живота, источником кровотечения являются, вероятнее всего, почки или мочеточник. Боль в животе или функциональная непроходимость кишечника могут быть признаком развития воспалительного процесса, злокачественной опухоли, травмы почки или мочеточника.
Существует 3 категории причин гематурии:
- внепочечные заболевания;
- гломерулярные болезни почек;
- негломерулярные болезни почек.
Почечную гематурию подразделяют на гломерулярную и негломерулярную, которые определяются при проведении фазовоконтрастной микроскопии.
Причины почечной гематурии:
• повышенная проницаемость клубочковых капилляров;
• нестабильность гломерулярной мембраны;
• почечное внутрисосудистое нарушение нормальных свойств белков;
• поражение интерстициальной ткани.
Внепочечная гематурия наблюдается у 65% больных. Возможные причины внепочечной гематурии:
1. Острые инфекции
2. Мочевые камни
3. Доброкачественная гипертрофия предстательной железы
4. Опухоли мочевых путей < br /> Острые инфекционные урологические заболевания такие, как цистит, уретрит и простатит в 20—25% всех случаев являются причиной гематурии.
У всех больных с гематурией и пиурией необходимо получить мочевую культуру; у большинства из них причиной гематурии является острый бактериальный цистит. Однако если посев мочи дает отрицательные результаты, возможной причиной инфекции могут быть хламидии или микобактерии туберкулеза.
Мочевые камни, рак предстательной железы и часто встречающаяся аденома простаты у пожилых мужчин так же могут протекать совместно с гематурией.
В зависимости от локализации источника гематурии ее подразделяют на начальную и терминальную. Различие между этими видами гематурии в том, что при начальной гематурии только первая порция мочи содержит кровь, а при терминальной гематурии наоборот: первая порция мочи не содержит крови, а последняя окрашена ею или несколько капель алой крови выделяется в конце мочеиспускания.
Гематурия - показание для срочного урологического обследования. Экскреторная цистоскопия выявляет расположение источника кровотечения при локализации процесса в верхних мочевых путях или почках.
Почечная колика: этиология, патогенез, диагностика, дифференциальная диагностика. Неотложная и квалифицированная медицинская помощь. Опасности несвоевременного купирования почечной колики и ее осложнений.
ПОЧЕЧНАЯ КОЛИКА — синдром, наблюдающийся при ряде заболеваний почек, основное проявление которых—острые боли в поясничной области.
Этиология и патогенез. Наиболее частыми причинами почечной колики бывают почечнокаменная болезнь, гидронефроз, нефроптоз, при которых нарушается уро-динамика в верхних мочевых путях. Почечную колику могут вызвать обструкция мочеточника сгустком крови, казеозны-ми массами при туберкулезе почек, опухолью, а также поли-кистоз и другие заболевания почек и мочеточников. Ведущая роль в развитии симптомокомплекса принадлежит спазму мочевых путей с их ишемией, растяжению фиброзной капсулы почки и лоханочно-почечному рефлюксу.
Симптомы, лечение. Приступ чаще всего развивается неожиданно в виде сильных болей в поясничной области, но иногда ему предшествует нарастающий дискомфорт в области почки. Ходьба, бег, езда на мотоцикле, поднятие тяжести нередко провоцируют приступ, но он может возникнуть и в покое. Интенсивность боли быстро нарастает, больной мечется, не находя места от боли, громко стонет, держась руками за больной бок. Боль локализуется в поясничной области, но затем перемещается вниз по ходу мочеточника, ирра-диирует в паховую область и половые органы. При исследовании мочи, как правило, обнаруживают эритроциты и небольшое количество белка, иногда—конкременты, сопи, сгустки крови. Нередко при камнях мочеточника почечная колика сопровождается болями в животе, парезом кишечника подобно картине острого живота. В таких случаях дифференциальная диагностика с аппендицитом, холециститом, кишечной непроходимостью и панкреатитом бывает нелегкой, тем более что приступ часто сопровождается тошнотой и рвотой, а наличие эритроцитов в моче не исключает наличия аппендицита. Если камень небольшого размера локализуется в нижнем отделе мочеточника или почечная колика связана с отхождением песка, то возникают частые, болезненные позывы на мочеиспускание. Приступ может сопровождаться ознобом, повышением температуры, тахикардией, лейкоцитозом, повышением СОЭ. Он может быстро закончиться или продолжаться много часов.
Диагноз почечной колики ставят на основании харатерной локализации и иррадиации боли, усиливающейся при пальпации и поколачивании в области почки, на основании изменений мочи, данных хромоцистоскопии и внутривенной урографии. При почечно-каменной болезни и гидронефрозе приступ может возникнуть как днем, так и ночьяо (больные спят на любом боку), при нефроптозе боль чаще возникает днем (больные предпочитают спать на больном боку). При хромоцистоскопии во время приступа индигокармин с больной стороны не выделяется или выделение его значительно запаздывает. Иногда в области устья мочеточника видны буллезный отек, кровоизлияния или ущемленный камень. Вне приступов при гидронефрозе выделение индигокармина всегда замедленно, а при нефроптозе, как правило, нормальное.
Внутривенная урография—наиболее ценный метод диагностики почечной колики и ее дифференциальной диагностики с острыми хирургическими заболеваниями органов брюшной полости. Она позволяет при нефролитиазе обнаружить камень и изменения мочевых путей, при гидронефрозе— расширение лоханки и чашечек, а при нефроптозе—патологическую смещаемость почки и изгиб мочеточника. Внутривенная урография выявляет также другие, более редкие причины почечной колики.
Лечение начинают с применения тепла (грелка, ванна температуры 37— 39 °С), спазмолитических и обезболивающих средств. Приступ могут купировать внутримышечное введение 5 мл раствора баралгина в сочетании с приемом баралгина внутрь по 0,5 г 3 раза в день или подкожные инъекции 1 мл 0,1% раствора атропина в сочетании в 1 мл 2% раствора промедола или 1 мл 2% раствора пантопона (или 1 мл 1 % раствора морфина). При затянувшемся приступе целесообразна новокаиновая блокада семенного канатика (круглой связки матки) со стороны поражения. Почечная колика, сопровождающаяся повышением температуры, — показание к госпитализации в урологическое отделение, где с лечебной целью может быть проведена катетеризация мочеточника.
Прогноз при своевременном и адекватном лечении благоприятный.
Острый пиелонефрит - первичный и вторичный. Клиника. Диагностика. Лечение в зависимости от вида пиелонефрита. Осложнения острого пиелонефрита.
Острый пиелонефрит представляет собой острый воспалительный процесс в почечной паренхиме и чашечно-лоханочной системе. В большинстве случаев он протекает как тяжелое инфекционное заболевание, сопровождающееся выраженной интоксикацией. Острый пиелонефрит может быть первичным, если ему не предшествуют заболевания почек и мочевых путей, и вторичным, если он возникает на почве другого урологического заболевания, «приводящего к нарушению оттока мочи либо расстройству крово-и лимфообращения в почке. Заболевание встречается во всех возрастных группах, однако им чаще болеют дети, а также женщины молодого и среднего возраста.
Острый пиелонефрит составляет 10–15% всех заболеваний почек.В течении острого пиелонефрита различают две стадии: серозное и гнойное воспаление. Гнойные формы пиелонефрита развиваются у 25–30% больных.К тяжелым гнойным воспалительным процессам почки относят апостематозный (гнойничковый) пиелонефрит, карбункул и абсцесс почки. В ряде случаев заболевание может осложниться сосочковым некрозом (некротический папиллит).
Первичный острый пиелонефрит возникает без предшествовавшего заболевания почки или мочевых путей, хотя в большинстве случаев и первичному пиелонефриту предшествуют хотя бы кратковременные и неуловимые обычными методами исследования нарушения уродинамики. При первичном пиелонефрите микроорганизмы проникают в почку гематогенным путем из отдаленных очагов инфекции.
Симптоматика и клиническое течение.
Для первичного острого пиелонефрита характерна триада симптомов — высокая температура тела, боль в поясничной области, изменения в моче, характерные для воспалительного процесса (лейкоцитурия, бактериурия). В клинической картине различают общие и местные симптомы. Первичный острый пиелонефрит сначала проявляется общими симптомами: ознобом, повышением температуры тела до высоких цифр, обильным потоотделением и головной болью (преимущественно в лобных долях), болью в мышцах и суставах, тошнотой, рвотой, общим недомоганием. Язык сухой, обложен. Пульс частый.
Местные симптомы связаны с появлением болей в области почки, пораженной воспалительным процессом (т. е. в поясничной области, в подреберье).Боли могут быть интенсивными, но тупыми и носят постоянный, а не приступообразный характер.Температура тела по вечерам достигает 39–40 ° и снижается к утру до 37,5–38 °С. Симптом Пастернацкого положительный. Мочеиспускание, как правило, не нарушено, кроме тех случаев, когда острый пиелонефрит является осложнением острого цистита либо приводит к воспалительному процессу в мочевом пузыре. Количество мочи чаще уменьшено вследствие обильного потоотделения.
Диагноз.
В диагностике острого первичного пиелонефрита основным критерием являются клиническая симптоматика и результаты лабораторных исследований. В ранней стадии острого первичного пиелонефрита, когда еще отсутствует лейкоцитурия, клиническая картина заболевания нередко ошибочно расценивается как проявление холецистита, аппендицита, гриппа, брюшного тифа и других инфекционных заболеваний. В связи с этим распознавание первичного острого пиелонефрита представляет весьма важную и ответственную задачу.
В анамнезе обращают внимание на наличие гнойных очагов в организме (фурункул, гайморит, пульпит, мастит, остеомиелит и др.), а также на перенесенные инфекционные заболевания (грипп, ангина, пневмония, холецистит, энтероколит и др.). В тех случаях, когда имеются характерные симптомы первичного острого пиелонефрита (повышение температуры тела, боли в поясничной области и изменения в моче, указывающие на воспалительный процесс), распознавание заболевания не вызывает трудностей.
Наибольшее значение в диагностике острого пиелонефрита имеют лабораторные методы исследования, в первую очередь выявление бактериурии и лейкоцитурии с определением их степени, активных лейкоцитов мочи и клеток Штернгеймера — Мальбина. Активные лейкоциты — это лейкоциты, попавшие в мочу из очага воспаления в мочевых путях, активно фагоцитирующие бактерии. При микроскопии осадка мочи отмечается броуновское движение протоплазмы.
Бактериологическое исследование мочи имеет целью не только выяснение характера микрофлоры, но и количественное ее определение, т. е. подсчет количества микроорганизмов в 1 мл мочи.
Для исследования берут среднюю порцию мочи при самостоятельном мочеиспускании после предварительной тщательной обработки наружных половых органов в области наружного отверстия мочеиспукательного канала ватным шариком, смоченным антисептическим раствором (раствор фурацилина 1:5000, 2% раствор борной кислоты и др.). Посев мочи должен быть произведен при комнатной температуре или не позднее 4 ч при хранении в холодильнике (+4 °С).
Важно сочетать бактериологические и бактериоскопические методы выявления бактериурии. У некоторых больных с острым первичным пиелонефритом после применения антибактериальных препаратов спустя 12–24 ч посев мочи уже не дает роста микроорганизмов, хотя микроскопия осадка мочи позволяет еще обнаружить 10 и более бактерий в 1 мл.
.Протеинурия наблюдается у большинства больных, но количество белка в моче не превышает 1 г/л. Реже отмечается небольшая цилиндрурия, которая указывает на вовлечение в воспалительный процесс клубочкового аппарата. Изменения со стороны крови выражаются в виде лейкоцитоза со сдвигом влево формулы белой крови и увеличения СОЭ.
Учитывая принципиальную разницу в лечебной тактике при первичном и вторичном остром пиелонефрите для их дифференциальной диагностики в первую очередь необходимо определить характер оттока мочи из почек. Если он не нарушен, то имеет место первичный пиелонефрит, если нарушен — вторичный.Для этих целей применяют ультразвуковое исследование почек (как менее инвазивный и малотравматичный метод), экскреторную урографию, радиоизотопную урографию и хромоцистоскопию.
Дифференциальная диагностика.
Острый пиелонефрит чаще всего приходится дифференцировать с общими инфекционными заболеваниями (сепсис, грипп и др.), а также с острым аппендицитом и острым холециститом. Трудности в дифференциальной диагностике возникают обычно в первые дни заболевания, когда отсутствуют его характерные клинические симптомы.
Лечение.
При первичном остром пиелонефрите в большинстве случаев лечение консервативное, больной должен быть госпитализирован в стационар.Режим больного — постельный. Рекомендуют обильное питье (соки, морсы) по 2–2,5 л в сутки, пищу, богатую углеводами (пудинги, легкие мучные блюда, сырые и вареные фрукты и т.п.), и кисломолочные продукты (творог, кефир и т.п.). В связи с происходящим при остром пиелонефрите повышенным распадом белка больным назначают парентеральное введение белковых препаратов.При улучшении состояния больного диету расширяют за счет легкоусвояемых белков. Поваренную соль не ограничивают, если у больного нет тяжелого двустороннего поражения почек с повышением артериального давления.
Основной лечебной мерой является воздействие на возбудителя заболевания антибиотиками и химическими антибактериальными препаратами в соответствии с данными антибиограммы, дезинтоксикационная и иммуностимулирующая терапия при наличии иммунодефицита. При остром пиелонефрите лечение следует начинать с наиболее эффективных антибиотиков и химических антибактериальных препаратов, к которым чувствительна микрофлора мочи, чтобы возможно быстрее ликвидировать воспалительный процесс в почке, не допуская перехода его в гнойно-деструктивную форму.
В тех случаях, когда нельзя быстро определить чувствительность возбудителя к современным антибактериальным препаратам, приходится ориентировочно судить о чувствительности по тому виду, к которому относится данный микроорганизм, так как имеются сведения о примерной чувствительности основных возбудителей пиелонефрита к современным антибактериальным препаратам. Если у больного с острым пиелонефритом не удается выделить из мочи возбудителя заболевания, то скорее всего проведенное до поступления в стационар антибактериальное лечение оказалось эффективным и его следует продолжить.
Чтобы уменьшить вероятность рецидива пиелонефрита и перехода его в хроническую форму, антибактериальная терапия должна продолжаться непрерывно не менее 6 нед. Это связано с тем, что при благоприятном течении острого пиелонефрита от момента проникновения инфекции в почку до полной ликвидации воспалительного процесса проходит в среднем 5 нед.В последние годы антибактериальные препараты успешно комбинируют с лекарственными средствами, дающими иммуностимулирующий эффект.
У большинства больных при рано начатом лечении течение острого первичного пиелонефрита благоприятное. Спустя 3–5 сут температура тела снижается до нормальных цифр, улучшается общее состояние, уменьшаются, а затем проходят боли в поясничной области, нормализуется гемограмма, уменьшается токсичность крови по уровню средних молекул, р–2-микроглобулина и парамецийному тесту.
Бактериурия исчезает в течение 7 дней, лейкоцитурия — позже, спустя 7–10 дней после бактериурии. СОЭ уменьшается до нормальных цифр в ближайшие 3–4 нед. Более продолжительное время сохраняется общая слабость, но примерно через 3–4 нед от начала заболевания у большинства больных наступает клиническое выздоровление.У некоторых больных при неблагоприятных условиях (особо вирулентная инфекция, значительное ослабление иммунобиологических сил организма) первичный острый пиелонефрит может протекать бурно; через 2–3 сут развивается апостематозный пиелонефрит или возникают множественные карбункулы почки, вследствие чего необходимо прибегать к оперативному вмешательству — декапсуляции почки, вскрытию гнойников, а при тотальном поражении — нефрэктомии.
При благоприятном течении острого первичного пиелонефрита больные находятся на стационарном лечении в среднем 10— 12 дней, после чего продолжают непрерывный прием антибактериальных препаратов до 6 нед в амбулаторных условиях под систематическим наблюдением уролога и контроля анализов мочи.
При наличии у больного ремиссии заболевания проводят курсы противорецидивного антибактериального лечения продолжительностью 7–10 дней ежемесячно в течение 6 мес. Для лечения целесообразно использовать те препараты, к которым ранее была выявлена чувствительность возбудителя пиелонефрита. В последующем при отсутствии признаков обострения заболевания контрольные обследования больного проводят 1 раз в 3 мес на протяжении 2 лет.
Прогноз.
При остром первичном пиелонефрите прогноз благоприятен, если проведенное антибактериальное лечение привело к стойкой ремиссии заболевания. Если же острый пиелонефрит переходит в хроническую форму, то прогноз становится неблагоприятным при развитии осложнений (хроническая почечная недостаточность, нефрогенная артериальная гипертензия, мочекаменная болезнь, пионефроз).
Вторичный острый пиелонефрит.
Отличается от первичного острого пиелонефрита по клинической картине большей выраженностью симптомов местного характера, что позволяет скорее и легче распознать заболевание.Самой частой причиной вторичного острого пиелонефрита являются камни почки и мочеточника, затем идут аномалии мочевых путей, беременность, стриктура мочеточника и мочеиспускательного канала, аденома предстательной железы, а у детей — вследствие нарушения уродинамики (осложнения в послеоперационном периоде, пузырно-мочеточниковый рефлюкс, мочекаменная болезнь).
Симптоматика и клиническая картина.
При наличии камня или другого окклюзирующего фактора атаке пиелонефрита нередко предшествует типичный приступ почечной колики. Застой мочи и инфекция приводят к более выраженной клинической картине острого пиелонефрита, чем при первичном воспалительном процессе в почке. Самочувствие больного быстро ухудшается: повышается температура тела, которая удерживается на цифрах 38–39 °С, усиливаются общая слабость, адинамия, головная боль, жажда, сухость во рту, появляются рвота, эйфория, тахикардия.
Боли в поясничной области принимают постоянный интенсивный характер. Пальпируется увеличенная и болезненная почка. Усиливается и становится «огненной» болезненность при пальпации в подреберье, резко выражен симптом Пастернацкого. Наблюдается выраженное защитное напряжение поясничных мышц и мышц передней брюшной стенки.
Диагностика.
В анамнезе обращают внимание на бывшие ранее приступы почечной колики и отхождение конкрементов, расстройства мочеиспускания, травмы, перенесенные ранее простатит, уретрит. Из объективных данных наиболее ценными для диагностики вторичного острого пиелонефрита являются высокая, гектического характера температура тела и особенно потрясающий озноб, а также перечисленные выше местные симптомы в области пораженной почки.
Для подтверждения диагноза важное значение имеют лабораторные методы исследования. Бактериурия и лейкоцитурия всегда выражены, кроме случаев полной окклюзии мочеточника пораженной почки. В моче содержится большое число активных лейкоцитов (50% и более) и у большинства больных обнаруживают клетки Штернгеймера — Мальбина. Бактериурия чаще, чем при первичном остром пиелонефрите, обусловлена бактериями группы протея и синегнойной палочкой. Часто наблюдается протеинурия с содержанием белка около 1 г/л. Иммунохимический анализ мочи выявляет наличие среди уропротеинов белков, молекулярная масса которых не превышает 200 000. Тубулярный тип протеинурии сочетается с ее селективным характером. Исследование мочи необходимо проводить несколько раз в течение суток, так как нередко у детей пиурия определяется не во всех порциях мочи.
Как правило, имеется высокий лейкоцитоз крови и сдвиг лейкоцитарной формулы крови влево с нейтрофилезом за счет увеличения палочкоядерных нейтрофилов (до 15–20%, а иногда и более) и с появлением более юных форм. СОЭ всегда увеличена в среднем до 40–45 мм/час. Резко выражена токсичность крови (повышение содержания средних молекул и (3–2-микроглобулина в 3–4 раза, время жизни парамеций в крови менее 20 мин). Для детей с острым гнойным пиелонефритом характерна анемия, обусловленная гемолитическим воздействием инфекции и угнетеним функции кроветворной системы в связи с интоксикацией.
Для установления стороны заболевания при одностороннем пиелонефрите или наибольшего поражения при двустороннем процессе диагностическую ценность имеет определение сравнительного лейкоцитоза. Подсчитывают количество лейкоцитов в крови, взятой из пальца и обеих поясничных областей. Более высокий лейкоцитоз указывает на сторону заболевания.
Содержание мочевины в сыворотке крови бывает повышено примерно у 25–30% больных тяжелым вторичным острым пиелонефритом, так как у многих из них имеется двусторонний воспалительный процесс в почках. При одностороннем заболевании повышение содержания мочевины в сыворотке крови может зависеть от резорбции мочи из пораженной почки вследствие лоханочно-почечных рефлюксов и токсического воздействия на контралатеральную почку.
Хромоцистоскопия у больных вторичным острым пиелонефритом в ряде случаев позволяет установить наличие, степень и причину нарушения пассажа мочи из почки. Удается выявить буллезный отек устья мочеточника при камне в интрамуральном отделе мочеточника или уретероцеле как причину нарушения пассажа мочи.
Рентгенологические методы исследования занимают наиболее важное место в диагностике вторичного острого пиелонефрита. Обзорная рентгенография мочевой системы позволяет выявить дополнительные тени, подозрительные на камни в почке или мочеточнике, а также увеличенные размеры пораженной почки, нечеткость контура поясничной мышцы и легкий сколиоз позвоночника в сторону поражения. На экскреторных урограммах у больных с окклюзией мочевых путей тень рентгеноконтрастного вещества в пораженной почке и по ходу мочеточника или вовсе не определяется, или (при частичной непроходимости) появляется позже, заполняя расширенные выше препятствия мочеточник, лоханку и чашечки. Это лучше определяется на более поздних урограммах (через 40–50 мин, 1,5 ч и позже).Ультразвуковое исследование выявляет расширение чашечно-лоханочной системы, нередко с наличием в ней конкремента.
Ретроградную уретеропиелографию следует выполнять только по строгим показаниям. Она необходима при рентгенонегативных камнях или других причинах нарушения пассажа мочи, которые не удается четко установить без данного исследования, а в то же время нужно срочно решить вопрос об оперативном вмешательстве. При этом катетеризация мочеточника может иметь одновременно и лечебное значение.
Дифференциальная диагностика.
Это обстоятельство облегчает дифференциальную диагностику острого вторичного пиелонефрита с общими инфекционными заболеваниями, острым аппендицитом и острым холециститом. Пальпируемость почки, положительный симптом Пастернацкого, дизурия, бактериурия, лейкоцитурия, большое количество активных лейкоцитов в моче, снижение или отсутствие функции почки на стороне заболевания свидетельствуют в пользу острого вторичного пиелонефрита.
Лечение.
При вторичном остром пиелонефрите лечение следует начинать с восстановления пассажа мочи из почки, что является принципиальным.При остром пиелонефрите, вызванном окклюзией мочеточника камнем небольших размеров, что позволяет надеяться на его самостоятельное отхождение в дальнейшем, и в ранние сроки (от 1 до 3 сут) от начала острого воспалительного процесса в почке попытка восстановления оттока мочи может быть предпринята с помощью катетеризации мочеточника. Если удается провести катетер мимо камня в лоханку, эвакуация ее содержимого приводит к быстрому купированию атаки пиелонефрита.
Если же катетеризация лоханки по тем или иным причинам (чаще всего в связи с непреодолимым препятствием в месте нахождения в мочеточнике камня) не удается, а лекарственная терапия не приводит к ликвидации атаки пиелонефрита в течение первых 3 сут, то производят экстренное оперативное вмешательство — уретеролитотомию, либо дренирование почки малотравматическим чрескожным пункционным методом под контролем ультразвука (чрескожная пункционная нефростомия).
Применение самоудерживающегося мочеточникового катетера (стент) позволяет не только купировать атаку пиелонефрита, но и произвести экстракорпоральное дробление камня в лоханке почки энергией ударной взрывной волны. Кроме этого, камень может быть извлечен из почки с помощью чрескожной пункционной нефростомии (механически, специальным инструментом), либо раздроблен в лоханке ударными волнами (через чрескожную нефростому). Данный катетер (стент) обеспечивает свободный отток мочи из почки после дробления камня, исключает окклюзию мочеточника фрагментами конкремента и способствует профилактике острого вторичного пиелонефрита.
При вторичном остром пиелонефрите в ранней стадии заболевания (2–3 сут), когда предполагают наличие серозного или незначительного гнойного воспалительного процесса в почке, можно ограничиться удалением камня из лоханки или мочеточника без дренирования лоханки почки. В более поздние сроки заболевания (4–6 сут), когда уже возник гнойно-некротический процесс в почке, удаление камня почки или мочеточника должно сопровождаться обязательным дренированием лоханки почки путем пиело-или нефростомии с одновременной декапсуляцией почки.
В еще более поздние сроки гнойно-воспалительного процесса в почке с признаками выраженной интоксикации организма основная цель оперативного вмешательства состоит в дренировании и декапсуляции почки, а устранение причины возникновения вторичного острого пиелонефрита (например, удаление камня мочеточника) допустимо лишь в том случае, если оно не усложняет операцию и не отягощает состояние больного. При множественных карбункулах почки, гнойном расплавлении ее паренхимы, пионефрозе и хорошей функции контралатеральной почки прибегают к нефрэктомии.
Консервативное лечение с острым пиелонефритом при наличии окклюзии мочевых путей не приносит успеха, несмотря на применение самых мощных антибиотиков и химических антибактериальных препаратов. И наоборот, своевременное устранение препятствия оттоку мочи или самостоятельное отхождение мелкого камня в мочеточнике приводит к быстрому купированию атаки острого пиелонефрита. В связи с этим основной задачей лечения больных острым вторичным пиелонефритом является быстрое восстановление оттока мочи.
Прогноз.
При вторичном остром пиелонефрите прогноз менее благоприятен, чем при первичном, так как у этих больных воспалительный процесс в почке гораздо чаще переходит в хроническую форму, либо осложняется гнойно-деструктивным и изменениями в почке, требующими нефрэктомии. Успех лечения пиелонефрита, а следовательно, и его прогноз в основном зависят от своевременности восстановления оттока мочи из почки.
Хронический пиелонефрит: этиопатогенез, диагностика, стадии, лечение. Критерии эффективности диспансерного наблюдения.
Хронический пиелонефрит, как правило, является следствием острого пиелонефрита. Наиболее важные причины перехода острого инфекцйонно-воспалительного процесса в почке в хронический следующие:
1. Своевременно нераспознанные и неустраненные причины нарушений оттока мочи (мочекаменная болезнь,стриктуры мочевых путей, аденома предстательной железы, пузырно-мочеточниковые рефлюксы, нефроптоз и др.)
2. Неправильное или недостаточное по длительностилечениеострого пиелонефрита, а также отсутствие систематического диспансерного наблюдения за больными, перенесшими острый пиелонефрит.
3. Образование форм бактерий и протопластов при пиелонефрите, которые способны длительное время находиться в межуточной ткани почки в неактивном состоянии, а приснижении защитных иммунных сил организма переходить в исходное состояние и вызывать обострение заболевания.
4. Хронические сопутствующие заболевания (сахарный диабет, ожирение, болезни желудочно-кишечного тракта, тонзиллит и др.), ослабляющие организм и являющиеся постоянным источником инфицирования почек.
5. Иммунодефицитные состояния.
Хронический пиелонефрит нередко начинается в детском возрасте, чаще у девочек, после типичной атаки острого пиелонефрита. Во время или после перенесенных острых инфекционных и вирусных заболеваний (грипп, ангина, пневмония, отит, энтероколит и др.) наступают новые обострения хронического пиелонефрита, которые нередко маскируются указанными заболеваниями и проходят незамеченными. Ослабление организма перенесенным инфекционным процессом и недостаточное антибактериальное лечение способствуют прогрессированию хронического пиелонефрита. В дальнейшем течение его у ребенка имеет волнообразный характер. Фаза ремиссии заболевания сменяется латентной фазой воспалительного процесса, а затем и активной.
Симптоматика и клиническое течение. Хронический пиелонефрит годами может протекать без четких клинических симптомов вследствие вялотекущего воспалительного процесса в межуточной ткани почки. Проявления хронического пиелонефрита во многом зависят от активности, распространенности и стадии воспалительного процесса в почке.
ФАЗЫ:
Латентная
Активная
Ремиссии
Диагноз. В диагностике хронического пиелонефрита существенную помощь оказывает правильно собранный анамнез. Необходимо с настойчивостью выяснить у больных перенесенные в детстве заболевания почек и мочевых путей. У женщин следует обращать внимание на отмечавшиеся во время беременности или вскоре после родов атаки острого пиелонефрита или острого цистита. У мужчин особое внимание необходимо уделить перенесенным травмам позвоночника, мочеиспускательного канала, мочевого пузыря и воспалительным заболеваниям мочеполовых органов.
Необходимо также выявлять наличие факторов, предрасполагающих к возникновению пиелонефрита, таких, как аномалии развития почек и мочевых путей, мочекаменная болезнь, нефроптоз, сахарный диабет, аденома предстательной железы и др.
Лейкоцитурия является одним из наиболее важных и часто встречающихся симптомов хронического пиелонефрита. Однако общий анализ мочи малопригоден для выявления лейкоцитурии при пиелонефрите в латентной фазе воспаления. Неточность общего анализа заключается в том, что при нем строго не учитывают количество надосадочной мочи, остающейся после центрифугирования, размеры капли, взятой для исследования, и покровного стекла. Почти у половины больных с латентной фазой хронического пиелонефрита лейкоцитурию не обнаруживают при общем анализе мочи. Вследствие этого при подозрении на наличие хронического пиелонефрита показано выявление лейкоцитурии с помощью методов Каковского — Аддиса (содержание лейкоцитов в суточной моче), Амбюрже (количество лейкоцитов, выделяющихся за 1 мин), де Альмейда — Нечипоренко (количество лейкоцитов в 1 мл мочи), Стенсфилда — Вебба (количество лейкоцитов в 1 мм3 нецентрифугированной мочи). Из перечисленных выше наиболее точным является метод Каковского — Аддиса, так как мочу для исследования собирают в течение большого промежутка времени. Однако, чтобы избежать при этом ложноположительных результатов, мочу следует собирать в две емкости: в одну собирают первые порции мочи (по 30–40 мл при каждом мочеиспускании), а в другую — остальную мочу. Поскольку первая порция содержит большое количество лейкоцитов за счет смыва из мочеиспускательного канала, ее используют лишь для учета общего количества выделенной мочи. Исследование мочи из второй емкости позволяет определить лейкоцитурию мочепузырного или почечного происхождения.
Если врач предполагает наличие у больного хронического пиелонефрита в фазе ремиссии, применяют провокационные тесты (преднизолоновый или пирогеналовый). Введение преднизолона или пирогенала провоцирует у больного хроническим пиелонефритом выход лейкоцитов из очага воспаления. Появление лейкоцитурии после введения преднизолона или пирогенала свидетельствует о наличии хронического пиелонефрита. Данный тест становится особенно убедительным, если в моче одновременно обнаруживают активные лейкоциты и клетки Штернгеймера — Мальбина.
Диагностическое значение при хроническом пиелонефрите имеют также уменьшение осмотической концентрации мочи (менее 400 мосм/л) и снижение показателей клиренса эндогенного креатинина (ниже 80 мл/мин). Уменьшение концентрационной способности почки может нередко наблюдаться и в более ранних стадиях заболевания. Оно свидетельствует о нарушении способности дистальных отделов канальцев поддерживать осмотический градиент в направлении кровь — канальцы. Отмечается также снижение канальцевой секреции как более ранний симптом хронического пиелонефрита.
Существенную помощь в диагностике хронического пиелонефрита оказывают рентгенологические методы исследования. Основными рентгенологическими симптомами заболевания являются следующие: 1) изменения размеров и контуров почек; 2) нарушения выделения почкой рентгеноконтрастного вещества; 3) патологические показатели ренально-кортикального индекса (РКИ); 4) деформация чашечно-лоханочной системы; 5) симптом Ходсона; 6) изменения ангиоархитектоники почки.
На обзорной рентгенограмме при хроническом пиелонефрите находят уменьшение размеров одной из почек, заметное повышение плотности тени и вертикальное расположение оси пораженной почки.
Экскреторная урография в различных модификациях является основным методом рентгенодиагностики хронического пиелонефрита. Рентгенологическая картина хронического пиелонефрита отличается полиморфизмом и асимметрией изменений, которые зависят от соотношения инфильтративно-воспалительных и рубцово-склеротических процессов.
Для хронического пиелонефрита характерна асимметрия поражения почек и снижения их функции, которая более четко выявляется на экскреторных урограммах, произведенных в ранние сроки (через 1, 3, 5 мин) после введения рентгеноконтрастного вещества и отсроченных (через 40 мин, 1 ч, 1,5 ч). На поздних урограммах определяется замедление выделения рентгеноконтрастного вещества более пораженной почкой вследствие задержки его в расширенных канальцах.
В I стадии хронического пиелонефрита, когда преобладают инфильтративные процессы, на рентгенограммах обнаруживают раздвигание чашечек, спазм их шеек и лоханки. Поскольку спазмы продолжаются 20–30 с, их чаще выявляют по данным урокинематографии, чем экскреторной урографии.
Во II стадии пиелонефрита, когда развиваются рубцово-склеротические изменения, появляются симптомы снижения тонуса чашечек лоханки и верхней трети мочеточника в виде умеренного их расширения и симптома края поясничной мышцы (в месте соприкосновения лоханки и мочеточника с краем поясничной мышцы наблюдается ровное уплощение их контура).
Появляются различные деформации чашечек: они приобретают грибовидную, булавовидную форму, смещаются, шейки их удлиняются и суживаются, сосочки сглаживаются.
Ретроградную пиелографию применяют при хроническом пиелонефрите крайне редко в связи с опасностью инфицирования почки, особенно госпитальными штаммами бактерий.
При хроническом пиелонефрите происходит постепенное уменьшение паренхимы почки, которое может быть более точно определено с помощью ренально-кортикального индекса (РКИ). Он представляет собой показатель отношения площади чашечно-лоха-ночной системы к площади почки. Ценность РКИ заключается.в том, что он указывает на уменьшение почечной паренхимы у больных хроническим пиелонефритом в I и II стадиях заболевания, когда без расчетного метода это установить не удается.
Важные сведения об архитектонике почки при хроническом пиелонефрите позволяет установить почечная артериография. Различают три стадии сосудистых изменений в почке при хроническом пиелонефрите. Из радиоизотопных методов исследования при хроническом пиелонефрите применяют ренографию как метод раздельного определения функции почек и установления стороны наибольшего поражения. Метод позволяет также осуществлять динамический контроль восстановления функции почки в процессе лечения.
Для определения количества и качества функционирующей паренхимы целесообразно применение динамической сцинтиграфии. При сегментарном поражении почки динамическая сцинтиг-рафия выявляет задержку транспорта гиппурана в зоне рубцово-склеротических изменений.
Дифференциальная диагностика.Хронический пиелонефрит чаще всего приходится дифференцировать от туберкулеза почки и гломерулонефрита. В пользу туберкулеза почки свидетельствуют перенесенный туберкулез других органов, дизурия, гематурия, рубцовые сужения верхних мочевых путей, протеинурия, менее выраженное преобладание лейкоцитурии над эритроцитурией. Достоверными признаками нефротуберкулеза являются: нахождение микобактерий туберкулеза в моче, стойко кислая реакция мочи, типичная картина туберкулезного Поражения мочевого пузыря при цистоскопии и характерные рентгенологические признаки заболевания.
Лечение. При хроническом пиелонефрите лечение должно предусматривать следующие основные мероприятия: 1) устранение причин, вызвавших нарушение пассажа мочи или почечного кровообращения, особенно венозного; 2) назначение антибактериальных средств или химиопрепаратов с учетом данных антибиограммы; 3) повышение иммунной реактивности организма.
Прогноз. При хроническом пиелонефрите прогноз находится в прямой зависимости от длительности заболевания, активности воспалительного процесса и частоты повторных атак пиелонефрита. Особенно ухудшается прогноз, если заболевание начинается в детском возрасте на почве аномалий развития почек и мочевых путей. Поэтому оперативная коррекция должна выполняться в самые ранние сроки выявления этих аномалий. Хронический пиелонефрит является наиболее частой причиной хронической почечной недостаточности и нефрогенной артериальной гипертензии. Прогноз становится особенно неблагоприятным при сочетании этих осложнений.
Паранефрит. Этиология. Клинические проявления. Принципы лечения.
Паранефрит - воспалительный процесс в околопочечной жировой клетчатке. Вокруг почки всегда имеется определенное количество жировой ткани. Эта ткань выполняет функцию поддержания почки и фиксации ее на нормальном месте, амортизационную функцию – защищает почку от травм.
Паранефрит вызывают те же микроорганизмы, что и пиелонефрит, но чаще всего в околопочечной жировой клетчатке обнаруживаются стафилококки и кишечная палочка. В настоящее время благодаря широкому применению антибиотиков паранефрит встречается значительно реже.
Паранефрит бывает :
первичный
вторичный.
Первичный паранефрит - если заболевание самой почки отсутствует. Это происходит, когда микробы заносятся в околопочечную клетчатку из других очагов воспаления (фурункул, остеомиелит, гнойная ангина) с кровью. Чаще это бывает при снижении защитных сил организма, вызванных переохлаждением, перегреванием, нарушениями иммунитета. Паранефрит может возникнуть после травмы поясничной области или проникающего ранения. Иногда к паранефриту приводят протекающие рядом воспалительные процессы соседних органов – матки, яичников, прямой кишки, аппендиците.
Вторичный паранефрит обычно бывает осложнением гнойно-воспалительного процесса в почке (абсцесс почки, карбункул почки, пионефроз.). По расположению в почечной клетчатке паранефрит может быть передним, задним, верхним, нижним или тотальным, когда воспалительный процесс поражает всю околопочечную клетчатку.
По течению паранефрит может быть острый и хронический. Если паранефрит долго протекает без лечения, он может распространиться на окружающие ткани и органы и вызвать перитонит (воспаление брюшины), гной из околопочечной клетчатки может проникнуть в кишку, плевральную полость, в мочевой пузырь. В начале заболевания у пациента может быть повышение температуры тела до 38-40 градусов, озноб, плохое самочувствие. Боль в поясничной области могут появиться значительно позже, иногда через 4-5 суток.
При остром начале паранефрита у больного могут появиться сильные боли. Из-за боли может появиться вынужденная поза больного лежа на боку с подтянутой к животу и согнутой в колене ногой. При этом разгибание ноги приводит к резкому усилению болей. В области поясницы может быть обнаружена припухлость и покраснение. Иногда паранефрит может имитировать острый аппендицит, абсцесс поддиафрагмального пространства, пневмонию.
Хронический паранефрит обычно протекает малозаметно. Постепенно на месте воспалительных очагов формируется соединительная ткань, околопочечная жировая клетчатка уплотняется и в конечном итоге почка оказывается замурованной в плотном слое склерозированной ткани.
Диагностику паранефрита осуществляют при помощи рентгенологических методов, контрастирования. Ультразвуковое исследование помогает уточнить расположение очага гнойного воспаления в жировой клетчатке. Для уточнения диагноза проводят пункцию околопочечной клетчатки, и содержимое пункции исследуют на наличие микроорганизмов и их чувствительность к антибактериальным препаратам. Значительно сложнее диагностировать хронический паранефрит и иногда он долгое время остается нераспознанным.
Лечение паранефрита. Если паранефрит выявлен на ранней стадии развития воспалительного процесса, для полного выздоровления пациента бывает достаточно назначения антибактериального препарата. Чаще назначают антибиотики пенициллинового ряда, цефалоспорины (цефотаксим, цефаклор), макролиды (эритромицин, азитромицин), аминогликозыды и фторхинолоновые препараты. Обязательно проводят лечение других очагов инфекции в организме и назначают препараты для повышения иммунной защиты организма. Если течение паранефрита тяжелое, проводят оперативное лечение, гнойный очаг вскрывают и оставляют дренаж. Если очаг гнойного расплавления небольшой возможно проведение пункции очага и удаление гнойного содержимого под контролем ультразвукового исследования. Если у пациента выявляют хронический пиелонефрит, его также лечат антибактериальными препаратами, только в этом случае лечение более длительное и обязательно назначаются физиотерапевтические процедуры.
Острый и хронический цистит. Этиология и патогенез. Стадии течения. Дифференциальная диагностика. Лечение. Профилактика.
Цистит - воспаление слизистой оболочки мочевого пузыря. Это одно из самых распространенных воспалительных заболеваний мочеполовых органов. Около 20-25 процентов женщин переносят цистит в той или иной форме, а 10 процентов страдают хроническим циститом, и цифры эти с каждым годом неуклонно растут. Мужчины страдают этим заболеванием гораздо реже - цистит встречается только у 0,5% мужчин.
Различают первичный и вторичный цистит, острый и хронический, инфекционный (специфический или неспецифический) и неинфекционный (химический, термический, токсический, аллергический, лекарственный, лучевой, алиментарный и др.). Вторичный цистит развивается на фоне заболеваний мочевого пузыря (камни, опухоль) или близлежащих органов (аденома и рак предстательной железы, стриктура уретры, хронические воспалительные заболевания половых органов). Цистит с преимущественной локализацией воспалительного процесса в области мочепузырного треугольника обозначают термином «тригонит».
Острый первичный цистит – это в основном чисто женское заболевание. Его возникновение связано с переохлаждением, перенесенной инфекцией, инструментальным исследованием, пренебрежением правилами личной гигиены. Одним из предрасполагающих факторов развития цистита является сахарный диабет. Развитие цистита также возможно вследствие аллергической реакции организма.
Предрасполагающими факторами для развития цистита являются травма его слизистой оболочки, частой крови в венах таза, гормональные нарушения, авитаминозы, переохлаждение и др. Большое значение имеет нарушение уродинамики, в том числе затрудненное или неполное опорожнение мочевого пузыря, приводящее к нарушению тонуса детрузора, застою или разложению мочи. При инфекционном цистите возможны восходящий, нисходящий, лимфогенный и гематогенный пути инфицирования.
К основным морфологическим признакам хронического цистита относят: метаплазию эпителия с формированием слизистых кист или ороговение его с образованием беловатых бляшек; изредка — полипозные разрастания, мелкие лейкоцитарные инфильтраты в подэпителиальном слое, напоминающие фолликулы. Глубокое поражение стенки мочевого пузыря приводит к склерозу соединительной ткани между мышечными волокнами, следствием чего является сморщивание мочевого пузыря. Для интерстициального цистита характерны изъязвление слизистой оболочки (эпителий в области язв отсутствует), гиалиноз и наличие множества тучных клеток в стенке мочевого пузыря. При аллергическом цистите в подэпителиальном и в мышечном слоях обнаруживают эозинофильные инфильтраты, тесно связанные с сосудами.
Лечение цистита
При остром цистите рекомендуют покой, щадящую диету, обильное питье (до 2—2,5 л жидкости в сутки); следует избегать переохлаждения тела, следить за регулярной функцией кишечника, исключить половые сношения. При выраженных болях назначают ректальные или вагинальные свечи с анальгетиками. Промывание мочевого пузыря при остром цистите противопоказано. Антибактериальную терапию проводят с учетом антибиотикограммы, до получения которой назначают антибиотики широкого спектра действия, нитрофураны, антигистаминные препараты. В лечении первичного хронического цистита важное место занимают выявление и санация очагов инфекции, у женщин — лечение гинекологических заболеваний или влагалищной инфекции. Для устранения инфекции нижних мочевых путей у мальчиков проводят лечение заболевания, с которым связано ее возникновение. У мужчин при выявлении основного заболевания показано соответствующее лечение — устранение причины нарушения оттока мочи. Противовоспалительная терапия хронического цистита целесообразна в течение 3—4 нед. (по антибиотикограмме), затем на длительное время (3—6 мес.) назначают нитрофураны или бактрим. Необходимо проводить ежемесячно бактериологическое исследование мочи, особенно в первые 6 мес. после прекращения приема лекарств. Выявление инфекции является показанием для повторного курса противовоспалительной терапии. У детей посевы мочи при стерильной моче следует проводить каждые 6—12 мес. до наступления пубертатного периода.
Лечение хронического цистита, особенно интерстициального, у женщин представляет значительные трудности. Целесообразно применение антигистаминных и гормональных препаратов (гидрокортизон, преднизолон), возможны гепаринотерапия (инстилляция и инфузионная терапия). Местно в качестве обволакивающих средств применяют вазелиновое масло, линимент дибунола, рыбий жир, а также препараты серебра, гидрокортизон, облепиховое масло, метилурацил.
При интерстициальных циститах назначают физиотерапевтические процедуры — ультразвуковую терапию, диатермию, электрофорез с раствором новокаина, ганглерона и ферментов, электростимуляцию мочевого пузыря. Применяют предпузырную, пресакральную и внутрипузырную новокаиновые блокады, растяжение сморщенного мочевого пузыря под наркозом. При рубцовом сморщивании мочевого пузыря показана хирургическая операция (уретероуретероанастомоз, односторонняя нефростомия, уретеросигмоанастомоз, илеоцистопластика).
Расстройства мочеиспускания, их причины и способы устранения.
В медицине все расстройства мочеиспускания объединяют в понятие дизурии.
В норме в течение суток здоровый человек выделяет в среднем 1.500-2 л мочи, это составляет около 75% принятой за сутки жидкости, остальные 25% выделяются легкими при дыхании, кожей, кишечником. Нормальная частота мочеиспускания колеблется от 4 до 6 раз в сутки. Мочевой пузырь опорожняется полностью. Акт мочеиспускания не должен приносить дискомфорта.
Мочеиспускание у человека — акт произвольный, полностью зависящий от сознания, т.е. позыв на мочеиспускание может быть подавлен даже при переполнении мочевого пузыря. Физиологическая емкость мочевого пузыря составляет 250—300 мл.
Среди расстройств акта мочеиспускания выделяют:
Поллакиурия – учащение мочеиспускания, характерно для заболеваний нижних мочевых путей и предстательной железы. Может быть резко выраженным — 15—20 раз в сутки и более. При каждом мочеиспускании выделяется небольшое количество мочи; общее количество, выделенное за сутки, не превышает нормы. Если же учащение мочеиспускания сопровождается выделением больших порций мочи, а суточный диурез значительно превышает норму, то это признак поражения механизма мочеотделения (диабет, хроническая почечная недостаточность и др.). Поллакиурия иногда сопровождается императивными (повелительными) позывами на мочеиспускание. Поллакиурия наблюдается:
днем и при движении, исчезая ночью и в покое - обычно бывает при камнях в мочевом пузыре.
ночная поллакиурия нередко имеет место при опухолях предстательной железы.
постоянная поллакиурия наблюдается при хронических заболеваниях мочевого пузыря, может возникнуть и при приеме некоторых лекарственных средств, например диуретиков.
Олигакиурия — редкое мочеиспускание
Никтурия, или ночная поллакиурия — преобладание ночного диуреза над дневным за счет количества мочи и частоты мочеиспускания. Бывает при образовании скрытых отеков в дневное время при ходьбе и физической нагрузке и уменьшением их ночью, может сопровождать диабет и заболевание предстательной железы.
Странгурия — затруднение мочеиспускания в сочетании с его учащением и болью.
Недержание мочи — непроизвольное выделение (утечка) мочи без позывов на мочеиспускание. Недержание мочи разделяют на:
стрессовое — недержание мочи при напряжении;
ургентное (императивное) – как следствие неудержимого позыва к акту мочеиспускания;
недержание мочи вследствие переполнения мочевого пузыря при отсутствии позыва к мочеиспусканию.
Количественные изменения мочи
Полиурия — патологическое увеличение количества выделяемой мочи. Больной выделяет более 2000 мл мочи. Полиурия как правило сопровождается поллакиурией и при каждом мочеиспускании выделяется большое количество мочи.
Полиурия характерна для:
хронического пиелонефрита,
поликистоза почек,
доброкачественной гиперплазии (аденоме) предстательной железы.
Опсоурия — позднее отделение большого количества мочи — через 1 сут и более после предшествовавшего обильного приема жидкости. Наблюдается чаще всего при сердечной недостаточности, может быть симптомом заболевания печени и поджелудочной железы.
Олигурия - уменьшение количества выделяемой мочи. При олигурии количество выделяемой за сутки мочи колеблется от 100 до 500 мл.
Анурия — прекращение поступления мочи в мочевой пузырь. Это состояние связано с тем, что моча либо не выделяется почечной тканью, либо не достигает мочевого пузыря вследствие закупорки верхних мочевых путей. При анурии позывы на мочеиспускание отсутствуют, из мочевого пузыря путем его катетеризации можно получить лишь небольшое (не более 20-30 мл) количество мочи.
Острый орхоэпидидимит: диагностика, способы лечения.
Орхит - это воспаление яичка, а эпидидимит - воспаление придатка яичка. Из-за тесной взаимосвязи между ячиком и его придатком воспалительный процесс вовлекает вместе эти два органа (орхоэпидидимит).
Причины развития орхоэпидидимита.
Чаще всего бывает инфекция, которая попадает из мочеиспускательного канала, предстательной железы, мочевого пузыря по семявыносящему протоку. Возможно и гематогенный путь распространения инфекции.
Симптомы.
Острый орхоэпидидимит начинается болью в яичке, поднимается температура тела до 39 гр. Яичко с придатком увеличиваются в размерах. Кожа мошонки становится гиперемированной. Отсрый период длится около недели, а затем боль стихает, температура тела нормализовывается. Такое течение встречается наиболее чаще. Однако, при несвоевременном лечении, острый период может осложниться абсцессом яичка или придатка. Кожа мошонки над местом абсцедирования становится ярко-красной, блестящей и резко болезненной при ощупывании.
Лечение.
Лечение острого орхоэпидидимита должно быть только в условиях стационара. Основной смысл в госпитализации заключается в предотвращении перехода серозной фазы воспаления в гнойную (абсцесс яичка и придатка). Лечение направлено на улучшение гемодинамики и лимфоттока в яичке и придатке. Для этого яичку придают возвышенное положение, назначают препараты улучщающие микроциркуляцию. Для уменьшения остроты воспаления местно прикладывают лед или холодные компрессы. С первого дня заболевания назначают антибиотики широкого спектра действия. В острый период применяют физиотерапевтические методики (УВЧ). Хорошим эффектом обладают новокаиновые блокады с антибиотиком и гидрокортизоном в семенной канатик. Нельзя забывать о местном использовании димексидовых аппликаций с антибиотиком и рассасывающими препаратами.
Прогноз.
Как правило, при гнойной форме орхоэпидидимита ткань яичка подвергается рубцеванию и атрофии. Воспалительный процесс в придатке может закончиться облитерацией семявыносящего протока. В случае двустороннего поражения может стать причиной обтурационной формы экскреторного бесплодия.
Острый и хронический простатит: классификация, симптоматика, диагностика, лечение.
Простатит (prostatitis) — воспаление предстательной железы. Предстательная железа — мужской орган, вследствие чего простатит может быть только у мужчин.
Различают следующие категории простатита:
Острый (бактериальный) простатит.
Хронический бактериальный простатит.
Острый простатит
Острый бактериальный простатит имеет инфекционное происхождение. Простатит появляется по причине попадания инфекции в мочеиспускательный канал(ифицирование мочеполовой системы)
Симптомы острого простатита
Острый простатит характерен своими симптомами интоксикации организма; повышение температуры, частое мочеиспускание с резкой болью, чувство жжение промежности, снжение напора струи мочи, боли в прямой кишке при испражнении. Поражение простаты проявляется болью в пояснице и паховой области. Так же присутствуют болезненные ощущения при мочеиспускании и частые позывы (особенно ночью). Иногда появляются гнойные выделения из мочеиспускательного канала. Локальный воспалительный процесс в предстательной железе, может дать начало сепсису (заражению крови), в таких случаях, общее состояние больного расценивается как критическое и требует экстренной медицинской помощи.
Лечение острого простатита
Для лечения острого простатита применяют антибактериальные препараты широкого спектра действия, рассчитанные на борьбу с различными типами инфекции. Показаниями к госпитализации является тяжёлое состояние больного с признаками тяжёлой интоксикации. При неосложнённом течении больные острым простатитом лечатся амбулаторно.
Прогноз
Для острого простатита характерно 95% - е выздоровление. Но иногда могут наступить осложнения в виде абсцессов.
Хронический простатит
Хронический бактериальный простатит развивается после перенесённого острого простатита и характеризуется длительным протеканием с фазами обострения и иллюзорного выздоровления. Факторами, предрасполагающими к хроническому простатиту, являются:
- Частое переохлаждение
- Гиподинамия (малоподвижный образ жизни)
- Заболевания мочеполовой системы.
- Табакокурение и неумеренное употребление алкоголя.
Признаки и симптомы
Простатит часто протекает бессимптомно или с неярковыраженной клинической картиной. Хронический простатит может стать причиной частых рецидивов цистита (воспалительный процесс мочевого пузыря), так как очаг воспаления в предстательной железе служит хранилищем инфекции для последующего заражения мочеполовой системы.
Лечение хронического простатита
В лечении хронического бактериального простатита используют длительные курсы антибактериальной терапии (6-8 недель). Лечение хронического простатита более длительное, чем острого, и иногда включает курс массажа простаты для улучшения кровообращения.
Регулярный секс является хорошей профилактикой простатита. Кроме того, необходимо периодически проверяться на наличие урологических инфекций и заболеваний. Раз в год надо желательно посетить уролога.
Симптомы простатита:
• Сложности при мочеиспускании – частое и болезненное мочеиспускание, учащенные позывы на мочеиспускание и боль во время мочеиспускания, слабая струя мочи. Необходимо не забывать, что частое мочеиспускание является нередко признаком сахарного диабета. Диабет в этом отношении отличается от простатита присутствием сильной жажды.
• Расстройство сексуальной функции – низкая сексуальная потребность, боль при семяизвержении, ухудшение эрекции, ее неполнота и кратковременность.
• Болевые ощущения в промежности. Боль при мочеиспускании тревожит многих заболевших. Боли при половом акте встречаются у 10-15% больных.
Длительное воспаление предстательной железы приводит к возникновению сексуальной дисфункции: сниженная эрекция, болезненное семяизвержение, истекание секрета простаты при напряжении. Присутствие хронического воспалительного процесса снижает концентрацию сперматозоидов в сперме, что иногда становится причиной бесплодия.
Туберкулез почки и мочевого пузыря – симптоматика, диагностика, лечение.
Туберкулез мочевой системы составляет 30-40 % внелегочных форм заболевания и занимает среди них 1-е место. Мужчины и женщины страдают одинаково часто, при этом наибольшее распространение туберкулезные поражения мочевой системы отмечены у лиц от 20 до 40 лет, в то время как заболеваемость среди детей остается низкой.
Этиология и патогенез туберкулеза органов мочевой системы. Специфическими возбудителями туберкулезного процесса в органах мочевой системы преимущественно являются микобактерии туберкулеза человеческого типа (М. tuberculosis). Роль микобактерии бычьего типа (М. bovis) и атипичных возбудителей из рода Micobacterium крайне незначительна.
Подавляющее большинство случаев нефротуберкулеза являются вторичными по отношению к существующим в организме клинически проявившимся или латентным очагам туберкулезного процесса, обычно расположенным в легких. Отмечено, что почечные поражения возникают в среднем спустя 8 лет после первичного легочного туберкулеза. С током крови микобактерии попадают в клубочковый аппарат обеих почек, расположенный в их коре, где образуются мельчайшие туберкулезные очажки. Они могут самопроизвольно рассасываться при нормальном состоянии защитных механизмов организма. В случае расстройств гемо- и уродинамики почек, а также нарушений в иммунной системе туберкулезный процесс из коркового вещества распространяется на мозговое, где в итоге развивается воспалительный процесс в почечных сосочках (туберкулезный папиллит). В дальнейшем воспаление постепенно приобретает деструктивный характер и охватывает всю толщу пирамид почек с казеозным распадом последних и формированием каверн, которые могут быть как изолированными, так и сообщающимися с чашечно-лоханочной системой. Кроме того, при прогрессировании специфического процесса возможно образование в почечной паренхиме большого количества полостей, связанных друг с другом, или поликавернозной формы туберкулеза с последующим исходом в туберкулезный пионефроз. При заживлении каверн происходит обызвествление казеозных очагов, что, однако, не означает их санацию, так как в глубине петрификатов нередко сохраняются жизнеспособные микобактерии. Несмотря на двустороннее поражение почек туберкулезной инфекцией, клинико-рентгенологические проявления носят чаще всего односторонний характер.
Длительно протекающий нефротуберкулез обусловливает постепенное вовлечение в специфический процесс лоханки и мочеточника. Распространение инфекции осуществляется по лимфатическим сосудам, залегающим в подслизистом слое верхних мочевых путей. На слизистой оболочке указанных органов возникают множественные бугорки и язвы, при заживлении которых формируются деформации и сужения их просветов.
Туберкулез мочевого пузыря всегда является вторичным по отношению к поражению почки и мочеточника. Сравнительно позднее вовлечение мочевого пузыря связано с высокой резистентностью его слизистой оболочки к микобактериальной инфекции. Распространение на орган специфического инфекта происходит лимфогенным путем по подслизистым верхних мочевых путей. Туберкулезные очаги, образующиеся в мочевом пузыре, имеют вид бугорков, которые могут изъязвляться. Казеозный распад слизистой оболочки может прогрессировать как по площади, так и в глубину с вовлечением мышечного слоя.
Клиническая симптоматика туберкулеза органов мочевой системы. Туберкулезное поражение органов мочевой системы не имеет патогномоничных симптомов. На ранних стадиях заболевания возможно бессимптомное течение. Однако при развитии начальных деструктивных изменений нередко бывает безболевая тотальная макрогематурия вследствие эрозии сосуда при изъязвлении почечного сосочка. Образование каверн в почках обычно сопровождается болью в поясничной области и симптомами общей интоксикации организма (незначительными подъемами температуры тела, повышенной утомляемостью, слабостью и похуданием). Кроме того, при выраженном разрушении почечной паренхимы может возникать интенсивная тотальная макрогематурия.
Нарушение уродинамики на почве специфических стенозов верхних мочевых путей проявляется ощущением тяжести в пояснице, периодически повторяющейся почечной коликой с повышением температуры тела до фебрильных цифр. При двустороннем нарушении пассажа мочи на первый план нередко выступают симптомы хронической почечной недостаточности.
Туберкулезное поражение мочевого пузыря проявляется, в основном, дизурическими явлениями: императивными позывами к мочеиспусканию, поллакиурией и странгурией. Больные с туберкулезным-циститом жалуются на постоянную боль над лоном и периодическую терминальную макрогематурию.
Таким образом, симптоматология туберкулеза органов мочевой системы может протекать под различными клиническими «масками», в связи с чем наибольшее значение приобретают лабораторные и аппаратно-инструментальные методы исследования.
Диагностика туберкулеза органов мочевой системы. При опросе больного следует обратить внимание на наличие в анамнезе туберкулеза легких или других органов, а также указание на имевшие место длительные контакты с больными туберкулезной инфекцией.
Физикальные методы исследования не обладают высокой информативностью, в особенности на ранних стадиях заболевания. В то же время при пальпации органов мошонки и предстательной железы могут определяться признаки их специфического поражения, которое нередко сопутствует нефротуберкулезу.
Лабораторная диагностика играет важную роль в распознавании туберкулеза органов мочевой системы. Общий анализ мочи позволяет выявить пиурию, гематурию, протеинурию, а также ее кислую реакцию, что характерно для туберкулезного поражения почек и мочевых путей. Для более точной количественной оценки указанных изменений мочевого осадка предпочтительнее использовать исследование мочи по методу Нечипоренко.
Следует отметить, что протеинурия при туберкулезном процессе в мочевой системе является одним из наиболее частых признаков, однако она является ложной, так как связана с наличием большого количества форменных элементов в моче. Кроме того, для данного заболевания более характерна пиурия с неспецифической бактериурией, нежели асептическая пиурия, которая в прежние годы считалась патогномоничным симптомом нефротуберкулеза.
Самым достоверным и раним признаком туберкулезного поражения почек и мочевых путей является микобактериурия, которая подтверждается с помощью бактериоскопии, посева мочи на специальные среды (Левенштейна или Прейса-кольниковой), биологической пробы и все чаще при использовании метода ПЦР.
Интермиттирующий характер выделения возбудителей вынуждает прибегать к указанным исследованиям многократно (до 7 раз), при этом негативный результат поисков микобактерий туберкулеза в моче не может служить основанием для отрицания заболевания.
Увеличения информативности исследований мочи добиваются проведением провокационных туберкулиновых проб, при которых в организм пациента вводится туберкулезный антиген, вызывающий обострение специфического процесса, что приводит к пиурии, протеинурии и микобактериурии.
УЗИ позволяет судить о состоянии чашечно-лоханочной системы, выявлять очаги обызвествления и каверны в пораженной туберкулезным процессом почке. В то же время типичных эхографических признаков туберкулеза органов мочевой системы не обнаружено, что делает указанный метод лишь вспомогательным по отношению к рентгенологической диагностике заболевания.
Рентгенологическое исследование позволяет установить топографию и распространенность патологического процесса. На обзорном снимке органов мочевой системы можно обнаружить очаги обызвествления в проекции почек. В отличие от конкрементов тени петрификатов имеют неоднородную структуру, неправильную форму и расположены в проекции почечной паренхимы, а не чашечно-лоханочной системы.
При сохраненной функции почек можно применять экскреторную урографию, которая позволяет судить о состоянии паренхимы и чашечно-лоханочных систем почек, мочеточников и мочевого пузыря.
При значительной потере выделительной функции почек в целях визуализации верхних мочевых путей показана ретроградная уретеропиелография, а в случае рубцовой обструкции мочеточника необходимо выполнять пункционную антеградную пиелографию. Нисходящая цистография как завершающий этап экскреторной урографии редко позволяет визуализировать признаки специфического поражения мочевого пузыря, в то время как при помощи ретроградной цистографии можно выявить пузырно-мочеточниковый рефлюкс, возникший в результате длительного туберкулезного процесса, разрушившего замыкательный аппарат цистоуретерального соустья.
Почечную ангиографию выполняют для определения внутриорганной ангиоархитектоники перед планируемой резекцией почки.
Широкие диагностические возможности КТ и МРТ позволяют получить высокоточную дополнительную информацию в отношении степени сохранности паренхимы почек, что также определяет показания к органосохраняющим операциям при нефротуберкулезе.
Для получения сведений о функциональном состоянии пораженных туберкулезом почек используют радиоизотопные методы исследования.
При вовлечении в специфический процесс мочевого пузыря целесообразно выполнение цистоскопии, при которой могут выявляться туберкулезные бугорки, представленные в виде желто-серых образований, окаймленных красноватым ободком, участков очаговой гиперемии, изъязвления и рубцовые изменения слизистой оболочки. Эти явления бывают особенно выражены в области устья со стороны пораженной почки.
Лечение туберкулеза органов мочевой системы. Лечебная тактика при туберкулезном поражении почек и мочевых путей зависит от стадии процесса. На ранних этапах развития специфического заболевания (I-II стадия нефротуберкулеза) эффективной оказывается медикаментозная терапия. Общепринято одновременное назначение нескольких препаратов разных групп на длительный срок (минимум на 9-12мес). При лечении туберкулеза органов мочевыделительной системы наиболее часто применяют лекарственные средства нового поколения: изониазид, рифампицин, этамбутол, протионамид, пиразинамид и др. Для повышения эффективности нередко их сочетают с фторхинолонами (ципрофлоксацин, офлоксацин, ломефлоксацин и др.). В то же время не утратили свою актуальность и такие противотуберкулезные препараты, как стрептомицин и тубазид.
Следует учитывать, что консервативная терапия туберкулеза приводит к постепенному замещению инфекционных очагов рубцовой тканью. В связи с этим лечение туберкулезного поражения мочеточника в целях предотвращения его грубого рубцевания целесообразно проводить на фоне дренирования внутренним мочеточниковым катетером-стентом.
Хирургическому лечению подвергаются только больные в поздних стадиях нефротуберкулеза. При III стадии процесса предпочтение отдается таким органосохраняющим операциям, как резекция почки, кавернэктомия и кавернотомия. Тотальная деструкция органа является прямым показанием к нефрэктомии.
Сморщивание мочевого пузыря вследствие его тотального туберкулезного поражения значительно нарушает качество жизни пациентов. В связи с этим при микроцистис применяют кишечную пластику, обеспечивающую увеличение объема мочевого пузыря.
За 2-3 нед. до любой операции по поводу туберкулеза органов мочевой системы, а также на протяжении 3-5 лет после нее необходимо проведение противотуберкулезной химиотерапии.
Прогноз при туберкулезе органов мочевой системы. Главным прогностическим фактором при туберкулезе почек и мочевых путей является стадия заболевания. На ранних этапах развития нефротуберкулеза и при отсутствии грубых деструктивных изменений в мочеточнике и мочевом пузыре адекватная консервативная терапия может приводить к полному излечению.
Выраженное разрушение почечной паренхимы делают сомнительным сохранение пораженного органа. Прогностически крайне неблагоприятным для жизни больного является клинически двустороннее поражение органов мочевой системы, в особенности на поздних стадиях.
Мочекаменная болезнь: этиопатогенез. Камни почек, мочеточника, мочевого пузыря: клиника, диагностика, современные методы лечения.
Мочекаменная болезнь - это заболевание, проявляющееся образованием камней в почках и других органах мочевыделительной системы. Мочекаменная болезнь встречается у людей самых разных возрастов, от детей до пожилых людей.
Основной механизм заболевания врожденный — небольшое нарушение обмена веществ, что приводит к образованию нерастворимых солей, которые формируются в камни. По химическому строению различают разные камни — ураты, фосфаты, оксалаты и др.
Предрасполагающие факторы:
Климатический фактор: в жарком климате в организме повышается концентрация некоторых солей, и могут начать образовываться камни.
Географический фактор. Здесь играет роль состав воды (жесткая вода с большим содержанием кальциевых солей способствует появлению уролитиаза), пищи (острая и кислая пища повышает кислотность мочи, от чего камни образуются легче).
Постоянный недостаток витаминов в пище и ультрафиолетовых лучей может способствовать камнеобразованию.
Травмы и заболевания костей — остеомиелит, остеопороз.
Хронические заболевания желудка и кишечника, такие как хронический гастрит, колит, язвенная болезнь.
Сильное обезвоживание организма, что может быть при инфекционном заболевании или отравлении.
Различные заболевания почек и органов мочеполовой системы — пиелонефрит, гидронефроз, нефроптоз, цистит, аденома предстательной железы, простатит и другие.
Камни почек
Заболевание проявляется болями в пояснице, появлением крови в моче, возможно самостоятельное отхождение камней с мочой.
Боли носят тупой, ноющий характер, но могут быть острыми. Чаще боли бывают с одной стороны. Если камни есть в обеих почках, то боли будут возникать одновременно или поочередно с обеих сторон. Характерна связь болей с движением, изменением положения тела.
Кровь в моче появляется обычно после сильной боли или после физической нагрузки, ходьбы. После сильного приступа боли также могут отходить камни.
Камни мочеточника
Смещаясь из почки, камень попадает в мочеточник. Боль при этом переходит из поясницы в пах, низ живота, половые органы, бедро.
Если камень располагается в нижней части мочеточника, то больной испытывает частые беспричинные позывы на мочеиспускание.
Если камень полностью перекрыл просвет мочеточника, то в почке скапливается моча, что вызывает приступ почечной колики (см. вопрос по почечной колике выше). Он проявляется острыми схваткообразными болями в пояснице, которые быстро распространяются на соответствующую половину живота. Боль может продолжаться несколько часов и даже дней, периодически стихая и возобновляясь. Больной при этом ведет себя беспокойно, не может найти удобного положения. Приступ заканчивается, когда камень изменяет свое положение или выходит из мочеточника. Если после приступа колики камень не отошел, то приступ может повториться. Обычно по окончании приступа появляется кровь в моче.
Камни мочевого пузыря
Основное проявление — боль внизу живота, которая может отдавать в промежность, половые органы. Боль появляется при движении и при мочеиспускании.
Другое проявление камней мочевого пузыря — учащенное мочеиспускание. Резкие беспричинные позывы появляются при ходьбе, тряске, физической нагрузке. Во время мочеиспускания может отмечаться так называемый симптом "закладывания" — неожиданно струя мочи прерывается, хотя больной чувствует, что мочевой пузырь опорожнен не полностью, и мочеиспускание возобновляется только после перемены положения тела.
В тяжелых случаях при очень больших размерах камня больные могут мочиться только лежа.
Осложнения:
Камни почки и мочеточника со временем обязательно приведут к развититю острого или хронического пиелонефрита. При отсутствии лечения может произойти гнойное расплавление почки, и ее придется удалять.
Камни мочевого пузыря могут спровоцировать развитие острого цистита с тяжелыми проявлениями.
Диагностика:
Уролог проводит общий анализ мочи, УЗИ и рентген органов мочевыделительной системы. При подозрении на камень мочевого пузыря проводится цистоскопия.
Лечение мочекаменной болезни может быть консервативным, инструментальным и оперативным.
Консервативное лечение проводится при небольном размере камня и отсутствии осложнений заболевания. Оно включает в себя правильную диету и прием некоторых лекарственных препаратов.
Диета зависит от вида уролитиаза. При образовании камней уратов исключаются субпродукты — мозги, почки, печень и др. При фосфатных камнях показано мясо, сало, мучные блюда, растительные жиры, исключаются молоко и молочные продукты, ограничиваются овощи и фрукты. При оксалатных камнях исключаются из еды салат, шпинат, ограничиваются картофель, молоко.
Большие камни почек удаляются только на операции. Камни мочеточника обычно удается низвести в мочевой пузырь и удалить эндоскопически. При камне мочевого пузыря проводится камнедробление через цистоскоп. Если эта процедура оказывается неэффективной, то делают операцию со вскрытием мочевого пузыря.
Часто оказывается эффективным метод дистанционной литотрипсии — дробление камня электромагнитными волнами. Эта методика наиболее предпочтительна, так как легче всего переносится больными. К сожалению, раздробить камни таким образом удается не всегда.
Профилактика мочекаменной болезни
Не есть: бульоны, шоколад, кофе, какао, острую и жареную пищу.
Ограничить: общее количество пищи (не переедать), жирную пищу, поваренную соль.
Пить много воды, не менее 1,5 л в сутки. Летом пить столько, чтобы никогда не ощущать жажды.
Регулярно принимать мочегонные настои или отвары различных трав.
Сильно не переохлаждаться, всегда держать в тепле поясницу.
Недержание мочи при напряжении у женщин (стресс инконтиненция) клинические проявления. Принципы лечения.
СНМ чаще всего встречается в возрасте от 35 до 60 лет. Среди различных видов недержания мочи (НМ) у женщин СНМ составляет от 5% до 78% .
Около 25% женщин, обратившихся к урологу и до 31% к гинекологу, указывают на симптомы непроизвольного выделения мочи при физической нагрузке.
Но только около 4% страдающих СНМ женщин обычно обращаются к врачу. Зачастую это связано не только с интимностью данного вопроса и нежеланием обсуждать его в семье или кабинете врача, но и общеизвестным суждением о неэффективности большинства методов лечения данного заболевания.
Причины, вызывающие СНМ, весьма разнообразны. В большинстве случаев болеют рожавшие женщины. В настоящее время доказано, что в развитии заболевания основную роль играет не количество, а характер родов: чаще СИ страдают женщины, перенесшие патологические роды, сопровождающиеся разрывами мышц тазового дна, промежности и мочеполовой диафрагмы. Причинами СНМ являются также различные гинекологические вмешательства, тяжелая физическая нагрузка, эстрогенная недостаточность в климактерическом периоде.
Классификация стрессового недержания мочи у женщин.
Упрощенно выделяют два основных вида СНМ: заболевание, связанное с дислокацией и ослаблением связочного аппарата неизмененного мочеиспуcкательного канала, что относится к анатомическому недержанию мочи, и заболевание, связанное с изменениями в самой уретре и сфинктерной системе, приводящими к нарушению функции замыкательного аппарата (сфинктерное недержание мочи).
Классификация СНМ по E. McGuire (1982).
I тип – дислокация (опущение) неизмененной уретры и шейки мочевого пузыря;
II тип – дислокация неизмененной уретры и шейки мочевого пузыря в сочетании с цистоцеле и ректоцеле;
III тип – нарушение структуры уретры и шейки мочевого пузыря вследствие предшествующих операций (повреждение внутреннего сфинктера).
Некоторые авторы предлагают сочетание II/III типов.
Симптоматика и клиническое течение
Основной жалобой больных является недержание мочи при физической нагрузке и сохраненном физиологическом акте мочеиспускания. В зависимости от степени поражения замыкательного аппарата мочевого пузыря, степень недержания мочи может быть различной – от нескольких капель до тотального недержания при малейшем движении. Степень клинической тяжести определяется по величине усилия, провоцирующего эпизод непроизвольной потери мочи во время физического напряжения:
I –тяжелые физические усилия: натуживание, упорной сильной кашель, повторное чихание;
II - –средние физические усилия: длительная ходьба с нагрузкой, бег, подъем по лестнице, умеренный кашель, смех;
III – незначительные физические усилия: переход в положение стоя, любые изменения тела, лежа при небольших физических нагрузках.
Диагностика.
Методы исследования СИ отличаются большим разнообразием, что связано с необходимостью четкого определения типа недержания мочи и зависимости его от повреждения тех или иных анатомических структур.
Для диагностике СНМ у женщин используется комплексная методика обследования больных:
1.Клинический метод исследования (жалобы больных, анамнестические данные, дневник мочеиспусканий, объективное обследование - общесоматический и гинекологический осмотр).
2.Эндоскопические методы (уретроцистоскопия).
3.Ультрасонографические исследования.
4.Магнитно-резонансная томография (МРТ).
5. Комбинированное уродинамическое исследование (КУДИ)
Необходимо получить информацию о факторах риска, в том числе и наследственных, выяснить гинекологический и акушерский анамнез, предшествующие оперативные вмешательства на гениталиях и органах малого таза, гормональный и неврологический статус, применяемых в момент обращения медикаментах и предшествующее медикаментозное лечение СИ.
Уточняется характер профессиональной деятельности, степень физических нагрузок и факторов влияющих на повышение внутрибрюшного давления (подъем тяжестей, наличие хронических заболеваний кишечника и дыхательных путей).
Регистрация суточного ритма спонтанных мочеиспусканий с количеством выделяемой мочи и эпизодами недержания осуществлялась с использованием дневника мочеиспусканий, который заполнялся больными самостоятельно.
После общесоматического обследования выполняется влагалищный осмотр с оценкой состояния кожи промежности, слизистой влагалища, половой щели и наружного отверстия уретры. В покое и при натуживании определяют положение шейки матки и матки, подвижность уретровезикального (УВ) сегмента и проксимальной уретры, наличие и степень опущения стенок влагалища с уретроцеле, цистоцеле и ректоцеле, состояние мышц тазового дна (леваторный тест), наличие рубцовых деформаций промежности, влагалища, уретры.
При оценке слизистой оболочки вульвы и влагалища обращали внимание на наличие атрофических изменений, которые могут указывать на эстрогенную недостаточность, последняя в свою очередь приводит к снижению тонуса уретры и нарушению ее замыкающей функции.
Особое значение при физикальном обследовании придается индикации непроизвольной потери мочи, которая констатировалась с помощью различных функциональных проб: кашлевой с барьером и с натуживанием или пробой Вальсальвы.
Цистоскопия применяется при анамнестически выявленном хроническом рецидивирующем цистите с определяемой лейкоцитурией и интраоперационно - для исключения перфорации мочевого пузыря.
Ультрасонографическое исследование позволяет детально изучить топографоанатомические взаимоотношения мочевого пузыря, мочеиспускательного канала и парауретрального пространства.
Для изучения анатомии тазовых органов у больных с выраженными нарушениями топографии мочевого пузыря и уретры , а также для оценки послеоперационных результатов нами применялась МРТ с индукцией магнитного поля 1,5 Тл, с использованием последовательностей SE, FLASH, Turbo SE в 3-х ортогональных проекциях и CINE МРТ при расслаблении и напряжении диафрагмы таза (проба Вальсальва) в условиях тугого наполнения мочевого пузыря.
Комбинированное уродинамическое исследование (КУДИ) - одновременное проведение урофлоуметрии, цистометрии наполнения, статической и стресс-профилометрии (динамической) и определения порога абдоминального давления, при котором регистрируется потеря мочи (VLPP).
Лечение.
Для лечения СНМ используются консервативное и хирургическое лечение. Предпочтительность того или иного подхода определяется причиной заболевания, степенью выраженности НМ, анатомическими нарушениями, ассоциацией с выпадениями тазовых органов, влиянием на качество жизни.
При I типе СИ предпочтение отдается консервативному методу лечения, особенно у больных с повышенным риском оперативного лечения. Специальные комплексы упражнений по Д.Н. Атабекову, Кегелю или с вагинальными конусами, укрепляют сфинктеры мочевого пузыря и оказывают стимулирующее воздействие на мышцы промежности. Широкое применение находят специальные эндоуретральные обтураторы, создающие препятствие непроизвольному выделению мочи. СНМ, наступившее в период климакса, в ряде случаев успешно лечится заместительной гормональной терапией. Нормализуют функцию замыкательного аппарата мочевого пузыря различные методы физиотерапевтического воздействия: вибромассаж, диадинамические и гальванические токи, амплипульс, электрофорез. В консервативной терапии СНМ применяют также медикаментозные препараты, обладающие антихолинергической активностью (оксибутин, троспиум хлорид, толтеродин, флавоксат).
Для коррекции II и III типов СНМ ведущим считается хирургическое лечение, а в лечении тяжелых форм СИ является методом выбора. В международной и отечественной литературе освещено от 100 до 500 различных операций и способов оперативного лечения стресс-недержания мочи. Наиболее современным хирургическим методом считается слинговая операция TVT (Tension-free Vaginal Tape)-свободная синтетическая петля, предложенная профессором Ulf Ulmsten (Uppsala, Швеция) в 1995 году (11).
Сущность операции состоит в проведении петли из синтетической ткани под средней третью уретры. Операция TVT малоинвазивна, безопасна, технически проста, удобно сочетается с хирургической коррекцией пролапса гениталий.
Опухоли почки, мочевого пузыря: клиника, диагностика, принципы комбинированного и комплексного лечения.
ОПУХОЛЬ ПОЧКИ
Самым частым видом опухоли почки является рак почечной паренхимы. Эпителиальные опухоли почечной лоханки и мочеточника встречаются значительно реже, чем опухоли паренхимы, составляя 16% от всех опухолей почки и верхних мочевых путей. Опухоли почки у взрослых составляют 2–3% от числа всех новообразований. Мужчины болеют чаще (примерно в 2 раза) чем женщины. Преимущественный возраст больных от 40 до 60 лет. Среди опухолей почки доброкачественные обнаруживаются редко. Злокачественные опухоли у детей в 95% смешанные, их принято называть опухолями Вильмса.
Причинами опухолей почки могут служить гормональные, лучевые, химические факторы.
Метастазирование.Злокачественные опухоли почки метастазируют гематогенным (по кровеносным сосудам) и лимфогенным путем. Метастазы наблюдаются более чем у половины больных. На первом месте по частоте метастазирования рака почки стоят легкиезатем кости, печень, головной мозг. Эта закономерность обусловлена наличием тесной связи между венозной системой почки и магистральными сосудами грудной и брюшной полостей, а также венозной сетью скелета.
Нередко метастаз рака почки проявляется клинически раньше, чем первичный очаг заболевания. Особенностью рака почки является сравнительно частое появление метастазов через много лет (10–15 и даже 20) после удаления первичной опухоли. В тоже время другая особенность этого вида рака состоит в том, что его легочные метастазы в некоторых случаях склонны к регрессии после удаления первичного очага.
На втором месте по частоте среди отдаленных метастазов опухолей почки стоят костные метастазы, которые чаще всего локализуются в костях таза, позвоночнике, ребрах, костях плечевого пояса, бедренных костях, своде черепа. Метастазы в печень отмечаются в поздних стадиях заболевания.
Региональные метастазы рака почки поражают главным образом паракавальные и парааортальные лимфатические узлы.
Помимо отдаленных и региональных лимфатических метастазов, рак почки дает метастазы вне лимфатических узлов в околопочечную жировую клетчатку, мышцы брюшной стенки, подкожную жировую клетчатку, в послеоперационный рубец. При этом отмечается не прорастание опухоли, а наличие отдельных, четко отграниченных очагов метастазирования. Помимо метастазирования рака почки, нередко наблюдается распространение опухолевого тромба по почечной вене в нижнюю полую вену.
Течение заболевания. Среди общих симптомов опухоли почки важное значение имеет ухудшение общего состояния в результате интоксикации организма продуктами обмена в опухолевой ткани, при этом отмечается общая слабость, потеря аппетита, похудание. Больных с подобными жалобами длительно лечат по поводу самых различных предполагаемых заболеваний, прежде чем возникает мысль о необходимости урологического обследования.
Похудание как проявление опухолевого процесса является следствием токсического воздействия продуктов распада опухоли на организм. Интоксикация ведет к снижению аппетита, что в свою очередь обусловливает потерю массы тела. Похудание чаще всего является признаком далеко зашедшего бластоматозного процесса.
Важным симптомом опухоли почки общего характера является повышение температуры тела. Этот симптом наблюдается у 20–30% больных раком почки. Иногда повышение температуры тела оказывается единственным проявлением заболевания. Температура тела чаще бывает около 37 С, однако иногда достигает 38–39 С, сопровождается ознобом, имитируя острое инфекционное заболевание.
Токсическое воздействие опухоли почки на костный мозг приводит к угнетению его функциии возникновению анемии, что является свидетельством далеко зашедшего опухолевого процесса. Проялением опухоли почки может быть полецитемия или вторичный эритроцитоз. Этот процесс объясняют повышенной продукцией эритропоэтина тканью опухоли почки. Наиболее частым из общих признаков опухоли почки является повышение СОЭ, которое может быть первым и единственным проявлением заболевания. У 5–10% больных злокачественными новообразованиями почки заболевание проявляется артериальной гипертензией.
К местным симптомам опухоли почки относится гематурия (примесь крови в моче), которая наблюдается у более половины больных. В отличие от многих других почечных заболеваний гематурия прираке почки нбывает чаще всего «безболевой», не сопровождаясь болями, нарушением мочеиспускания и другими симтомами. Она возникает чаще всего внезапно, на фоне удовлетворительного общего состояния и быстро проходит. Гематурия при опухоли почки тотальная, в ряде случаев с червеобразными сгустками крови, являющимися слепками просвета мочеточника, либо бесформенными, если они образуются в мочевом пузыре. Сгустки могут отсутствовать. Характерным для опухоли признаком является возникновение острых болей в области почки вслед за гематурией. Иногда после начала кровотечения развивается типичный приступ почечной колики, который проходит после отхождения с мочой кровяных сгустков. Интенсивная гематурия может вызывать также тампонаду мочевого пузыря кровяными сгустками и острую задержку мочеиспускания.
Ввиду кратковременности гематурии при опухоли почки, повторения ее через неопределенный срок, иногда через несколько лет, важнейшее значение приобретает срочная цистоскопия в момент кровотечения для выявления его источника.
Вторым по частоте местным симптомом являются боли в области почки, которые бывают чаще тупыми, ноющими (иногда с иррадиацией в пах, бедро), реже по типу почечной колики.
Прощупываемая опухоль представляет собой наиболее характерный, однако наиболее редкий и самый поздний из симптомов, составляющих триаду местных признаков опухоли почки.
Важным местным признаком опухоли почки служит варикоцеле. Причинами его при злокачественнойопухоли почки могут быть: 1) сдавление левой почечной вены или ее прорастание опухолью; 2) перегиб левой почечной вены в результате смещения почки книзу; 3) сдавление нижней полой вены или непосредственно одной из из яичковых вен опухолью либо пакетами пораженных метастазами лимфоузлов; 4) тромбоз нижней полой вены.
Диагностика. При осмотре и пальпации обычно выявляют лишь далеко зашедшие опухоли почки. О большой опухоли почки может свидетельствовать деформация живота. При осмотре можно также обнаружить варикоцеле, а при обструкции нижней полой вены - расширение вен передней брюшной стенки, отечность нижних конечностей.
Пальпация почки с пораженной опухолью, должна быть максимально бережной во избежание травмирования опухоли. Степень подвижности опухоли или почки при пальпации в известной степени служит показателем операбельности.
К методам лабораторной диагностикиотносятся общие анализы крови и мочи, биохимические и иммунологические исследования. Общие анализы крови выявляют изменения, специфические не только для рака почки: повышение СОЭ, анемию. Анализы мочи обнаруживают эритроцитурию. Могут наблюдаться протеинурия и лейкоцитурия, особенно при сочетании опухоли почки с пиелонефритом.
Из биохимических методов исследования наиболее широко применяют исследование ферментов, белка и белковых фракций, определение содержания кальция в сыворотке, реакцию Данилина. Характерными неспецифическими для первичного рака почки признаками являются повышение активности щелочной фосфатазы и ряда других ферментов в сыворотке крови, повышение уровня а2-глобулина (синдром Штауффера).
В последнее время для диагностики рака почки применяют иммунологические методы. Используя классические методы иммунодиффузного анализа (реакция радиальной иммуно-диффузии, иммуноэлектрофорез, встречный иммунофорез, двойная иммунодиффузия по Оухтерлони и др.), можно выявить глубокие нарушения метаболизма сывороточных белков; ферритина, трасферрина, альбумина и др.
Установлено, что опухолевая ткань почки избирательно на капливает ферритин. Этот белок находится в опухолевой ткани в 10–220 раз более высокой концентрации, чем в нормальных почках и раковых опухолях других органов. Уровень другого железосодержащего белка - трансферрина- в опухолевой ткани почки повышен в 3 раза. Указанные характерные изменения происходят в белковом спектре крови у 80% больных. После нефрэктомии у больных отмечена тенденция к нормализации указанных показателей, что является доказательством патогномоничности описанных выше изменений сывороточных белков для рака почки.
В последние годы большое внимание уделяют радиоизотопной диагностике опухолей почки. С этой целью применяют статическую нефросцинтиграфию (или сканирование почек).
Широкое применение в онкоурологии находит ультразвуковое сканирование для диагностики опухолей и кист почки. Метод безвреден, безопасен, не требует предварительной подготовки больного и обладает высокой диагностической информативностью.
Несмотря на внедрение в клиническую практику указанных выше методов, заключительным этапом диагностики опухоли почки является рентгенологическое исследование.
Рентгенологическое обследование больного начинают с обзорной урографии, выявляющей изменения конфигурации почки- и ее положения, петрификаты в ткани опухоли. В ряде случаев, когда по обзорной рентгенограмме нельзя судить о контурах почки, прибегают к томографии или пневмо-ретроперитонеуму, с помощью которых получают более рельефное изображение тени почки.
Экскреторная урография позволяет уточнить как функциональные, так и морфологические особенности почки, пораженной опухолью, и, кроме того, выявить состояние противоположной почки.
Брюшная аортография должна быть первым этапом почечной ангиографии, на котором определяют тип васкуляризации пораженной почки (одиночная, удвоенная или добавочная артерия), распознают опухоль, характер ее роста (в глубь органа или кнаружи), ее взаимоотношения с окружающими органами, наличие метастазов в противоположной почке, печени.
Селективную почечную а р т е р и о г р а ф и ю следует выполнять при необходимости уточнения данных аортографии.
Дифференциальная диагностика. Наиболее часто приходится дифференцировать опухоль от солитарной кисты почки, что оба заболевания иногда сочетаются. При гидронефрозе прощупывают опухолевидное образование в подреберье, однако консистенция его тугоэластическая, поверхность гладкая, а гематурия отмечается редко. Поликистозпочек симулирует опухоль в случае его асимметрического развития, когда прощупывают только одну уве личенную плотную бугристую почку.
При карбункуле (реже абсцессе) почки подозрение на наличие опухоли обычно возникает в связи со сходной рентгенологической картиной (деформация, оттеснение чашечно-лоханочной системы, ампутация чашечек). Аналогичным образом проводят дифференциальную диагностику опухоли и туберкулеза почки.
Лечение. Единственным радикальным методом лечения злокачественных опухолей почки является операция. В последние годы показания к радикальному оперативному лечению опухолей почки значительно расширились, а противопоказания — сократились. Это связано со значительным совершенствованием хирургической техники, развитием современной анестезиологии и реаниматологии, появлением мощного арсенала антибактериальных препаратов, сердечно-сосудистых средств, применением лучевого лечения и противоопухолевой химиотерапии как до, так и после операции.
Даже при наличии метастазов удаление основного опухолевого очага может продлить жизнь больного. Одиночные метастазы в легкие, печень, кости конечностей в современных условиях уже не могут расцениваться как противопоказания к нефрэктомии, ибо по поводу таких метастазов с успехом может быть проведено радикальное оперативное лечение (лобэктомия или пульмонэкто-мия, резекция печени, ампутация или экзартикуляция конечности).
Выбор оперативного доступа к почке, пораженной опухолью, обусловлен в основном размерами и локализацией опухоли. Можно выделить три основных вида оперативного доступа при нефрэктомии по поводу опухоли: ретроперитонеальный, трансперитонеальный и торакоабдоминальный.
Лучевое лечение можно рекомендовать после нерадикально выполненного оперативного вмешательства (оставление инфильтрированной жировой капсулы почки, пораженных метастазами лимфатических узлов, опухолевого тромба в почечной или нижней полой вене), до операции при очень больших размерах и неподвижности опухоли, при ясно иноперабельной опухоли или ее метастазах (для снятия болей, уменьшения гематурии).
Лекарственное лечение включает проведение химиотерапии и гормонотерапии.
Применение противоопухолевых химиопрепаратов (химиотерапия) при раке малоэффективно в связи с нечувствительностью к ним как самой опухоли, так и ее метастазов.
В последние годы при опухолях почки получила распространение гормонотерапия- лечение гормонами, оно основано на том, что опухоли почки вызванные эстрогенами, поддаются тормозящему влиянию гормонов противоположного действия — тестостерона или прогестерона. При клиническом применении этих гормонов у больных с далеко зашедшим раковым процессом в почке, подтвержденным гистологически, и с множественными метастазами у половины пациентов достигается субъективное ухудшение, а в некоторых случаях и объективное (регрессия легочных или костных метастазов).
Прогноз. При опухоли почки прогноз зависит прежде всего от стадии процесса. Наихудшие отдаленные результаты лечения зарегистрированы у больных с прорастанием почечной вены и метастазами. Особенно неблагоприятный прогноз у неоперированных больных. По мере роста первичной опухоли или распространения метастазов состояние их неуклонно ухудшается: нарастает общая слабость, истощение, во многих случаях отмечаются лихорадка, гематурия, сильные боли. Больные погибают от тяжелой интоксикации, кахексии, анемии. Важным прогностическим фактором является возраст больных, среди больных моложе 40 лет отмечена меньшая выживаемость, чем среди более пожилых.
ОПУХОЛИ МОЧЕВОГО ПУЗЫРЯ
Опухоли мочевого пузыря составляют около 4% всех новообразований, уступая по частоте только опухолям желудка, пищевода, легких и гортани. Согласно мировой статистике, частота этого заболевания нарастает.
У мужчин опухоли мочевого пузыря отмечают значительно чаще, чем у женщин (4:1). Большую часть опухолей мочевого пузыря у мужчин объясняют более частым контактом с канцерогенными веществами и более длительной задержкой мочи в пузыре.
Новообразования мочевого пузыря встречаются в основном у лиц старше 50 лет. Опухоли мочевого пузыря у детей наблюдаются редко — в 60 раз реже, чем у взрослых, чаще у мальчиков. Опухоли могут располагаться во всех отделах мочевого пузыря, однако наиболее частая их локализация- мочепузырный треугольник и прилегающие к нему участки.
В настоящее время наибольшее распространение получила химическая теория происхождения опухолей мочевого пузыря. Во второй половине XIX в. было обращено внимание на частое возникновение новообразований мочевого пузыря у рабочих, занятых в производстве анилиновых красителей. В дальнейшем было установлено, что не сами канцерогенные ароматические амины ф-нафтиламин, бензидин), а их конечные метаболиты (вещества типа ортоаминофенолов) вызывают образование опухолей мочевого пузыря. Затем выяснилось, что большим сходством с дериватами ароматических аминов обладают некоторые вещества, являющиеся продуктами обмена вещества в человеческом организме, главным образом метаболиты типа ортоаминофенолов (скатол, индол и т.п.), обладающие канцерогенными свойствами. Указанные эндогенные канцерогенные ортоаминофенолы постоянно находятся в моче здоровых людей. В связи с этим важное патогенетическое значение приобретает застой мочи в пузыре. Опухоли мочевого пузыря у детей носят мезенхимальный характер. При морфологическом исследовании их обнаруживается рабдомиосаркома, леймиосаркома, миксосаркома. Крайне редко выявляются миомы, дермоиды, ангиомы, фиброэпителиомы. Саркомы отличаются выраженной злокачественностью.
Симптомы и клиническое течение. Симптоматика опухолей мочевого пузыря складывается в основном из гематурии и дизурии. Гематурия — более ранний признак, чем дизурия, так как кровотечение может возникнуть вследствие травматизации ворсин неинфильтрирующей опухоли (папилломы) при сокращении мочевого пузыря. При опухолях мочевого пузыря гематурия бывает тотальной, если опухоль кровоточит постоянно, или терминальной, если кровотечение возникает только при сокращении мочевого пузыря. Реже наблюдается микроскопическая гематурия (эритроцитурия). Длительность и частота кровотечения при опухолях мочевого пузыря колеблются в широких пределах. Иногда гематурия бывает кратковременной, повторяется с многомесячными и даже многолетними интервалами. В ряде случаев она длится несколько дней и даже несколько недель подряд и повторяется часто. При запущенных распадающихся опухолях мочевого пузыря гематурия обычно имеет постоянный характер.
Затрудненный отток мочи из мочевого пузыря и верхних мочевых путей, распад опухоли и изъязвление пузырной стенки способствуют присоединению инфекции и возникновению цистита и пиелонефрита. При этом моча становится гнойной. При распадающихся опухолях пузыря гнойная моча приобретает щелочную реакцию, зловонный аммиачный запах, в осадке появляются соли — фосфаты. Мочеиспускание при инфильтрирующем росте опухоли болезненное, особенно к концу акта, учащенное, с императивными позывами. Иногда инфильтрирующие опухоли мочевого пузыря сопровождаются болями постоянного характера, не связанными с мочеиспусканием или усиливающимися при нем. Иррадиация болей в промежность, половые органы, крестец, ягодичную область, бедро свидетельствует о прорастании нервных узлов или ветвей.
Инвазия опухоли мочевого пузыря в близлежащие ткани и их последующий некроз могут привести к образованию пузырно-влагалищных или пузырно-прямокишечных свищей с соответствующей клинической симптоматикой.
Инфильтрующий рост опухоли может вызвать сдавление устья мочеточника, сопровождающееся болями в области почки, развитием гидроуретеронефроза и пиелонефрита. При сдавлении устьев обоих мочеточников к этим явлениям присоединяются признаки почечной недостаточности вплоть до развития уремии.
Диагноз. В задачи диагностики новообразования мочевого пузыря входит не только распознавание наличия опухоли, но и определение ее стадии, состояния слизистой оболочки пузыря вокруг опухоли и верхних мочевых путей, наличия или отсутствия метастазов. Все это требует детального исследования не только мочевых органов, но и других органов и систем.
В определении величины опухоли и ее взаимоотношения с окружающими тканями важное значение имеет бимануальная пальпация области мочевого пузыря. Ее производят одной рукой через переднюю стенку живота над лобком, а другой через прямую кишку у мужчин или влагалище у женщин, в горизонтальном положении больного при опорожненном мочевом пузыре и полном расслаблении мышц, которого достигают с помощью наркоза. При такой пальпации можно определить плотный инфильтрат в области мочевого пузыря, распространение его в ткани малого таза, прямую кишку, предстательную железу, влагалище, матку, кости таза.
Цитологическое исследование осадка мочи играет существенную роль в диагностике опухолей мочевого пузыря. Патогномоничным признаком опухоли мочевого пузыря является присутствие в осадке ее одиночных опухолевых клеток или их комплексов. Признаками рака являются: 1) наличие крупных клеток; 2) полиморфизм клеток; 3) различные размеры клеток; 4) изменения ядра. Большое значение для диагностики имеет обнаружение компактных групп злокачественных клеток или мелких фрагментов раковой ткани, нежели отдельных клеток.
Отрицательные результаты исследования не означают отсутствия опухоли.
Ведущим методом исследования при подозрении на опухоль мочевого пузыря является цистоскопия. Она позволяет обнаружить опухоль, получить представление о локализации, размерах, количестве и внешнем виде опухолей, состоянии слизистой оболочки вокруг опухоли и устьев мочеточников.
Эндовезикальная биопсия необходима при определении вида патологического процесса в мочевом пузыре. Однако для установления доброкачественности или злокачественности опухоли этот метод недостаточно точен, так как позволяет получить для исследования лишь поверхностные участки опухоли, ее ворсины, а малигнизация всегда начинается в глубине опухоли, в ее основании и подлежащей ткани.
Рентгенологическое исследование позволяет получить ценные сведения для распознавания опухоли мочевого пузыря, определения ее стадии и оценки состояния верхних путей. При цистографии неинфильтрирующая опухоль мочевого пузыря дает дефект наполнения, но контуры пузыря при этом остаются неизменными и симметричными. Деформация контуров мочевого пузыря (скошенность стенки, изъеденность контуров, приподнятость шейки мочевого пузыря над лобковым симфизом) свидетельствует об инфильтрирующем росте опухоли. При прорастании опухолью паравезикальной клетчатки мочевой пузырь может быть расположен асимметрично по отношению к костям таза, будучи оттеснен опухолевым инфильтратом в ту или другую сторону.
Экскреторная урография дает представление о наличии или отсутствии папиллярной опухоли лоханки и мочеточника, функциональной способности почек, динамике опорожнения и анатомических изменениях почечных лоханок, мочеточников и мочевого пузыря. На поздней нисходящей цистограмме может быть виден дефект наполнения, обусловленный опухолью мочевого пузыря.
Тазовая венография выявляет признаки инвазии опухоли мочевого пузыря в околопузырную клетчатку: одностороннее заполнение тазовых вен, избыточное развитие мелкой венозной сети, смещение сосудистых коллекторов в латеральную сторону, деформацию париетальных вен таза, полулунные дефекты наполнения в них.
Лимфангиоаденографияпозволяет обнаружить метастазы в паховых, подвздошных, парааортальных и паракавальных лимфатических узлах в виде увеличения размеров узлов, дефектов наполнения или неравномерного скопления в них рентгеноконтрастного вещества. При полном нарушении проходимости лимфатических путей и узлов на том или ином уровне они совершенно не заполняются. Подобная блокада лимфотока может быть выявлена с помощью радиоизотопного лимфосканирования или лимфосцинтиграфии.
В настоящее время стали шире применять трансабдоминальную и эндовезикальную эхографию (ультразвуковое сканирование) мочевого пузыря для определения степени инфильтрации опухолью его стенки. Ультразвуковое сканирование мочевого пузыря можно проводить только при наполненном мочевом пузыре. На двухмерных эхограммах получают сагиттальный и горизонтальный срезы мочевого пузыря. По ультразвуковым картинам можно различать три варианта опухолей мочевого пузыря: 1) опухоль, занимающая слизистый и подслизистый слой; ультразвуковая картина стенки пузыря ровная, без утолщений; 2) опухоль, инфильтрирующая мышечный слой пузырной стенки; 3) опухоль, распространяющаяся за пределы пузырной стенки.
Дифференциальная диагностика. В ряде случаев необходима дифференциальная диагностика опухолей мочевого пузыря с патологическими процессами, которые при цистоскопии имеют большое сходство с опухолью, а порой и вовсе не отличимы от нее. К таким процессам относят туберкулезные или сифилитические опухолеподобные грануляции в мочевом пузыре, туберкулезные и простые язвы мочевого пузыря, эндометриоз мочевого пузыря, хронический геморрагический цистит, гранулематозный цистит, узелковый периартериит мочевого пузыря.
Лечение. Методы лечения опухолей мочевого пузыря делят на оперативные и консервативные. К оперативным относят эндовезикальные инструментальные и трансвезикальные хирургические вмешательства. Консервативное лечение состоит в лучевой и медикаментозной терапии. Оперативное лечение имеет несколько вариантов. Эндовезикальная электрокоагуляция является методом лечения неинфильтрирующих опухолей (типичные папилломы) мочевого пузыря. Она не требует вскрытия пузыря, хорошо переносится больными, легко и быстро разрушает небольшие папилломы. Однако после электрокоагуляции нередко наблюдаются рецидивы опухоли и обсеменение слизистой оболочки мочевого пузыря, поэтому данный метод лечения рекомендуется применять только у пожилых или ослабленных больных. Эндовезикальная лазерная коагуляция мочевого пузыря дает лучшие результаты. В остальных случаях даже при типичных папилломах вместо электрокоагуляции в настоящее время используют трансуретральную электрорезекцию мочевого пузыря.
Трансуретральную электрорезекцию производят с помощью специального эндоскопического инструмента — резектоскопа — при помощи подвижного петлевидного электрода, на который подается переменный ток высокой частоты. Движениями петли срезают основание опухоли мочевого пузыря вместе с подлежащими слоями его стенки в пределах здоровых тканей, коагулируют кровоточащие сосуды.
Трансвезикальная электрорезекция заключается в высоком сечении мочевого пузыря и электрорезекции опухоли током высокой частоты. Данный метод применяют по тем же показаниям, что и трансуретральную электрорезекцию, но в тех случаях, когда цистоскопия невыполнима (стриктура мочеиспускательного канала, уменьшение вместимости мочевого пузыря, гематурия и т.п.).
Резекция мочевого пузыря (иссечение части органа) нашла широкое распространение в урологической практике. При всем многообразии способов борьбы с опухолями мочевого пузыря существует один основной принцип. Он может быть сформулирован следующим образом: необходимо стремиться к полному удалению или разрушению опухоли, сохранив при этом нормальную структуру и функцию мочевого пузыря. Достоинство метода — сохранение органа и нормального мочеиспускания.
В ряде случаев проводят паллиативные операции. При полной задержке мочеиспускания на почве раковой инфильтрации шейки мочевого пузыря или вследствие тампонады пузыря сгустками крови бывает необходима экстренная эпицистостомия. При стойком нарушении оттока мочи из верхних мочевых путей вследствие сдавления опухолью мочеточников и присоединения гнойного пиелонефрита, уросепсиса, высокой азототемии показана пиело- или нефростомия либо уретерокутанеостомия.
Консервативное лечение состоит из лучевой и лекарственной терапии.
Лучевую терапию как самостоятельный метод лечения при опухолях мочевого пузыря применяют редко, главным образом при иноперабельных опухолях с паллиативной целью. Чаще ее проводят в комбинации с оперативным лечением. Предоперационное облучение способствует уменьшению перифокальных воспалительных изменений и самой опухоли и тем самым облегчает оперативное вмешательство, а в ряде случаев делает иноперабельную опухоль операбельной. Послеоперационная лучевая терапия показана при недостаточно радикально выполненном вмешательстве и для профилактики рецидивов опухоли. Из способов облучения наиболее эффективна при опухолях мочевого пузыря телегаммате-рапия. В последние годы использование в клинической практике источников высоких энергий (бетатроны, линейные ускорители) открывает новые возможности в лучевом лечении больных раком мочевого пузыря.
Лекарственное лечение (химиотерапия) как самостоятельный лечебный метод малоэффективно при опухолях мочевого пузыря, однако в комплексе с оперативным и лучевым лечением может улучшить исход заболевания. Наиболее благоприятные результаты получены при лечении комбинацией противоопухолевых химиопрепаратов (метотрексат, винбластин, адриабластин, цисплатина), а также внутрипузырными инсталляциями.
Прогноз. После своевременно предпринятого комплексного лечения прогноз наиболее благоприятен. Важным условием благоприятного исхода после органосохраняющих операций является систематическое диспансерное наблюдение за больными, лечившимися по поводу опухолей мочевого пузыря. Поскольку эти опухоли весьма склонны к рецидивам, больным в течение всей жизни необходим регулярный цистоскопический контроль для выявления рецидивной опухоли мочевого пузыря и своевременной ее ликвидации. В течение 1-го года после операции контрольную цистоскопию проводят каждые 3 мес, в течение следующих 3 лет — 2 раза в год, а затем ежегодно.
Новообразования яичка. Клиника. Диагностика.
Распространенность опухолей яичка относительно мала. Однако их эпидемиологическая значимость повышается из-за того, что болеют, главным образом, молодые мужчины, и заболеваемость неуклонно возрастает. Ежегодный относительный рост заболеваемости раком яичка составляет 2%, в основном за счет повышения частоты развития опухоли у мужчин 15-29 лет.
Эпидемиология
Опухоли яичка составляют около 1% всех новообразований у мужчин и в 0,5-0,65% случаев является причиной смерти. Диагностируется главным образом в возрасте 20-35 лет, причем у мужчин этой возрастной группы они являются наиболее частыми злокачественными новообразованиями. Очень редко, только в 1-2% случаев, развиваются двусторонние опухоли яичка. Для больных с раком яичка риск возникновения опухоли в противоположном яичке возрастает в 2-3 раза.
Этиология и патогенез
Одним из важнейших этиологических факторов развития опухоли является крипторхизм. При этой аномалии риск возникновения практически всех гистологических типов рака повышается в 11-14 раз.
По данным некоторых авторов, при крипторхизме риск развития семиномы почти в 2 раза выше, чем для других типов опухолей яичка. В то же время, согласно другим сообщениям, крипторхизм чаще является причиной возникновения несеминомных опухолей яичка.
В настоящее время основную роль в развитии рака яичка отводят влиянию эстрогенов на внутриутробное развитие ткани яичка. Установлено, что если во время беременности, особенно в первые два месяца, женщина принимала эстрогены, то риск развития рака яичка у сына повышается в 2-5 раз. Учитывая, процесс опущения яичка также находится под гормональным контролем и избыток эстрогенов может его нарушить, можно предположить, что учащение частоты возникновения рака яичка при крипторхизме также связано с эстрогенами. Это косвенно подтверждается тем, что при крипторхизме в контралатеральном опустившемся яичке риск развития опухоли в 2 раза выше, чем в обычно.
Среди других факторов, связанных с повышением риска развития рака яичка, отмечают чрезмерное потребление жирной пищи, травмы яичка, вирусные поражения, в том числе ВИЧ.
Классификация
В зависимости от локализации первичного очага различают гонадные и экстрагонадные опухоли яичка. Частота последних низка. Основными экстрагонадными локализациями рака являются средостение и забрюшинное пространство. Развитие экстрагонадных опухолей связывают с распространением гонадных клеток-предшественников в эмбриональном периоде.
Согласно гистологической классификации опухоли яичка разделяют на герминативные (герминогенные) и негерминативные (негерминогенные).
Герминативные опухоли в свою очередь подразделяют на опухоли одного гистологического типа и опухоли более чем одного гистологического типа.
Гистологическая классификация герминативных опухолей яичка
Опухоли одного гистологического типа |
Опухоли более чем одного гистологического типа |
Семинома. Эмбриональная карцинома. Тератома. Хориокарцинома. Опухоль желточного мешка. |
Эмбриональная карцинома и тератома (с или без семиномы). Эмбриональная карцинома и опухоль желточного мешка (с или без семиномы). Эмбриональная карцинома и семинома. Опухоль желточного мешка и тератома (с семиномой или без нее). Хориокарцинома и любые другие элементы. |
Наиболее частым гистологическим типом опухолей яичка является семинома, она составляет 25-60% всех новообразований яичка. Ко времени диагностики около 10% больных с семиномой уже имеют метастазы.
Несеминомные опухоли яичка часто входят в состав смешанных опухолей. Эмбриональная карцинома – наиболее частая несеминомная опухоль. Она развивается у более молодых мужчин, чем семинома. К моменту диагностики у 1/3 больных есть метастазы. Реже встречаются опухоли желточного мешка, главным образом, у мальчиков двух лет. Она является частой опухолью яичка в раннем детском возрасте. Хориокарцинома в чистом виде крайне редка и обнаруживается в возрасте 18-35 лет. Тератома образуется чаще в возрасте до 30 лет. У детей и юношей тератомы обычно имеют более доброкачественное течение.
Герминативные опухоли яичек склонны к метастазированию. Риск раннего метастазирования наименьший при тератоме и наивысший при хориокарциноме.
К негерминативным опухолям яичка относятся главным образом новообразования, развивающиеся из стромы полового тяжа. Среди них выделяют хорошо дифференцируемые, смешанные и недифференцируемые опухоли. К первым относят опухоли из клеток Лейдига, опухоли из клеток Сертоли и гранулезоклеточные опухоли.
Основной классификацией является система TNM. Критерий S характеризует уровень сывороточных маркеров опухоли яичка.
Первичная опухоль (Т). Распространение первичной опухоли устанавливается после радикальной орхиэктомии: рТх – первичная опухоль не оценивалась (если радикальная орхиэктомия не выполнялась, используется обозначение Тх); рТ0 – нет доказательств наличия первичной опухоли;
pTis – carcinoma in situ;
рТ1 – опухоль ограничена яичком и придатком яичка без признаков лимфатической / васкулярной инвазии; рТ2 – опухоль ограничена яичком и придатком яичка с признаками лимфатической – васкулярной инвазии, или опухоль прорастает белочную оболочку с вовлечением влагалищной оболочки яичка;
рТ3 – опухоль прорастает в семенной канатик с или без признаков лимфатической / васкулярной инвазии;
рТ4 – опухоль распространяется на мошонку с или без признаков лимфатической / васкулярной инвазии;
Метастазы в региональные лимфатические узлы (N):
Nx – региональные лимфатические узлы не оценивались;
No – нет метастазов в региональных лимфатических узлах;
N1 – метастазы в единичных лимфоузлах, 2 см и менее в наибольшем размере;
N2 - – метастазы в единичных лимфоузлах, более2 см, но менее 5 см в наибольшем размере; или во множестве лимфоузлов, но не более 5 см в наибольшем размере;
N3 – метастазы в лимфоузлах более 5 см в наибольшем размере.
Отдаленные метастазы (М):
Мх – наличие отдаленных метастазов не оценивалась;
М0 – нет отдаленных метастазов;
М1 – наличие отдаленных метастазов;
М1а – метастазы в легких или в отдаленных лимфоузлах;
М1b – другие (кроме легких и лимфатических узлах) отдаленные метастазы.
Сывороточные маркеры опухоли яичка (S):
Sx – исследование сывороточных маркеров не проводилось;
S0 – уровень сывороточных маркеров в норме;
S1 – лактатдегидрогеназа (ЛДГ)<1,5хN* и человеческий хорионический гонадотропин (ЧХГ)<1000 нг/мл и альфа-фетопротеин (АФП)<1000г/мл;
S2 – ЛДГ 1,5 – 10хN*, или ЧХГ 1000 – 10000 нг/мл, или АФП 1000 – 10000 нг/мл;
S3 – ЛДГ > 10хN*, или ЧХГ > 10000 нг/мл, или АПФ > 10000 нг/мл; N* - значение верхней границы нормы для ЛДГ.
Хирургические стадии, определяемые во время операции и по результатам гистологического исследования удаленных тканей.
Стадия I Опухоль ограничена яичком. Возможно наличие метастазов опухоли в паховых лимфатических узлах. Прорастание опухоли белочной оболочки яичка и/или семенного канатика, что повышает риск метастазирования в забрюшинные лимфоузлы и рецидива. Эта стадия соответствует клиническим стадиям I и II.
Стадия II Метастазы в за брюшинные и пара аортальные лимфоузлы. Установлено, что риск рецидивирования повышается, если вовлечено более 5 лимфоузлов, если величина одного или более вовлеченных лимфоузлов более 2 см, или если опухоль прорастает в клетчатку вокруг лимфоузлов. Эту стадию подразделяют на подгруппу с минимальными поражениями забрюшинных лимфатических узлов (МП) и с объемными поражениями забрюшинных лимфатических узлов (ОП). У больных, относящихся к подгруппе ОП, один или несколько забрюшинных лимфатических узлов более 5 см. У таких пациентов прогноз хуже. Хирургическая стадия II соответствует клинической стадии III без отдаленных метастазов.
Стадия III Характеризуется наличием отдаленных метастазов. Также подразделяется в зависимости от величины метастазов на стадии с минимальными и объемными поражениями (соответственно МП и ОП). При МП метастазы локализованы в лимфатических узлах и легких и не превышают 2 см в диаметре. ОП проявляется наличием метастазов более 2 см в диаметре, а также распространением опухоли на другие органы и ткани (печень, мозг и другие). Хирургическая стадия III соответствует клинической стадии III с отдаленными метастазами.
Симптоматика
Основными симптомами опухоли яичка являются увеличение и уплотнение яичка при пальпации и чувство тяжести в мошонке. У 70-90% больных именно эти симптомы являются первыми.
Боль не является характерным клиническим проявлением рака яичка, однако может быть приблизительно в 1/3 случаев.
Одним из ранних симптомов опухоли яичек может быть гинекомастия. Ее появление объясняется тем, что повышение уровня ЧТХ при некоторых герминативных формах рака может стимулировать выработку эстрадиола клетками Лейдига.
У 15% больных первичная опухоль яичка протекает бессимптомно, и первые проявления заболевания у них связаны с метастатическим поражением. Увеличение забрюшинных лимфатических узлов чаще всего проявляется болями в животе, спине, нарушением венозного оттока из нижних конечностей вследствие сдавления нижней полой вены. При метастазах в легких клиническая картина сходна с таковой при хроническом бронхите. Типичным симптомом является кашель.
Атипичные симптомы опухоли яичка могут наблюдаться при эктопии и крипторхизме. При этом клиническая картина может быть сходна с острой кишечной непроходимостью, острым аппендицитом или новообразованиями органов брюшной полости.
При первичной экстрагонадной локализации тестикулярной опухоли будут своеобразные клинические проявления.
При забрюшинной опухоли могут быть боли в животе и спине, нарушение венозного оттока из нижней половины тела.
Диагностика
При пальпации яичка и выявлении его уплотнения или увеоичения можно заподозрить наличие новообразования. Пальпаторное исследование является начальным этапом диагностики рака яичка.
Важное значение придается выявлению сывороточных опухолевых маркеров – человеческого хорионического гонадотропина (ЧХГ), альфа-фетопротеина (АПФ) и лактатдегидрогеназы (ЛДГ). При определении ЧХГ могут быть ложноположительные результаты, поскольку имеется перекрестная реакция между ЧХГ и лютеинизирующим гормоном. В этой связи рекомендуют измерять бета-субъеденицу ЧХГ, для которой эта перекрестная реакция незначительна. Повышение уровня ЧХГ выявляется у 100% больных хориокарциномой, 60% - эмбриональной карциномой, 25% - опухолями желточного мешка и только у 10% - с семиномой. Повышение уровня АПФ отмечается у 70% больных с эмбриональной карциномой и у 75% больных с опухолями желточного мешка, но отсутствует при хориокарциноме и семиноме.
УЗИ яичка используется для дифференциальной диагностики опухолей яичка и других заболеваний, например, эпидидимита. Точность УЗИ при опухолях яичка весьма высока и достигает 90%.
Важная диагностическая роль отводится непосредственно оперативному вмешательству – радикальной паховой орхэктомии. Обычная трансскротальная биопсия яичка не рекомендуется, поскольку повышается риск локальной диссеминации опухолевых клеток в мошонке и их распространения в паховые лимфатические узлы.
Регионарными лимфоузлами для яичка являются параортальные и паракавальные, а если в анамнезе были какие-либо вмешательства в пахово-мошоночной области – то и паховые.
Иногда удается пропальпировать увеличенные пораженные надключичные и шейные лимфатические узлы.
Наиболее точным методом определения лимфатических узлов, главным образом забрюшинных, является компьютерная томография. Эта информация необходима для выбора правильной тактики лечения больных с раком яичка. Однако необходимо учитывать, что у 25-30% больных с опухолью яичка и отсутствием данных КТ за поражение лимфатических узлов, при морфологическом исследовании последних обнаруживаются микроскопические метастазы.
Другими часто используемыми методами диагностики метастазов в забрюшинных лимфатических узлах являются каваграфия и лимфангиография. При значительном увеличении забрюшинных лимфатических узлов на экскреторных урограммах возможно обнаружить смещение или сдавление мочеточника.
Легкие являются самой частой локализацией отдаленных метастазов. Для их выявления необходимо выполнить рентгенографию легких в двух проекциях. Однако в случаях небольших размеров метастазов могут быть ложноотрицательные результаты. В этих случаях показано выполнение КТ легких, позволяющей обнаружить метастазы до 3 мм в диаметре.
Метастатическое поражение печени можно выявить при УЗИ и сцинтиграфии печени, при подозрении на наличие метастазов в мозге – ЯМР.
Лечение
Тактика лечения герминативных опухолей яичка зависит от гистологического строения опухоли, стадии заболевания, наличия и поражения контрлатерального яичка.
Подходы к лечению семиномных и несеминомных опухолей различны. Смешанные опухоли, содержащие семиномные и несеминомные компоненты, должны рассматриваться при планировании лечения как несеминомы. Если при семиноме обнаруживается повышение уровня сывороточного АПФ, то стратегия лечения аналогична таковой при несеминоме.
В связи с использованием прогностической классификации тактика лечения опухолей яичка в последние годы претерпела некоторые изменения. У больных с хорошим прогнозом возможно снижение доз химиопрепаратов с целью уменьшения токсичности, а у больных с плохим диагнозом, наоборот, необходимо увеличивать интенсивность химиотерапии для повышения эффективности лечения.
Тактика лечения герминативных опухолей яичка
Клиническая стадия |
Семинома |
Несеминома |
Carcinoma in situ |
Локальная радиотерапия яичка (20 Гр) |
|
I стадия |
1. Радикальная орхиэктомия, затем адъювантная радиотерапия забрюшинных лимфоузлов. 2. Радикальная орхиэктомия, затем наблюдение с химио- или радиотерапией при выявлении рецидивов. 3. Радикальная орхиэктомия, затем адъювантная химиотерапия карбоплатином. |
1. Радикальная орхиэктомия с забрюшинной лимфаденэктомией. 2. Радикальная орхиэктомия, затем наблюдение с химио- или радиотерапией при выявлении рецидивов. 3. Радикальная орхиэктомия, затем адъювантная химиотерапия |
II стадия |
Семиномы с МП. Радикальная орхиэктомия, затем радиотерапия. Семиномы с ОП. 1. Радикальная орхиэктомия, затем радиотерапия. 2. . Радикальная орхиэктомия, затем комбинированная химиотерапия |
1. Радикальная орхиэктомия с забрюшинной лимфаденэктомией с последующим контролем. 2. Радикальная орхиэктомия с забрюшинной лимфаденэктомией, затем адъювантная комбинированная химиотерапия. 3. Радикальная орхиэктомия, затем химиотерапия с последующей резекцией остаточных образований (если имеются). |
III стадия |
Радикальная паховая орхиэктомия, затем комбинированная химиотерапия |
1. Комбинированная химиотерапия, при необходимости резекция остаточных опухолевых образований. 2. Интенсивные режимы химиотерапии аутотрансплантацией костного мозга. |
Рецидивный рак яичка
Тактика лечения рецидивов и прогноз зависят от многих факторов, главными из которых являются гистологический тип опухоли, характер предыдущего лечения и локализация рецидива.
Комбинированная терапия. Эффективность дополнительных курсов химиотерапии по поводу рецидивов опухоли яичка не превышает 25% у больных, лечившихся ранее комбинациями препаратов, включавшими цисплатин. Более благоприятны исходы лечения больных с одиночными рецидивами. Чаще всего дечение больных с рецидивами начинают режимом VIP. Возможно применение новых комбинаций препаратов, например: цисплатин, ифосфамид, паклитаксел (таксол).
Интенсивные режимы химиотерапии с аутотрансплантацией костного мозга. Применяют при недостаточной эффективности стандартных доз химиопрепаратов.
Хирургическая резекция одиночных метастазов при химиорефрактерных опухолях. Выбор этого метода лечения определяется резецируемостью опухоли, количеством и степенью резистентности к химиотерапии, а также гистологическим типом опухоли.
Доброкачественная гиперплазия предстательной железы. Этиология, клиника, диагностика. Современные методы медикаментозного и хирургического лечения.
Доброкачественная гиперплазия простаты - доброкачественная опухоль, увеличение в количестве клеток периуретральных желез простаты.
Самое частое заболевание у мужчин старшего возраста.
Возникает в возрасте 40-50 лет. В возрасте 50 лет около 25% мужчин имеют симптомы ДГПЖ, а в возрасте 65 лет - уже 50%, со временем заболевание развивается у 85% мужчин.
Гистологические (микроскопические) признаки ДГПЖ встречаются, уже начиная с 30-40-летнего возраста.
Причины
Причины ДГПЖ точно не известны, предполагается, что это полиэтиологическое, зависящее от многих причин, заболевание. Достоверно известно, что ДГПЖ зависит от наличия мужских половых гормонов - андрогенов.
При наступлении атрофических процессов в предстательной железы ко времени угасания половой активности неуправляемо разрастаются парауретральные железки в центре предстательной железы , функция которых до сих пор полностью не ясна. Предполагается, что они являются железами внутренней секреции, антагоническими по отношению к мужским половым железам. В образование ДГПЖ вовлекается не только железистая, но и мышечная и соединительная ткани, в результате чего она может иметь не только аденоматозный (железистый), но и фиброзный (рубцовый) или миоматозный (мышечный) характер. В узелках соединительной ткани бывает обычно больше, чем железистой, иногда в соотношении 4:1 и даже 5:1. Чем больше узлы и размер простаты, тем большую часть занимает железистый компонент. Узлы ДГПЖ по мере роста вытесняют и замещают ткань железы.
В зависимости от развития узлов в пределах той или иной зоны простаты формируются боковые доли или средняя доля.
Нарушения мочеиспускания при ДГПЖ обусловлены как механическим сдавлением уретры (мочеиспускательного канала) узлами ДГПЖ, так и сокращением мышц простаты и уретры вследствие гиперактивности адренорецепторов шейки мочевого пузыря, простатического отдела уретры и простаты.
Нарушение оттока мочи заставляет "напрягаться" детрузор - мышцу мочевого пузыря изгоняющую мочу. Это приводит к ее повреждению и развитию у 52-80% пациентов с ДГПЖ простаты гиперактивного мочевого пузыря.
Проявления
ДГПЖ проявляется нарушениями мочеиспускания, которые называют Симптомами Нижних Мочевыводящих Путей (СНМП):
Симптомы наполнения (раздражения) - расстройство нервно-мышечного аппарата мочевого пузыря:
частое мочеиспускание днем и ночью (ноктурия)
неотложные (императивные) позывы к мочеиспусканию
Симптомы опорожнения (обструкции) - сужение просвета уретры увеличенной простатой и спазмированными мышцами:
задержка мочеиспускания
затрудненное мочеиспускание,
необходимость выраженного напряжения передней брюшной стенки для начала мочеиспускания
слабая струя мочи
прерывистость потока мочи
капание в конце акта мочеиспускания
ощущение неполного опорожнения мочевого пузыря
Нет прямой зависимости между размерами ДГПЖ и выраженностью нарушения мочеиспускания, которая также зависит от направления роста ДГПЖ и нарушения функции мочевого пузыря. При разрастании из задней группы желез средняя доля ДГПЖ, нависая над уретрой в виде клапана, может вызвать задержку мочи. В то же время большая ДГПЖ, растущая из боковых периуретральных желез назад, в сторону прямой кишки, может не давать никаких клинических проявлений болезни.
Нередко острая (внезапная) задержка мочи становится первым клиническим проявлением ДГПЖ.
По клиническому течению выделяют три стадии ДГПЖ:
Первая стадия
Учащается мочеиспускание, особенно ночью, иногда до 5-8 раз. Струя мочи становится вялой, мочеиспускание затрудненным, со временем, чтобы опорожнить пузырь, приходится натуживаться. Возможно недержание мочи во время сна вследствие произвольного расслабления наружного сфинктера упетры. Полное опорожнение пузыря достигается благодаря комленсаторной функции мышечной стенки (детрузора) мочевого пузыря. Функция почек обычно не нарушена.
Продолжительность первой стадии от 1 до 12 лет.
Вторая стадия
Присоединяется чувство неполного опорожнения мочевого пузыря. Позывы к мочеиспусканию учащены днем и ночью. Часто в утренние часы больным приходится мочиться в 2-3 приема. Струя мочи становится отвесной, прерывается каплями, больной вынужден тужиться, что может привести к образованию грыжи или выпадению прямой кишки. При гипертрофии стенки пузыря образуется грубая складчатость, препятствующая притоку мочи из верхних мочевыводящих путей, из-за чего она застаивается в мочеточниках и почках. Постепенно наступает истончение, атония мышечных волокон детрузора. Свободная от мышечных волокон часть стенки мочевого пузыря вытягивается, образуя мешки - ложные дивертикулы мочевого пузыря. Остаточная моча составляет 100-200 мл, а иногда до литра и более. Развиваются признаки нарушения функции почек: сухость во рту, повышенная жажда и др.
Третья стадия
Количество остаточной мочи увеличивается до 1,5-2 литров. Мочевой пузырь резко растянут, его контуры просматриваются в виде шаровидной или овальной опухоли, доходящей до пупка и выше, его чувствительность снижается, и больные ошибочно полагают, что наступило улучшение. Ночью, а затем и днём моча периодически или все время выделяется непроизвольно, каплями из переполненного мочевого пузыря - парадоксальная ишурия. Появляются вызванные нарушением работы почек полная потеря аппетита, слабость, жажда, сухость во рту, тошнота запоры - хроническая почечная недостаточность. При отсутствии адекватной терапии больные умирают от уремии.
Для симптоматики при ДГПЖ характерно волнообразное течение - симптомы то усиливаются, то ослабляются даже без лечения. Ухудшение симптоматики часто бывает связано с такими провоцирующими факторами, как охлаждение, прием алкоголя, стрессы.
ДГПЖ - медленно прогрессирующее заболевание, часто без развития каких-либо симптомов. С возрастом происходит постепенный рост простаты, усиление симптомов. Встречаются и случаи улучшения как субъективных, так и объективных параметров.
ДГПЖ влияет на качество жизни пациента, вынуждает изменять свой образ жизни: ограничивать питье, вставать в течение ночи для мочеиспускания, ограничивать социальную и сексуальную активность.
Осложнения
Острая задержка мочи в I и II стадии заболевания провоцируется длительным воздержанием от мочеиспускания, запорами, поносом, переохлаждением, погрешностями в диете, приемом алкоголя (включая пиво), переутомлением, психическими стрессами, катетеризацией мочевого пузыря. После выведения мочи катетером мочеиспускание может восстановиться, либо формируется хроническая задержка мочеиспускания.
Гематурия (наличие крови в моче) обусловлена повреждением варикозно расширенных вен в области шейки мочевого пузыря при повышении в нем давления мочи или камнями мочевого пузыря, когда она возникает после ходьбы, физической нагрузки.
Камни мочевого пузыря образуются в результате застоя в нем мочи.
Дивертикулы мочевого пузыря (ложные), гидронефроз, цистит, пиелонефрит и хроническая почечная недостаточность. Хронический простатит при ДГПЖ у 70% пациентов.
Пузырно-мочеточниковый рефлюкс - заброс мочи из мочевого пузыря в мочеточник.
Диагностика
Опрос.
IPSS (International Prostatic Symptom Score - Международная шкала оценки простатических симптомов)
При пальцевом ректальном исследовании простата обычно симметрично увеличена, хотя возможна и асимметрия, со сглаженной продольной бороздкой, эластической консистенции, безболезненная.
Общие анализ крови, биохимический анализ крови, ПСА (простатспецифический антиген) для исключения Рака предстательной железы.
Анализ мочи.
УЗИ простаты трансабдоминальное: объем мочевого пузыря, толщина стенок детрузора, камни, выпячивания, опухоли мочевого пузыря, поражение верхних отделов мочевыводящих путей - мочеточники, почки, объем остаточной мочи, размер и форма предстательной железы.
Трансректальное ультразвуковое исследование (ТРУЗИ)
Рентгенологические методы показаны только при инфекции мочевыводящих путей, гематурии, мочекаменной болезни, предшествующих операциях, расширении чашечно-лоханочной системы почек, камнях и дивертикулах мочевого пузыря. При цистографии ДГПЖ видна в виде холма, вдающегося в просвет мочевого пузыря. Экскреторная урография позволяет выявить расширение чашечно-лоханочной системы и мочеточников.
Урофлоуметрия позволяет оценить скорость потока мочи.
Цистоскопия: увеличенные доли предстательной железы, вдающиеся в просвет мочевого пузыря. При наличии камней их обнаруживают визуально.
Дифференциальная диагностика
Простатит, рак предстательной железы, стриктура уретры, склероз шейки мочевого пузыря, нейрогенный мочевой пузырь.
Исключение заболеваний нервной системы, сопровождающихся расстройствами мочеиспускания, похожими на имеющиеся при ДГПЖ (сфинктеро-детрузорная псевдодиссинергия, тоннельная пудендопатия, миофасциальный синдром тазового дна).
Лечение
Лечение ДГПЖ зависит от стадии заболевания и индивидуальных особенностей, индивидуальной переносимости препаратов.
В I стадии лечение обычно консервативное.
Во II стадии при отсутствии эффекта от консервативного - оперативное лечение.
В III стадии только хирургическое лечение.
Медикаментозное лечение
Растительные препараты, чаще производные вееролистной пальмы (Saw Palmetto, Sabal Serullata) и африканской сливы (Pygeum Africanum) имеют противовоспалительное и противоотечное действие. Экстракт Saw Palmetto по механизму действия близок к ингибиторам 5 a-редуктазы (финастериду), но эффект его менее выражен. Экстракт Pygeum Africanum снижает активность факторов роста и тем самым тормозит развитие узелков гиперплазии в простате, защищает мочевой пузырь от поражения при ДГПЖ. Также используют препараты на основе семян тыквы, крапивы.
a-адреноблокаторы действуют симптоматически, расслабляя мышечный компонент простаты и уретры. В результате улучшается поток мочи и снижается выраженность симптомов. a-адреноблокаторы снижают артериальное давление и могут вызывать ретроградную эякуляцию.
Ингибитор 5 a-редуктазы финастерид используется при размерах простаты более 40 мл. Он снижает либидо, потенцию, уменьшает объем спермы, в некоторых случаях вызывает гинекомастию (увеличение грудной железы).
При больших размерах простаты более эффективны ингибиторы 5 a-редуктазы, при выраженной симптоматике в комбинации с альфа-блокаторами. Если размеры железы не велики, а симптомы выражены, альфа-блокаторы сочетают с растительными экстрактами для торможения развития ДГПЖ. Если же симптомы выражены слабо или умеренно, железа увеличена умеренно в сочетании с хроническим простатитом, назначают растительные экстракты.
Инвазивное лечение
Проводится при неэффективности консервативного и если имеются:
острая задержка мочеиспускания, не устранимая консервативно
гидронефроз
почечная недостаточность
большой дивертикул мочевого пузыря
рецидивирующая инфекция мочевого тракта
камни мочевого пузыря
рецидивирующая гематурия (наличие крови в моче)
В последнее время предпочтение часто отдается эндоскопическим методикам лечения ДГПЖ:
трансуретральная резекция предстательной железы (ТУРП)
трансуретральная электровапоризация предстательной железы (ТУВП или ТУВ)
трансуретральная инцизия предстательной железы (ТУИП)
трансуретральная игольчатая абляция простаты (TUNA)
лазерные методы
При больших размерах ДГПЖ применяется открытое хирургическое вмешательство - аденомэктомия, в зарубежной литературе - простатэктомия. Оперативное вмешательство далеко не всегда избавляет пациента от проблем с мочеиспусканием, которые могут быть обусловлены спазмированием мышц и нарушением работы мочевого пузыря.
Минимально инвазивные неэндоскопические методы лечения
катетеризация мочевого пузыря при невозможности операции
микроволновая гипертермия, термальная терапия при отсутствии риска малигнизации опухоли
балонная дилятация
термальные методы - трансуретральная микроволновая микроволновая терапия (ТУМТ)
фокусированный ультразвук высокой интенсивности
криодеструкция (разрушение холодом)
инъекции этанола (спирта)
стенты
Воздействие температуры на ткани:
гипертермия (41°-45°) - происходит воздействие в первую очередь на злокачественные клетки, нормальные также подвергаются воздействию, но выживают
термотерапия (45°-60°) - селективность к нормальным и новообразованным клеткам теряется
абляция (60°-100°) - коагуляционный некроз и удаление ткани
>100° - вапоризация (испарение)
Осложнения оперативного лечения: ретроградная эякуляция и эректильная дисфункция.
Профилактика
Эффективная профилактика ДГПЖ отсутствует.
Мужчинам старше 40 лет показаны профилактические осмотры у уролога для исключения рака предстательной железы.
Варикоцеле. Классификация. Клинические проявления, принципы лечения.
Варикоцеле - это варикозное расширение вен яичка и семенного канатика. Варикоцеле одно из самых распространенных заболеваний среди мужчин, которое часто приводит к весьма неприятным последствиям.
Причины варикоцеле
Варикоцеле развивается в результате двух причин.
1. Врожденная слабость сосудистой стенки. Чаще всего варикоцеле развивается в результате генетической предрасположенности к такого рода проблемам. Практически всегда у кого-то из родственников пациента с варикоцеле обнаруживаются варикозное расширение вен конечностей, плоскостопие, пороки клапанов сердца, фимоз или другие проявления недостаточности соединительной ткани. Часто эти заболевания сопутствуют друг другу.
2. Повышенное давление крови в венах малого таза или мошонки. На самом деле это скорее предрасполагающий фактор, нежели причина заболевания. Но иногда встречаются настолько явно выраженные анатомические изменения, ведущие к повышению давления в венах, что этот фактор становится причиной варикоцеле. Яичковая вена может перегибаться, пережиматься другими сосудами, проходить через складки тканей и т.д. Все это приводит к сужению просвета вены и как следствие - повышению давления в ней.
Реже повышение давления крови в вене вызывается общими явлениями - хронические запоры или диарея, поднятие тяжестей, напряжение мышц брюшного пресса и т.д. Эти факторы могут способствовать развитию варикоцеле, но едва ли способны стать причиной заболевания.
Патогенез
По венам мошонки кровь течет от яичка и окружающих тканей к сердцу. При этом кровь течет снизу вверх, против силы тяжести. В норме обратному току крови по венам препятствует специальный клапанный аппарат венозной стенки. При расширении вен эти клапаны перестают работать, в результате чего кровь начинает совершать в вене так называемые "маятникообразные движения". В итоге кровоток резко замедляется, и страдает кровоснабжение яичка в целом.
Нарушение кровоснабжения яичка приводит к тому, что его обедненные кислородом ткани начинают хуже функционировать. Кроме того, температура яичек в норме на несколько градусов ниже температуры тела. При варикоцеле яичко находится в окружении сплетения расширенных вен, температура его становится равной температуре тела, и функция угнетается еще больше. Все это приводит к появлению симптомов заболевания.
Степени развития варикоцеле
По тому, насколько сильно расширены вены яичка и семенного канатика, различают 4 степени варикоцеле.
1 степень - вены яичка не прощупываются руками, их варикозное расширение определяется только инструментально (УЗИ, допплерография).
2 степень - расширение вен прощупывается в положении стоя, в положении лежа варикоцеле не определяется.
3 степень - расширенные вены прощупываются и в положение стоя, и в положение лежа.
4 степень - расширенные вены яичка и семенного канатика видны невооруженным глазом.
Чаще всего варикоцеле развивается у юношей в период полового созревания, быстро достигает какой-то степени и больше не прогрессирует. Крайне редко одна степень варикоцеле переходит в другую.
Практически всегда варикоцеле бывает левосторонним. Очень редко приходится сталкиваться с двусторонним варикоцеле и исключительно редко варикоцеле развивается справа.
Проявления варикоцеле
Как уже было сказано, при варикоцеле страдает функция яичка. Это может проявляться двумя путями - либо возникает боль или неприятные ощущения в яичках, либо мужчина становится бесплодным.
Описанные симптомы встречаются у разных мужчин с варикоцеле по-разному. Если принять всех мужчин, страдающих варикоцеле, за 100%, то у половины из них не будет никаких проявлений заболевания, 25% будут испытывать неприятные ощущения в яичке и 25% будут страдать бесплодием. Причем эти цифры никак не зависят от стадии заболевания.
Боли в яичках при варикоцеле
Чаще всего боли или неприятные ощущения имеют тянущий, давящий характер, часто пациенты описывают это состояние как тяжесть в мошонке. Обычно эти ощущения не присутствуют постоянно, а появляются после физических нагрузок, полового акта, тепловых процедур или после длительного малоподвижного состояния.
Совсем необязательно неприятные ощущения в мошонке при левостороннем варикоцеле появляются именно слева. Чаще всего пациенты затрудняются определить, в какой половине они выражены сильнее, и нередко боли локализуются главным образом справа.
Бесплодие и варикоцеле
Среди всех мужчин, страдающих бесплодием, варикоцеле отмечается у 40% из них. При этом относительно редко варикоцеле проявляется какими-либо другими симптомами. Поэтому все мужчины, показатели спермограммы которых не соответствуют норме, обязательно должны пройти обследование на этот счет.
Бессимптомное течение варикоцеле
Это наиболее распространенный вариант заболевания. Большая часть случаев варикоцеле протекает бессимптомно, никак не беспокоит человека. Многие мужчины живут с варикоцеле всю жизнь, имеют детей и знать не знают ничего про это заболевание. Часто варикоцеле оказывается случайной находкой при прохождении осмотра совершенно по другому поводу.
Диагностика варикоцеле
Начиная со второй степени варикоцеле обнаруживается урологом при осмотре. Если увеличение вен значительное, и диагноз не оставляет сомнений, то дополнительного обследования не требуется. Если степень варикоцеле маленькая, то нужно провести специальное обследование - УЗИ или допплерографию мошонки.
УЗИ или допплерография при подозрении на варикоцеле обязательно должны проводиться в двух положениях пациента - лежа и стоя. Если это не сделано, обследование теряет всякий смысл.
Какой именно метод обследования выбрать, большого значения не имеет. Допплерография точнее, и позволяет окончательно подтвердить или опровергнуть диагноз. Однако выполненное грамотным специалистом УЗИ органов мошонки также рассеивает все сомнения по поводу диагноза варикоцеле.
Допплерография или УЗИ мошонки в положениях лежа и стоя должны обязательно проводиться всем мужчинам при бесплодии и при болях в яичках.
Помимо всего сказанного, при варикоцеле обязательно должна быть сделана спермограмма.
Лечение варикоцеле
Существуют только оперативные способы лечения варикоцеле. Если вам придется где-нибудь услышать о лечении варикоцеле без операции - не верьте этому, эффективного лечения варикоцеле без операции не существует.
Операция при варикоцеле должна быть проведена обязательно, если заболевание проявляется болями в мошонке или бесплодием. И в том и в другом случае избавиться от варикоцеле - единственный путь избавления от проявлений заболевания.
Если же мужчину с варикоцеле ничего не беспокоит, необходимость операции является спорным вопросом. Обычно он решается исходя из возможности бесплодия. Если мужчина еще предполагает иметь детей, то операцию лучше сделать, если нет, то без нее можно обойтись. Чаще всего получается, что если варикоцеле обнаружено у подростка или молодого мужчины, то есть смысл избавиться от заболевания, а если речь идет о мужчине в возрасте, то делать это не обязательно.
Есть несколько видов операций при варикоцеле, и все они делятся на два типа.
1 тип. Суть операций этого типа заключается в том, чтобы полностью перевязать, пересечь или удалить варикозно расширенную вену.
Достоинства операций этого типа: относительная простота исполнения, минимальный объем оперативного вмешательства, минимальное время нахождения в стационаре, меньшая стоимость по сравнению с операциями второго типа.
Недостатки: относительно высокий процент рецидивов и нефизиологичность операции.
Рецидивы при операциях первого типа связаны с тем, что вены у каждого человека расположены индивидуально и могут варьировать в очень широких пределах. Если от варикозно расширенной вены отходит веточка, и при операции эту веточку не заметят и не перевяжут, никакого результата операция не даст. Это принято называть рецидивом заболевания, но фактически это просто неэффективность лечения. Для разных операций первого типа процент рецидивов разный, в зависимости от вида операции он колеблется от 10% до 40%.
Второй недостаток - нефизиологичность этих операций. Как уже было сказано, результатом операции является полное прекращение кровотока по расширенной вене. В результате яичко остается без кровообращения, и под влиянием этого стресса открываются новые пути для сброса крови.
Этот процесс занимает около недели. В течение этой недели нередко яичко начинает болеть, а если боли в яичке были и раньше, они заметно усиливаются. Также есть данные, что во время этих событий может нарушаться барьер между тканью яичка и иммунной системой, в результате чего в крови появляются антиспермальные антитела, и у мужчины развивается или прогрессирует бесплодие.
2 тип. При операции этого типа вены яичка удаляются полностью, а затем осуществляется их восстановление - пластика. Этот тип операций представлен только одним видом операции, которая носит название микрохирургическая реваскуляризация яичка.
Преимущества этой операции заключается в том, что сразу после операции в яичке восстанавливается нормальное кровообращение. Варикозно расширенные вены при этом полностью удаляются, и рецидив заболевания полностью исключен. После микрохирургической реваскуляризации яичка пациент не испытывает болей в течение недели, как при операциях 1 типа.
Недостатки операции: высокая сложность оперативного вмешательства, более продолжительное нахождение в стационаре, более высокая стоимость операции.
Профилактика варикоцеле
Варикоцеле развивается главным образом в силу анатомической или генетической предрасположенности к этому заболеванию. Поэтому ни о какой особенной профилактике варикоцеле речь не идет. После окончания периода полового созревания (лет 19-20) есть смысл пройти обследование у уролога, и если никаких признаков варикоцеле обнаружено не будет, на этот счет можно не волноваться.
Если варикоцеле уже есть, то нужно стараться избегать тяжелых физических нагрузок и проблем со стулом. И то и другое ведет к повышению внутрибрюшного давления и в результате давления крови в венах малого таза, что может привести к прогрессированию заболевания.
Водянка яичка и семенного канатика. Клинические проявления. Принципы лечения.
Водянка яичка — это состояние, при котором во влагалищной оболочке мошонки в результате врождённого порока или воспалительных заболеваний собирается серозная жидкость. Также при водянке яичка жидкость может происходить из семенного канатика или влагалищного отростка брюшины, собираясь в мошонке.
Происхождение водянки яичка
Эмбриологически влагалищный отросток представляет собой выпячивание перитонеальной брюшины, который (отросток) нисходит совместно с яичком в мошонку через паховый канал приблизительно на 28-ю неделю гестационного периода, постепенно зарастая в период младенчества и детства.
В связи с эти по строению водянку яичка можно разделить на 3 группы.
Сообщающаяся водянка яичка (врождённая водянка яичка) , при котором из-за незаращения влагалищного отростка брюшины перитонеальная жидкость поступает и скапливается в мошонке. Также при этом пороке развития часто образуются косые паховые грыжи.
Несообщающаяся водянка яичка, при котором влагалищный отросток не зарастает полностью, однако не сообщается с брюшной полостью.
Водянка семенного канатика — это вариант водянки яичка, при котором средняя часть влагалищного отростка остаётся незаращённой при закрытом дистальном его конце. Проксимальный же конец влагалищного отростка может быть как открытым, так и закрытым.
Водянка яичка у взрослых обычно бывают вторичными. Причиной первичных водянок яичка при остром течении могут быть травмы, инфекции, лучевая терапия. При хроническом же течении водянка яичка является следствием постепенного скопления жидкости, как результат хронической инфекции после хирургических вмешательств. Водянка яичка также обратимо может влиять на фертильность.
Клиническое течение водянки яичка
Большинство случаев водянок яичка проходит бессимптомно или же сопровождается незначительными клиническими проявлениями. Необходимо определить начало и продолжительность заболевания, а также оценить степени тяжести водянки яичек. Также следует установить имевшиеся в анамнезе заболевания и особенности мочеполовой системы, сексуальный анамнез, травмы в недавнем прошлом или системные заболевания. Обычным симптомом водянки яичка является увеличенная безболезненная мошонка. Могут возникать чувство тяжести, распирания, тянущие ощущения или дискомфорт в области мошонки. Реже могут быть жалобы на чувство дискомфорта, распространяющееся по подвздошной и поясничной области. Водянка яичка обычно безболезненна. Боль часто является симптомом присоединившихся инфекционных осложнений (острого эпидидимита). Размеры мошонки могут варьировать — уменьшаясь в лежачем положении и увеличиваясь в положении стоя.
Размеры водянок яичка, протекающих хронически, обычно превосходят таковые при остром течении. Общие симптомы, такие как лихорадка, озноб, тошнота, рвота, обычно отсутствуют при неосложнённом гидроцеле. Клинические проявления со стороны мочеполовой системы также не характерны для неосложнённого течения водянки яичка.
Осложнения водянки яичка
Крайне большие размеры водянки яичка могут привести к нарушению кровообращения в яичке. Это может стать причиной атрофии ткани яичка и привести в последующем к бесплодию.
В результате травмы может возникнуть кровотечение в полость водянки яичка.
Ущемление или сдавление сопутствующей грыжи.
Осмотр при водянке яичка
Водянка яичка – это скопление жидкости вокруг яичка, которая располагается выше и спереди по отношению к яичку, в отличие от сперматоцеле, которое обычно находится выше и позади яичка.
В 7-10 % случаев водянка яичка бывает двусторонней. Также водянка яичка часто сочетается с грыжами, особенно справа. Размеры и консистенция мошонки при пальпации могут изменяться в зависимости от положения тела. Обычно мошонка становится меньше и мягче в лежачем положении и увеличивается и становится более напряжённой после долгого стояния. Признаки интоксикации организма обычно отсутствуют. Пациенты обычно не температурят, сохраняя в норме все основные жизненные показатели. Живот и яички обычно безболезненны, вздутия живота не наблюдается. Перистальтические шумы аускультируются в мошонке в случае наличия грыжевого кишечного содержимого в мошонке. При отсутствии инфекционных осложнений при остром течении водянки яичка не наблюдается гиперемии или изменения цвета кожи мошонки.
Диафаноскопия – это наиболее простой способ диагностики водянки яичка.
Полость водянки яичка свободно проницаема для лучей, установленного позади мошонки источника света – это положительный симптом просвечивания. Диафаноскопия рутинный, но не специфичный метод диагностики водянки яичка. Диафаноскопия может использоваться для дифференцировки с другими заболеваниями, сопровождающимися увеличением мошонки (например, грыжи или опухоли).
Диагностика водянки яичка
Важно провести дифференциальную диагностику между водянкой яичка и различными острыми заболеваниями органов мошонки (перекрут яичка, ущемлённая грыжа). Около 50% острых состояний в начальных стадиях не диагностируются. Диафаноскопия при подобных острых состояниях не может выявить степень тяжести заболевания. Ультразвуковое исследование и допплерография кровотока в яичке показаны при подозрении на острые заболевания органов мошонки:
Травматическое кровоизлияние в полость водянки яичка.
Перекрут яичка с или без вторичной водянкой яичек.
Ишемия (нарушение кровоснабжения) яичка.
УЗИ может с точностью подтвердить диагноз. Также ультразвуковое исследование помогает определить аномалии развития яичка, кисты придатка яичка, опухолевые образования органов мошонки, состояние придатков, сперматоцеле, грыжи.
При наличии боли или гематоцеле (наличие крови в мошонке) после травмы, ультразвуковое исследование может помочь в дифференцировке между водянкой яичка и ущемлением грыжи. Водянка яичка выявляется как полость заполненная жидкостью внутри семенного канатика или окружающая яичко.
Доплерография водянки яичка используется для оценки кровообращения. Необходимо срочно выполнять допплерографию при подозрении на перекрут яичка или кровотечение, обусловленное травмой мошонки или промежности. Однако малодоступность данного метода исследования в клинической практике снижает его пользу.
Сцинтиграфия яичек – это радиоизотопный метод исследования чрезвычайно полезен у детей при подозрении на перекрут яичка. Снижение или отсутствие потока к одному из яичек предполагает наличие перекрута. Чувствительность метода до 90%, однако данный процент снижается у младенцев, при ранних перекрутах, неполных перекрутах, и последующем самостоятельном устранении перекрута. Специфичность сцинтиграфии яичек для перекрута яичек может быть до 90%, однако она снижается при наличии в мошонке жидкости (водянка яичка, грыжа, абсцесс, кровь).
Л ечение
водянки яичка
ечение
водянки яичка
Прогноз при врождённой водянке яичка весьма благоприятный. Большинство врождённых случаев водянки яичка разрешаются самостоятельно к первому году жизни. Если этого не происходит, То водянку яика необходимо лечить. Водянка яичка легко устраняется хирургическими методами.
У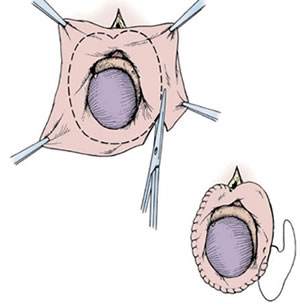 детей водянка
яичка
лечится
лигированием (перевязкой) открытого
влагалищного отростка брюшины через
разрезы в паховой области с иссечением
дистального мешка. В случаях вторичного
происхождения водянки
яичка
прогноз
лечения
зависит от основного заболевания.
детей водянка
яичка
лечится
лигированием (перевязкой) открытого
влагалищного отростка брюшины через
разрезы в паховой области с иссечением
дистального мешка. В случаях вторичного
происхождения водянки
яичка
прогноз
лечения
зависит от основного заболевания.
У взрослых и пожилых мужчин возникновение водянки яичка иногда связано со злокачественными новообразованиями и редко разрешается без хирургического лечения.
К роме
того возможен вариант
лечения водянки
яичка
отсасыванием жидкости из полости водянки
яичка
при помощи иглы – пункционные
способ лечения водянки
яичка.
Этот вид лечения мало распространён,
так как обычно водяночная жидкость
вновь накапливается в оболочках яичка.
Введение склерозирующих препаратов
после аспирации водяночной жидкости
может предотвратить рецидив пункционного
способа лечения
водянки
яичка.
Аспирация и введение слерозирующих
препаратов показано пациентам с высоким
хирургическим риском.
роме
того возможен вариант
лечения водянки
яичка
отсасыванием жидкости из полости водянки
яичка
при помощи иглы – пункционные
способ лечения водянки
яичка.
Этот вид лечения мало распространён,
так как обычно водяночная жидкость
вновь накапливается в оболочках яичка.
Введение склерозирующих препаратов
после аспирации водяночной жидкости
может предотвратить рецидив пункционного
способа лечения
водянки
яичка.
Аспирация и введение слерозирующих
препаратов показано пациентам с высоким
хирургическим риском.
Оперативное лечение водянки яичка
И
Лечение водянки
яичка — операция Винкельмана
Лечение водянки
яичка — операция Бергмана
Исход операции водянки яичка
Мошонка может оставаться увеличенной до одного месяца. Пациент может вернуться к повседневной деятельности в течение 7-10 дней, однако следует избегать подъёма тяжестей и половой жизни до 6 недель. При правильной технике оперативного лечения водянка яичка не рецидивирует.
Нежелательный исход
Припухлость мошонки, сохраняющаяся в течение нескольких месяцев, может рассматриваться как осложнение иссечения водянки. Также может быть инфицирование раны.
Лечение водянки
яичка — операция Лорда
Крипторхизм. Клинические проявления. Принципы лечения.
Крипторхизм - это состояние, при котором одно или оба яичка не находятся на своем месте в мошонке. При внутриутробном развитии яички располагаются в брюшной полости плода. В норме незадолго до родов яички опускаются в мошонку и у доношенного ребенка при рождении или в первые дни после рождения яички должны определяться в мошонке.
Крипторхизм довольно часто встречается в детской урологии. Так, у доношенных детей он диагностируется в 3 % случаев, а у недоношенных - в 30 %. Однако после года жизни ребенка соответственно у 75 и 90 % детей яички самостоятельно опускаются в мошонку, и общая частота крипторхизма в популяции в годовалом возрасте составляет 1-2 %. Двусторонний крипторхизм имеет место у 10% пациентов.
Этиология заболевания неизвестна.
Большое значение данной нозологии обусловлено тем, что при крипторхизме:
Риск развития рака яичка выше в 20-40 раз. 10% случаев от общего числа тестикулярного рака развивается в неопущенном яичке. Вероятность развития рака в 4 раза выше при внутрибрюшном крипторхизме, чем при ингвинальным (паховым).
Нарушается фертильность. Только 30 % пациентов с двусторонним крипторхизмом фертильны. Нарушения фертильности более выражены при более высоком расположении яичка и более продолжительном нахождении его вне мошонки.
Чаще встречается сопутствующая мошоночная грыжа.
Повышен риск перекрута яичка, особенно в постпубертатном периоде.
Классификация. Классификация состояний, сопряженных с отсутствием одного или обоих яичек в мошонке, проводится в зависимости от расположения яичка следующим образом:
Внутрибрюшной крипторхизм (10% случаев) - яичко расположено проксимальнее внутреннего пахового кольца в брюшной полости.
Ингвинальный (паховый) крипторхизм - яичко расположено в паховом канале между наружным и внутренним паховым кольцом.
Эктопия яичка (5% случаев) - яичко расположено дистальнее внутреннего пахового кольца, но вне своего обычного пути опущения в мошонку. Чаще всего эктопированное яичко обнаруживается в паховой области (паховая эктопия), в промежности, на бедре (бедренная эктопия), у корня полового члена, над лоном и, изредка, в противоположной половине мошонки.
Анорхизм (4% случаев) - врожденное отсутствие яичек.
Блуждающее яичко (ложный крипторхизм) - строго говоря, не является проявлением крипторхизма. При данном состоянии имеет место высокий рефлекс кремастера - мышцы, поднимающей яичко. Кремастерный рефлекс имеет наибольшую активность в возрасте от 2 до 7 лет. Яичко обычно определяется в субингвинальной или премошоночной области и может быть без усилия помещено обратно в мошонку.
Диагностика. Обследование пациента при отсутствии яичка в мошонке проводят в теплом помещении. Пальцы одной руки располагают у основания мошонки, предотвращая смещение яичка, другой рукой осуществляют пальпацию. Если яичка в мошонке нет, то пальпируют паховый канал (по направлению от верхней передней подвздошной ости вниз и медиально к лобковому бугорку), промежность, надлонную область и бедренный канал. Если яичко находится у выхода из пахового канала, его деликатно пытаются низвести в мошонку, что позволяет провести дифференциальную диагностику между истинным и ложным крипторхизмом. Для того чтобы отличить крипторхизм от врожденного отсутствия или эктопии яичка, проводится УЗИ или МРТ брюшной полости и органов малого таза. Если яичко не пальпируется, в ряде случаев проводится лапароскопия с последующим низведением яичка в случае обнаружения его в брюшной полости. При отсутствии пальпируемых яичек с обеих сторон до оперативных манипуляций показано проведение теста с введением хорионического гонадотропина и определение базального уровня фолликулостимулирующего (ФСГ) и лютеинизирующего (ЛГ) гормонов. При отсутствии повышения уровня тестостерона в ответ на введение хорионического гонадотропина и повышенных базальных уровнях ФСГ и ЛГ достоверно устанавливается диагноз анорхизма.
Лечение. Целью лечения крипторхизма является восстановление нормального положения яичек до наступления 2-го года жизни ребенка, поскольку если в 2 года яичко не опустилось в мошонку, происходит необратимое нарушение сперматогенеза. Консервативные методы лечения крипторхизма предполагают использование хорионического гонадотропина или рилизинг-фактора (рилизинг-гормона) лютеинизирующего гормона. Эффективность гормонотерапии составляет 20-30 %. При эктопии яичка она неэффективна, однако может быть использована для улучшения состояния тканей перед операцией.
Нередко при крипторхизме сразу же рекомендуют оперативное лечение, особенно, если речь идет о расположении одного или обоих яичек в брюшной полости, эктопии яичка или сочетании крипторхизма с пахово-мошоночной грыжей, незаращением влагалищного отростка и прочими аномалиями. Операциями выбора являются орхидофуникулолизис (освобождение яичка и семенного канатика от окружающих тканей) и орхипексия (фиксация яичка в мошонке после предварительного низведения). Орхипексия в раннем возрасте снижает риск развития рака яичка. При грубых морфологических изменениях производится удаление яичка. Лучший возраст для операции орхипексии - 12-18 мес.
Рак предстательной железы. Этиология, клиника, диагностика. Современные методы медикаментозного и хирургического лечения.
На сегодняшний день смертность от рака предстательной железы у мужчин стоит на втором месте после рака легких. Рак предстательной железы может развиться абсолютно у любого мужчины старше 45-50 лет.
Причины до конца не выяснены. Развитие рака простаты связывают с гормональными изменениями у мужчин пожилого возраста, в частности, с высоким уровнем тестостерона — мужского полового гормона. Рак предстательной железы является гормонозависимой опухолью, то есть рост опухоли стимулируется тестостероном. Поэтому у мужчин, у которых уровень тестостерона в крови выше, возникновение рака простаты вероятнее и течение его будет злокачественнее.
Рак предстательной железы отличается медленным и злокачественным течением, дает ранние метастазы. Чаще всего распростаранение идет в кости (таз, бедра, позвоночник), легкие, печень, надпочечники.
Клиника
Рак предстательной железы может проявляться учащением мочеиспускания, болями в промежности, кровью в моче и в сперме. Но может не отмечаться ни одного из этих симптомов. Тогда первым проявлением заболевания станут метастазы раковой опухоли. Это могут быть боли в костях (в тазу, бедрах, позвоночнике), боли в груди. В далеко зашедших случаях может развиться острая задержка мочи, а так же симптомы раковой интоксикации — резкое похудание, слабость, бледность кожи с землистым оттенком.
Диагностика
Пальпация предстательной желези через прямую кишку (пальцевое ректальное исследование).
Лабораторные исследования: Самым лучшим и прогрессивным методом на сегодняшний день является определение в крови ПСА (PSA) — так называемого простатспецифического антигена. Преимущество этого метода заключается в том, что сегодня это практически единственный способ заподозрить рак простаты на самой ранней стадии.
Другие исследования — УЗИ, рентгеновские методы, позволяют определить размер опухоли и состояние других органов.
Окончательный диагноз рака предстательной железы ставится после проведения биопсии простаты — специальной иглой через промежность или через прямую кишку берется маленький кусочек железы для исследования.
Методы лечения рака
Оперативные методы лечения применяются только тогда, когда опухоль еще не дала метастазов. В этом случае выполняется удаление предстательной железы примерно также, как это описано в вопросе "Аденома предстательной железы".
Медикаментозные методы лечения представляют собой лечение гормонами. Гормональные препараты снижают или блокируют тестостерон, и это позволяет уменьшить скорость роста опухоли и ее метастазов.
Обладают рядом неприятных побочных эффектов — повышение артериального давления, снижение потенции, гинекомастия и другими.
Лучевая терапия представляет собой облучение области предстательной железы радиоактивным излучением. Это позволяет снизить скорость роста опухоли, уменьшить вероятность появления метастазов. Часто лучевая и медикаментозная терапия применяются вместе для усиления эффекта лечения.
Профилактика
Рекомендуется каждому мужчине старше 45 лет раз в год делать анализ крови на ПСА и консультироваться у уролога по поводу результатов анализа. Если есть подозрение на рак, то обязательно должна быть выполнена биопсия простаты, а в случае подтверждения диагноза — операция удаления предстательной железы.
Аномалии почек: классификация, клиника, диагностика, лечение.
Согласно современной классификации, различают следующие аномалии почки:
1. Аномалии почек
1.1 Аномалии количества почек (Агенезия, Добавочная почка)
1.2 Аномалии положения почек (Дистопия (эктопия))
2. Аномалии взаимоотношения почек (Симметричные и Ассиметричные формы сращения)
3. Аномалии величины и структуры почек
3.1 Аплазия почки
3.2 Гипоплазия почки
4. Кистозные аномалии почек
4.1 Поликистоз почек
4.2 Губчатая почка (болезнь Каччи - Риччи)
4.3 Мультикистозная дисплазия
4.4. Мультиокулярная киста
4.5. Солитарная киста
5. Удвоение почки и мочеточников
Аномалии количества почек
Агенезия. Отсутствие закладки почки. Встречается с частотой 1 на 1000 новорожденных. Чаще встречается у плодов мужского пола (1: 3). Дети с агенезией обоих почек нежизнеспособны и обычно рождаются мертвыми. Часто сочетается с агенезией мочевого пузыря, дисплазией половых органов. Единственная почка гипертрофированна и компенсирует отсутствие второй почки. Однако повышенная на нее нагрузка способствует развитию пиелонефрита, литиаза. Она может быть врожденно - дефектной. Диагноз ставится на основании рентгенологического исследования, хромоцистоскопии, почечной ангиографии.
Добавочная почка. Редкая аномалия. Добавочная почка меньше обычной, имеет нормальное анатомическое строение. Артерии ее кровоснабжающие отходят от аорты. Мочеточник впадает в мочевой пузырь самостоятельным устьем, может сообщаться с мочеточником основной почки. Клиническое значение добавочная почка имеет лишь при эктопии мочеточника, при поражении опухолевым или воспалительным процессом.
Диагноз основывается на рентгенографии:
выделительная урография
ретроградная пиелография
аортография
Лечение: нефрэктомия.
