
- •Основний постулат і основна ідея статистичної фізики
- •Розподіл Максвела – приклад статистичного розподілу.
- •Фізичний зміст параметрів розподілу Максвела.
- •Тепер запишемо вирази для густини імовірності
- •Властивості і застосування максвелівського розподілу. Розподіл компонента швидкості
- •Розподіл Больцмана.
- •Мікроскопічний опис макроскопічних систем
- •Мікроскопічний опис класичної системи.
- •Фазовий простір.
- •Фазовий об’єм у - просторі.
- •Фазовий об’єм ідеального газу
- •Внаслідок незалежності координат і імпульсів частинок фазовий об’єм системи
- •Задання мікростану квантової системи.
- •Енергія всього газу системи
- •Розрахунок числа можливих станів для ідеального газу.
- •Співвідношення невизначеностей і число квантових станів.
- •Закони статистичного розподілу для систем багатьох частинок
- •Залежність функції розподілу від енергії системи.
- •2. Мікроканонічний розподіл.
- •Канонічний розподіл Гіббса.
- •Великий канонічний розподіл Гіббса.
- •Квантові статистики.
- •06601, Київ-30, вул. Пирогова, 9.
Фізичний зміст параметрів розподілу Максвела.
Одна з умов для визначення сталих С і випливає з вимоги, щоб інтеграл від густини імовірності по всіх можливих значеннях аргументу був рівний одиниці. Ця умова називається умовою нормування і записується так:
![]() або
або
![]() .
.![]()
Звідси стала С визначається через сталу :
![]() .
.
З
останнього виразу видно, зокрема, що
стала
повинна бути додатна, оскільки в
противному випадку інтеграл розходиться
і стала С
виявляється
рівною нулю. Значення визначеного
інтеграла
![]() можна знайти в таблицях, воно виявляється
рівним
можна знайти в таблицях, воно виявляється
рівним
![]() .Остаточно
одержуємо:
.Остаточно
одержуємо:
|
(8) |
Стала залежить від умов, в яких знаходиться газ, і тому її можна виразити через параметри газу. Для цього розглянемо конкретне фізичне завдання. Користуючись уже відомим способом знаходження середніх статистичних, знайдемо середню кінетичну енергію, яка припадає на один ступінь вільності розглядуваного ідеального газу (на компоненту vx):
![]()
(за теоремою про рівномірний розподіл енергії).
Для
знаходження інтеграла
![]() ,
продиференціюємо по
рівняння
,
продиференціюємо по
рівняння
![]()
Враховуючи одержане, можна записати
![]() .
.
Звідси
|
(9) |
За допомогою цього співвідношення до статистичної теорії вводиться температура Т.
Тепер запишемо вирази для густини імовірності
|
(10) |
|
(11) |
Розподіли імовірностей (10) і (11) нормовані на одну молекулу газу.
Формула (11) відома як функція розподілу Максвела.
Зважаючи
на те, що
![]() ,
функцію розподілу Максвела можна
записати так:
,
функцію розподілу Максвела можна
записати так:
|
(12) |
Зауважимо,
що
![]() якщо
якщо
![]() - це відображення симетрії руху молекул
– якщо центр мас всього газу нерухомий,
то переважного напрямку швидкості
немає.
- це відображення симетрії руху молекул
– якщо центр мас всього газу нерухомий,
то переважного напрямку швидкості
немає.
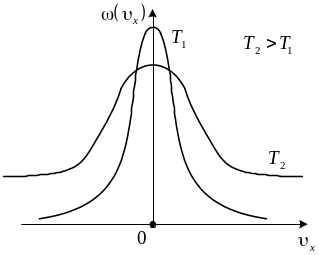
Властивості і застосування максвелівського розподілу. Розподіл компонента швидкості
Густина імовірності
для компонента швидкості
![]() обчислюється за формулою (10). Вона
нормована на одну молекулу:
обчислюється за формулою (10). Вона
нормована на одну молекулу:
![]() - імовірність того, що компонента (vx)
знаходиться в інтервалі [vx,
vx+dvx,].
- імовірність того, що компонента (vx)
знаходиться в інтервалі [vx,
vx+dvx,].
Якщо інтервал dvx досить малий, то число молекул, компоненти швидкості яких знаходяться у цьому інтервалі, визначаються формулою:
![]() ,
,
де N - загальне число молекул газу.
|
|
|
![]() :
:
чим
більша Т,
тим менша
![]() .
З температурою пов’язана також
“напівширина” розподілу, тобто величина
.
З температурою пов’язана також
“напівширина” розподілу, тобто величина
![]() ,
що відповідає
,
що відповідає
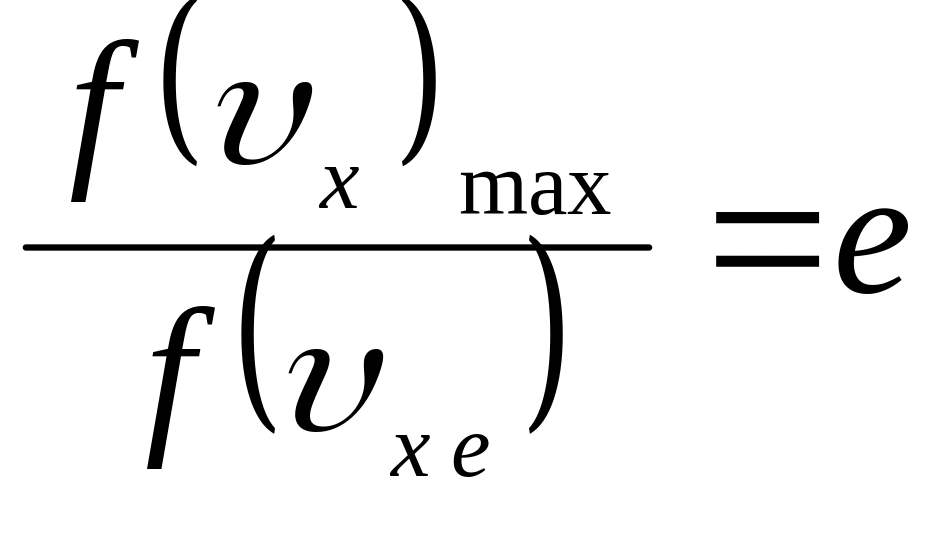 - зменшенню функції розподілу в е
разів порівняно з
- зменшенню функції розподілу в е
разів порівняно з
![]() значенням. Ця “напівширина” визначається
з умови
значенням. Ця “напівширина” визначається
з умови
![]()
Таким чином, із зменшенням температури розподіл стає “вужчим” і “вищим”, що пояснюється зменшенням середньої кінетичної енергії молекули при Т0
Розподіл швидкостей молекул за абсолютним значенням.
Ми уже зауважували,
що F(![]() )=F(
)=F(![]() )
якщо абсолютні значення
і
однакові.
)
якщо абсолютні значення
і
однакові.
Знайдемо імовірність того, що швидкість деякої молекули має значення в інтервалі [v, v+dv,].
![]() .
.
Цю імовірність можна знайти скориставшись теоремою про додавання імовірностей несумісних подій (якщо молекула має швидкість та в цей момент вона не може мати швидкість - несумісні події), додаючи імовірності однакових за модулями але різних за напрямами швидкостей:
![]()
Сумування
ведеться по всіх
![]() для яких
для яких
![]() однакова.
Тоді
можна винести за знак суми, а
однакова.
Тоді
можна винести за знак суми, а
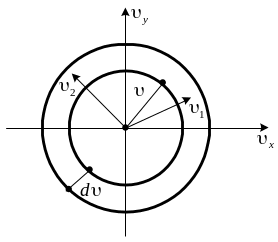
![]() -
це об’єм сферичного шару, обмеженого
сферами з радіусами v
і v+dv:
=
-
це об’єм сферичного шару, обмеженого
сферами з радіусами v
і v+dv:
=![]() .
.
|
![]()
Враховуючи вигляд , одержимо
![]() (13)
(13)
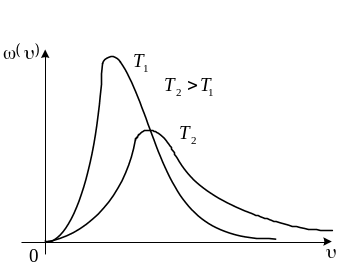
Формула (13) – розподіл Максвела для модуля швидкості.
Графічно цей розподіл виглядає так:
|
Вона
знаходиться з умови
![]()
![]() .
.
Із збільшенням
температури максимум розподілу зміщується
в сторону більших швидкостей, а висота
кривої в максимумі зменшується.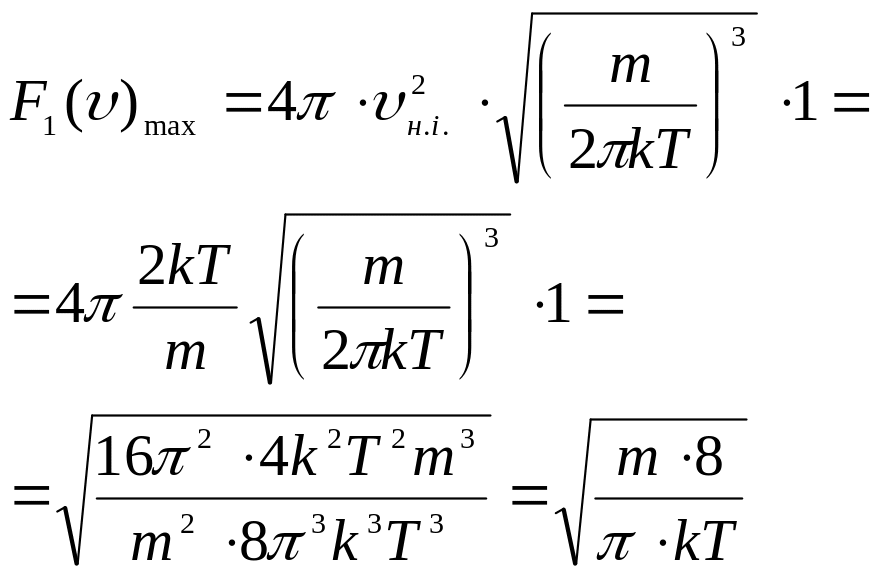
Застосування максвелівського розподілу.
В будь-якій системі, енергія якої рівна сумі енергій окремих частинок (система з адитивною енергією), для розподілу частинок має місце вираз аналогічний максвелівському.
Маючи в своєму розпорядженні функції густини імовірності Максвела можна розв’язувати завдання двох типів.
По-перше, можна знаходити середні значення функцій швидкості частинки.
По-друге, можна знаходити імовірності тих чи інших подій, наприклад, імовірність того, що компонент чи модуль швидкості знаходяться в певних межах.
Зокрема за допомогою розподілу (17) можна обчислити середнє значення самого модуля швидкості:
|
(19) |
Це значення можна порівняти з величиною середньоквадратичної швидкості:
|
(20) |
Хоча
остання величина всього лише на 7% більша,
ніж
![]() ,
ця різниця вказує на ту обставину, що
операція усереднення, взагалі кажучи,
не комутує з іншими операціями, як,
наприклад, піднесення до квадрату.
,
ця різниця вказує на ту обставину, що
операція усереднення, взагалі кажучи,
не комутує з іншими операціями, як,
наприклад, піднесення до квадрату.

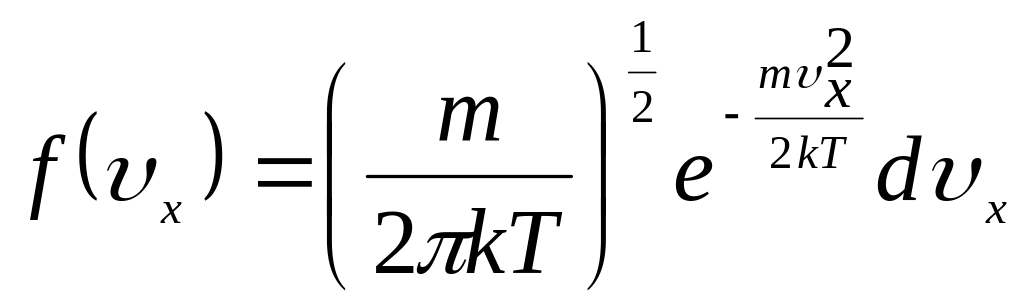 ,
,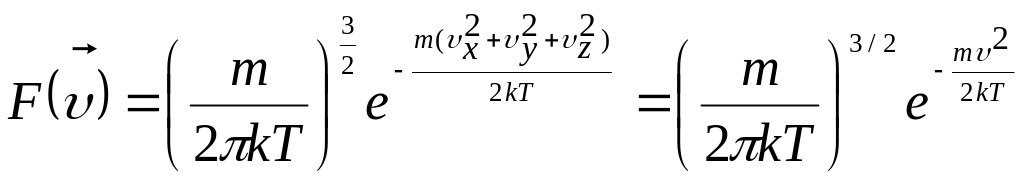 ,
,
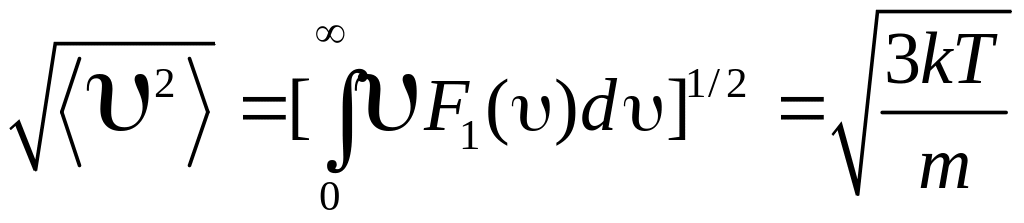 .
.