
- •Принятые сокращения и аббревиатуры
- •Предисловие
- •1− Скоба; 2 − неподвижная плоскость; 3 − подвижная плоскость;
- •4 − Винт; 5 − стебель; 6 − шкала; 7 − гильза; 8 − трещотка; 9 − тормоз
- •1 Определение истинной плотности горной породы
- •2 Определение плотности образцов горных пород
- •3 Определение пористости горных пород
- •4 Определение водопоглощения горных пород
- •1 Определение равновесной влажности древесины
- •3 Определение предела прочности древесины при сжатии вдоль волокон
- •4 Определение предела прочности древесины при статическом изгибе в тангентальном направлении
- •6 Изучение пороков древесины
- •7 Определение породы древесины по внешнему виду
- •Методы испытаний
- •I Определение водопоглощения, открытой пористости и плотности
- •2 Определение пределов прочности кирпича при изгибе и сжатии
- •2.1 Приготовление формовочной массы
- •2.2 Формование изделий
- •3 Кирпич с 21 пустотами (пустотность 34 %, 45 %)
- •1 − Смеситель. 2 − лопасти. 3 − уплотняющие винты. 4 − решетка с ножами. 5 − вакуум-камера. 6 − вал.
- •7 − Корпус (цилиндр) пресса. 5 − переходная головка. 9 − мундштук
- •4 Обжиг изделий
- •1 Определение нормальной густоты и текучести гипсового теста
- •2 Определение сроков схватывания
- •3 Определение тонкости помола
- •4 Изготовление образцов-балочек
- •5 Определение марки гипсового вяжущего вещества по прочности
- •2 Определение скорости гашения извести
- •1 Определение тонкости помола цемента
- •2 Определение нормальной густоты цементного теста
- •1 − Станина; 2 − набор сит; 3 − стойки; 4 − упор для вращения сит;
- •5 − Электродвигатель; 6 − шатунно-эксцентриковый механизм
- •3 Изготовление образцов-балочек из цементно-песчаной растворной смеси
- •1 − Станина; 2 − смесительная чаша; 3 − откидная траверса;
- •4 − Валик для перемешивания раствора.
- •4 Хранение образцов до испытания
- •5 Определение прочности образцов
- •1 Гидрофобизация цемента
- •2 Оценка влияния пластифицирующей добавки на свойства гипсового теста
- •3 Оценка влияния пав на сроки схватывания гипса
- •1 Определение насыпной плотности песка и подсчет его пустотности
- •2 Определение зернового состава и модуля крупности песка
- •3 Определение удельной поверхности песка
- •4 Определение водопотребности песка
- •1 Определение насыпной плотности щебня и подсчет его пустотности
- •2 Определение зернового состава и наибольшей крупности щебня
- •3 Определение дробимости щебня
- •4 Определение водопотребности щебня
- •2 Определение ц/в
- •3 Определение расхода воды
- •4 Определение расчетного расхода цемента
- •6 Определение абсолютного объёма заполнителей
- •7 Определение доли песка в смеси заполнителей
- •1 Корректирование состава бетона при расчетном в/ц для обеспечения заданной консистенции бетонной смеси
- •1.1 Приготовление бетонной смеси
- •1.2 Определение подвижности бетонной смеси
- •1.3 Определение жесткости бетонной смеси
- •1.4 Корректирование состава бетонной смеси
- •2 Определение коэффициента уплотнения бетонной смеси
- •3 Изготовление контрольных образцов-кубов
- •1 Определение предела прочности бетона при сжатии
- •2 Нахождение оптимального в/ц
- •2 Изготовление образцов полимерного бетона
- •3 Проведение сравнительных испытаний образцов
- •1 Приготовление бетонной смеси
- •2 Определение плотности бетонной смеси
- •3 Определение средней плотности отформованной смеси
- •4 Определение пористости газобетонной смеси
- •5 Определение пористости и прочности газобетона
- •1 Определение подвижности растворной смеси
- •2 Определение плотности растворной смеси
- •3 Определение расслаиваемости растворной смеси
- •4 Определение водоудерживающей способности
- •5 Определение средней плотности раствора
- •6 Определение марки строительного раствора
- •7 Приготовление штукатурных растворов
- •1 Определение глубины проникания иглы и расчет вязкости битума
- •2 Определение растяжимости битума
- •3 Определение температуры размягчения битума
- •1 Изучение свойств стали
- •2 Определение твердости
- •1 Определение марки строительной стали
- •2 Определение ударной вязкости
- •1. Определение марки строительной стали
- •1 Метод определения времени и степени высыхания.
- •2 Определение массовой доли летучих и нелетучих веществ
- •3 Определение условной вязкости лакокрасочных материалов
- •3.1 Определение условной вязкости по вискозиметру типа в3-246
- •3.2 Определение условной вязкости по шариковому вискозиметру
- •4 Определение адгезии методом решетчатых надрезов
- •5 Определение укрывистости
- •6 Определение эластичности пленки при изгибе
- •1…12 – Стержни; 13 – панель; 14 – струбцина
- •I часть. Группы древесных пород
- •II часть. Древесные породы
- •Глоссарий
- •Черепок – изделие, получаемое после обжига.
3 Определение температуры размягчения битума
Определение температуры размягчения производят на приборе 'Кольцо и шар", состоящего из металлического штатива 1 с тремя пластинками 5 и стакана 6 (рисунок 46). Расстояние между нижней и средней пластинками равно 25,4 мм. В средней пластинке имеются два отверстия диаметром около 19 мм для установки в них колец 2, залитых испытуемым битумом.
Кольца с битумом помещают в отверстие на пластинке прибора. В среднее отверстие пластинки вставляется термометр 4 так, чтобы нижняя точка ртутного резервуара термометра была на одном уровне с нижней поверхностью битума в кольцах.
Если температура размягчения битума ниже 80 C, штатив с кольцами ставят на 5 мин в стакан, наполненный водой, имеющей температуру 4,5...5,5 C.
Если температура размягчения битума выше 80 C, то образец выдерживают в течение 15 мин в глицерине при температуре 35±0,5 C.
По истечении 15 мин штатив вынимают из стакана, на каждое кольцо в центре поверхности битума кладут стальной шарик 3 диаметром 9,5 мм (рисунок 47а) и опускают штатив обратно в стакан.
Стакан устанавливают на нагревательный прибор так, чтобы плоскость колец была строго горизонтальной. Температура воды или глицерина в стакане после первых трех минут нагрева должна подниматься со скоростью 5±0,5 C в минуту.
За температуру размягчения битума принимают температуру, при которой выдавливаемая шариком капля битума коснется нижней пластинки прибopa (рисунок 47б).
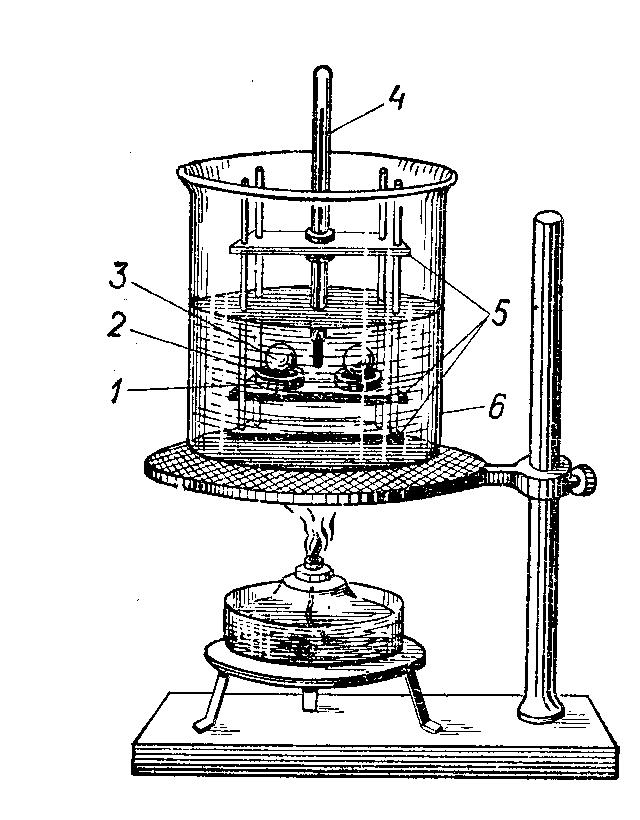
Рисунок 46 – Прибор «Кольцо и шар»
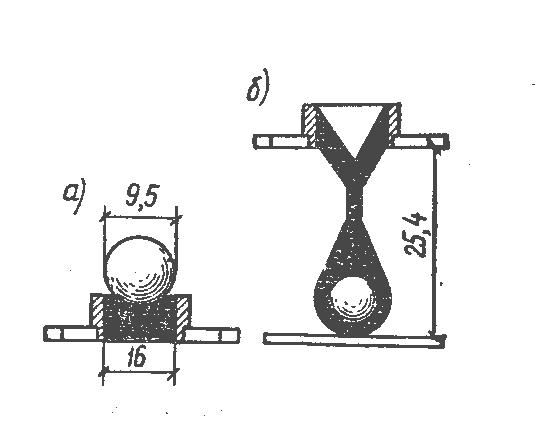
Рисунок 47 – Положение шара в приборе «Кольцо и шар»
Расхождение между двумя параллельными определениями не должно превышать 0,5 C.
По результатам опытов в отчете следует дать аргументированные объяснения выявленным закономерностям с позиции теории дисперсной структуры битума и указать границы температурных интервалов различных его состояний; а также установить марку исследуемого битума. Составить характеристики кровельных материалов, обосновать их свойства и назначение.
4 Определение водонепроницаемости рулонных кровельных материалов
Водонепроницаемость рулонных кровельных материалов определяют на трех образцах размером 130х130 мм. Для испытания применяют прибор, изображенный на рисунке 48. Каждый образец в отдельности помещают между резиновыми прокладками. Поднимают сосуд до тех пор, пока расстояние между верхним уровнем воды в сосуде и нижней поверхностью образца, отмеченной на линейке, станет равным по высоте водяного столба, предусмотренной стандартом на испытываемый материал. При этом на внешней поверхности образца не должно появиться признаков проникания воды.
Поверх образца для предохранения его от деформации надо укладывать металлическую сетку с крупными отверстиями.
Определять водонепроницаемость можно также по времени, через которое образец пропускает воду при постоянном гидростатическом давлении, и по гидростатическом давлению, выдерживаемому образцом в течение определенного промежутка времени.
Водонепроницаемость пергамина можно определять и упрощенным методом. Образец материала размером 300х300 мм осторожно сгибают, придавая ему форму коробки с площадью основания 100х100 мм и высотой 100 мм. Изготовленную коробку помещают на металлический или фанерный лист, сверху которого наложена фильтровальная бумага, пропитанная раствором лакмуса или метилового красного.
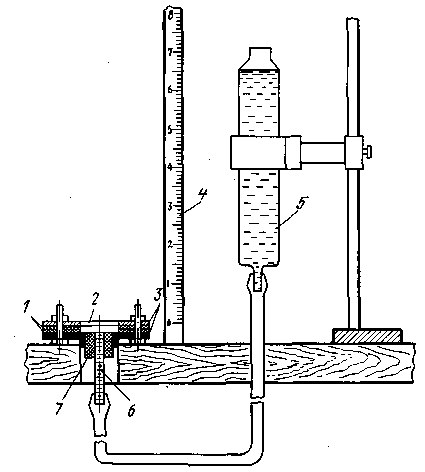
Рисунок 48 – Прибор для определения водонепроницаемости
рулонных кровельных материалов:
1 – резиновые прокладки; 2 – образец; 3 – фланец; 4 – градуированная линейка;
5 – стеклянный сосуд; 6 – стеклянная трубка; 7 – резиновая пробка
В коробку на высоту 50 мм наливают воду, температура которой 20±2 оС, подкисленную соляной или серной кислотой, и выдерживают ее столько времени, пока цвет индикаторной бумаги не начнет изменяться под действием воды, просочившейся через испытываемый материал. В процессе испытания поддерживают постоянный уровень воды в коробке, доливая ее, если она испаряется.
Время в сутках от начала испытаний до изменения цвета индикаторной бумаги считают характеристикой водонепроницаемости.
Контрольные вопросы
1 К какой группе строительных материалов относят нефтяные битумы?
1 К лакокрасочным материалам.
2 К органическим вяжущим.
3 К неорганическим вяжущим.
4 К строительным растворам.
2Укажите положительные свойства битума.
1 Невысокая температура размягчения.
2 Гидрофобность и водонепроницаемость.
3 Хрупкость при динамических нагрузках.
4 Малая адгезия к каменным материалам.
3Каковы основные группы углеводородов в составе нефтяных битумов?
1 Масла, смолы и асфальтены.
2 Бензин, лигроин и парафин.
3 Бензол, фенол и их производные.
4 Мицеллы и коллоидные частицы.
4 Что представляют собой битумы по структуре при нормальной температуре?
1 Жидкости с высокой вязкостью.
2 Стеклокристаллические тела, характеризующиеся температурным интервалом размягчения.
3 Кристаллические тела с низкой температурой плавления.
4 Коллоидные дисперсные системы.
5 Какие основные показатели лежат в основе классификации битумов по маркам?
1 Пределы прочности при сжатии и растяжении.
2 Средняя плотность и прочность сцепления с поверхностью каменного образца.
3 Вязкость, растяжимость и температура размягчения.
4 Степень водостойкости и водонепроницаемости.
6 Укажите стандартные условия испытания образцов битума на пенетрометре
1 Температура, 25 C, время погружении иглы 5 с под действием груза массой 100 г.
2 Температура 20 C; время погружения иглы 10 с под действием груза массой 100 г.
3 Температура 25 C, время погружения иглы 30 с под действием груза массой 200 г
4 Температура 20 C, гремя погружения иглы 1 с под действием груза массой 50 г.
7 Какой критерий используют для характеристики растяжимости битума в дуктилометре?
1 Время деформации в минутах до момента разрыва образца.
2 Величину деформации в сантиметрах, отмеченную в момент разрыва битумного образца.
3 Величину деформации в сантиметрах, снятую через 5 с после начала деформации образца.
4 Максимальное напряжение в МПа, отмеченное при испытании.
8 Что принимают за температуру размягчения битума при его испытании на приборе "Кольцо и шар"?
1 Температуру, при которой шарик начинает выдавливать битум через кольцо.
2 Температуру, при которой шарик погрузится в кольцо, заполненное битумом.
3 Температуру, при которой шарик начинает выходить из кольца с битумом.
4 Температуру, при которой битум с шариком коснется нижней пластинки прибора.
9 Как можно повысить термостойкость битума?
1 Ввести в битум тонкоизмельченный минеральный порошок.
2 Добавить в битум сырую нефть.
3 Ввести в состав битума органический растворитель.
4 Приготовить на основе битума эмульсии.
10 Чем отличается пергамин от рубероида?
1 Пергамин получают на основа дегтевых вяжущих, а рубероид – на основе битумных.
2 Пергамин не имеет покрытия основы тугоплавкими битумами с обеих сторон.
3 Пергамин – гидроизоляционный материал, а рубероид – кровельный.
4 Пергамин – безосновный материала, а рубероид – основный.
Лабораторная работа № 18
ЧЕРНЫЕ МЕТАЛЛЫ
Общие сведения
Металлы – вещества, обладающие металлическим блеском, пластичностью, высокой прочностью, электро- и теплопроводностью, ковкостью и свариваемостью.
Атомы в твердых телах стремятся к такому расположению в пространстве, чтобы энергия их взаимодействия была минимальной. Этому способствует определенный порядок в пространственном размещении частиц, определяемый понятием кристаллическая решетка. Важнейшей особенностью кристаллического состояния является упорядоченное расположение частиц вещества. Если вписать кристаллическую решетку в систему координат, то по расстоянию между ближайшими частицами в кристалле и углам между осями координат можно рассчитать взаимное расположение частиц в твердом теле. Для изучения кристаллического строения можно выделить элемент объема из минимального количества частиц (атомов), многократным переносом (трансляцией) которого в пространстве можно построить весь кристалл.
Такой элементарный объем, который характеризует особенности строения данного типа кристалла, называется элементарной ячейкой. (рисунок 49).

Рисунок 49 − Основные виды элементарных ячеек кристаллических решеток металлов
а) объемно-центрированная кубическая кристаллическая ячейка;
б) гранецентрированная кубическая кристаллическая ячейка;
в) гексагональная кристаллическая ячейка
Наиболее распространенные кристаллические решетки:
− объемно центрированный куб (ОЦК);
− гранецентрированный куб (ГЦК);
− гексагональная плотноупакованная кристаллическая решетка (ГПУ) и неплотно упакованная кристаллическая решетка.
Менее распространены ромбоэдрическая, тетрагональная и более сложные кристаллические решетки.
Кристаллические решетки характеризуются следующими основными параметрами (таблица 54):
− период решетки – расстояние между центрами двух соседних частиц (атомов, ионов) в элементарной ячейке решетки (а, в, с) – межплоскостное расстояние а, которое выражается в ангстремах (1Å = 10-8 см);
− атомный радиус – половина межатомного расстояния между центрами ближайших атомов в решетке при нормальной температуре и атмосферном давлении. Он не является постоянной величиной и зависит от ряда факторов, важнейшими из которых являются координационное число и тип химической связи между атомами в кристалле;
− энергия кристаллической решетки – энергия, выделяющаяся при образовании кристаллов из ионов, атомов или других частиц, образующих кристалл, когда исходное состояние этих частиц газообразное. От ее величины зависят температура плавления, модуль упругости, прочность, твердость. Увеличение валентности атомов приводит к увеличению энергии решетки;
− координационное число К (плотность) – количество атомов, находящихся на наиболее близком и равном расстоянии от любого выбранного атома в решетке;
− базис решетки – количество атомов, приходящихся на одну элементарную ячейку решетки.
Таблица 54 – Характеристики кристаллической решетки
Тип кристаллической решетки |
Обозначение |
К |
Базис |
Кубическая простая |
К |
8 |
1 |
Объемно центрированный куб |
ОЦК |
8 |
2 |
Гранецентрированный куб |
ГЦК |
12 |
4 |
Гексагональная плотноупакованная |
ГПУ |
12 |
4 |
Плотность упаковки атомов в разных плоскостях и по разным направлениям в кристалле разная. Поэтому и свойства кристаллического тела в разных направлениях разные – анизотропия.
Частицы вещества в кристаллической решетке удерживаются за счет электрических связей:
− ионная связь – кристаллы состоят из разноименно заряженных ионов (Na, Cl). Такие кристаллы отличаются хрупкостью;
− ковалентная связь (атомные кристаллы) – обобществление валентных электронов соседних атомов (алмаз; карбиды Fe3C, SiC; нитриды). Свойства тел с такой связью могут сильно различаться. Как правило, они имеют малую плотность, обладают высокой хрупкостью, иногда высокой твердостью;
− полярная связь (молекулярные кристаллы). Такой связью обладают водород, азот, углекислота, вода в твердом закристаллизованном состоянии;
− металлическая связь. Кристаллы с такой связью имеют высокую прочность, металлический блеск, высокие показатели электро- и теплопроводности.
Кристаллизация протекает в результате переохлаждения расплава, температура которого зависит от скорости охлаждения. Размер кристаллов также зависит от степени переохлаждения расплава.
Для металлов характерна перекристаллизация в твердом состоянии − полиморфизм. Это явление имеет большое практическое значение: благодаря полиморфизму железа возможно широкое изменение свойств стали посредством термической обработки (закалки, отжига).
Условия кристаллизации влияют на правильность геометрических форм кристаллов. Реальные кристаллы не имеют правильного, идеального регулярного расположения атомов в решетке. В них встречаются дефекты – различные несовершенства.
В зависимости от размеров, формы и пространственного расположения различают следующие дефекты.
Объемные дефекты, имеющие значительную протяженность во всех направлениях (усадочные; газовые раковины; трещины, образовавшиеся на различных стадиях технологии слитков, отливок или при дальнейшей обработке).
Поверхностные дефекты – нарушение порядка расположения атомов в местах стыка сросшихся при кристаллизации зерен. Нарушение порядка в пограничных зонах зерен обычно усугубляется скоплением в этих участках различного рода посторонних включений (шлак и др.). Однако и внутри зерна никогда не наблюдается идеальное строение кристаллической решетки. Установлено, что каждое зерно состоит из отдельных элементов-блоков, размер которых колеблется в пределах 10-3…10-5 см. Отдельные блоки повернуты друг относительно друга на углы порядка нескольких минут. Более крупные образования из нескольких блоков образуют субзерна (фрагменты) – повернуты на несколько градусов. К поверхностным дефектам относятся также и дефекты упаковки.
Точечные дефекты, когда отдельные узлы решетки могут быть не заняты атомами (вакансии), отдельные атомы могут оказаться в межузлиях (дислоцированный атом) или наблюдается появление атомов внедрения или замещения (примесные атомы).
Линейные дефекты (дислокации) – смещение рядов атомов по отношению к их правильному расположению в кристаллической решетке. Разновидностями линейных дислокаций (рисунок 50) являются краевые, винтовые (рисунок 51) и смешанные дислокации.
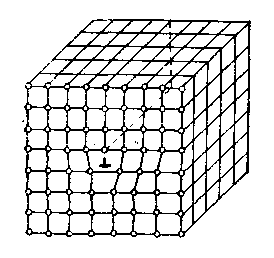
Рисунок 50 − Линейная дислокация в кристаллической решетке
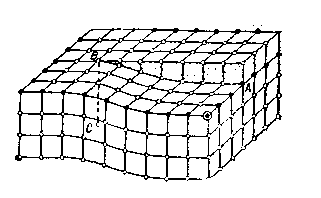
Рисунок 51 − Винтовая дислокация в кристаллической решетке
В чистом виде металлы не применяются в строительной технике. основными недостатками чистых металлов является большая деформативность и пластичность. В соединениях с другими элементами металлы способны образовывать сплавы.
Сплавы – металлические вещества с характерными свойствами металлов, получаемые при затвердевании жидких расплавов. Помимо сплавления сплавы можно получить спеканием, электролизом и др.
В отличие от чистых металлов сплавы обладают более широким диапазоном свойств, и именно они применяются в промышленности. Сплав образуется из соответствующих компонентов, в качестве которых могут применяться чистые элементы и устойчивые химические соединения. При кристаллизации сплавов могут образовываться следующие основные твердые фазы: твердые растворы, химические соединения, механические смеси.
Процесс кристаллизации металла из расплава легко представить на диаграмме состояния однокомпонентной системы, которая имеет одну критическую точку – температуру кристаллизации.
При кристаллизации расплава наблюдается как минимум две критические точки (температуры начала и окончания кристаллизации). Это можно рассмотреть на диаграмме состояния двухкомпонентной системы. Линии ликвидуса и солидуса.
Сплавы в зависимости от состава, условий образования могут быть в различных состояниях (твердые растворы, химические соединения, механические смеси).
Твердые растворы. Наиболее распространенная фаза в металлических сплавах. Особенность строения – наличие в их кристаллической решетке разнородных атомов при сохранении типа кристаллической решетки растворителя. По характеру распределения атомов растворенного вещества в кристаллической решетке растворителя различают 2 типа твердых растворов: растворы замещения и растворы внедрения.
Химические соединения. Они образуются в результате химического взаимодействия компонентов, при этом атомы располагаются в строгом порядке и количественном соотношении. Например, в сплавах железа образуется карбид железа (цементит) Fe3C. Как правило, это твердые, прочные, но хрупкие вещества. Наличие их в сплаве ведет к его упрочнению с одновременным понижением пластичности и ударной вязкости.
Химические соединения металлов делятся на две группы.
1 группа − соединения с нормальной валентностью, которые дают металлы с типичными неметаллами (О, S, Cl). Такими соединениями являются оксиды, сульфиды, хлориды. В сплавах такие соединения находятся в виде так называемых неметаллических включений.
2 группа – металлические соединения. Наиболее важные из них – фазы внедрения и электронные соединения. Отличаются разнообразием типов межатомных связей (металлической, ковалентной, ионной) с преобладанием металлической связи.
Механические смеси. Они образуются путем срастания кристаллов между собой при раздельной кристаллизации компонентов. Каждый из компонентов сохраняет свои специфические свойства. Структура сплава состоит из кристаллов веществ А и В, связь между которыми осуществляется по границам зерен. Свойства сплавов − средние значения.
Железо – серебристо-белый металл. В технически чистом железе примесей 0,10…0,15 %. Свойства зависят от степени его чистоты. Для технически чистого железа tпл = 1539 оС. Твердость невысокая НВ = 80. Железо обладает хорошей пластичностью.
Сталь представляет собой сплав железа и углерода С с количеством углерода до 2,14 %. Сталь обладает пластичностью и упругостью. В зависимости от содержания углерода различают стали следующих видов.
Углеродистая сталь. Содержит только нормальные примеси (Si, Mn, P, S, O):
− низкоуглеродистая сталь содержит углерода менее 0,3 %. Она обладает высокой пластичностью и идет на изделия, изготовляемые штамповкой;
− среднеуглеродистая сталь содержит углерода от 0,30 до 0,65 %. Кроме пластичности она обладает твердостью и прочностью. Из нее в основном изготовляют прокатные изделия;
− высокоуглеродистая (инструментальная) сталь содержит углерода от 0,65 до 1,50 %. Она обладает высокой твердостью, но является весьма хрупкой и идет на изготовление инструментов.
Легированная сталь кроме нормальных примесей содержит и другие добавки (Ni, Cr, W, V, Mo, Ni, Fl и др.). Количество добавок изменяется в больших пределах (2…10 %). К ним относятся и нержавеющие стали, которые содержат легированных добавок более 10 %.
Процесс получения стали связан с уменьшением количества углерода и примесей в чугуне путем окисления кислородом воздуха или кислородом, содержащимся в железной руде, до таких соединений, которые могут быть переведены в шлак или удалены из чугуна в газообразном состоянии.
Окисление примесей происходит при участии закиси железа по схемам
2Fe + O2 = 2FeO.
C + FeO = CO + Fe.
Mn + FeO = MnO + Fe.
Si + 2FeO = SiO2 + 2Fe.
2P + 5FeO = P2O5 + 5Fe.
Наличие извести в шлаке способствует удалению серы:
FeS + CaO = CaS+FeO.
В конце процесса окисления сталь содержит большое количество закиси железа, которая вредна, так как повышается хрупкость. Чтобы избавиться от нее, необходимо после окисления провести раскисление. Для этого применяют ферросплавы, а также алюминий.
Mn + FeO = MnO + Fe.
Si + 2FeO = SiO2 + 2Fe.
2Al + 3FeO = Al2O3 + 3Fe.
Образовавшиеся оксиды всплывают и удаляются вместе со шлаком.
В зависимости от полноты проведения процесса раскисления жидкого металла различают:
− спокойную сталь, получающуюся при полном раскислении и застывании металла без выделения газа; такая сталь в слитке имеет плотное и однородное строение;
− кипящую сталь, получающуюся при неполном раскислении. В этом случае в процессе застывания закись железа продолжает реагировать с углеродом металла, выделяя оксид углерода в виде пузырьков. Этот процесс продолжается до выделения большей части газа; часть его еще остается в металле и при охлаждении образует газовые пузыри. При этом образуются зоны ликвации, которые характерны неравномерным распределением вредных примесей, что приводит к снижению качества стали. Достоинства кипящей стали – хорошая свариваемость, улучшение процесса обработки и более низкая стоимость.
− полуспокойная сталь занимает промежуточное положение между спокойной и кипящей сталями.
Цель работы
Изучить основные свойства сталей и определить ее твердость.
Порядок выполнения работы
Для решения поставленной задачи каждое звено студентов изучает различные типы сталей, определяет их пригодность в строительной технике и твердость различными способами.
МЕТОДЫ ИСПЫТАНИЙ
