
- •1. Вступ
- •1.1. Предмет і мета дисципліни "Фізична хімія"
- •1.4. Тематичний план та зміст лекційного курсу 6 тетраместру
- •1.5. Індивідуальні та домашні завдання для самостійної роботи студентів
- •2. Розрахункові завдання
- •2.1. Основні поняття хімічної термодинаміки
- •2.1.1. Основні визначення
- •2.1.2. Перший закон термодинаміки
- •2.1.3. Закон Геса
- •2.1.4. Теплоємність
- •2.1.5. Закон Кірхгофа
- •2.1.6. Другий закон термодинаміки
- •2.1.7. Постулат Планка
- •2.1.8. Термодинамічні потенціали
- •2.1.9. Рівняння Гібса-Гельмгольца
- •2.1.10. Хімічний потенціал.
- •2.1.11. Хімічна рівновага. Стандартна і емпіричні константи рівноваги.
- •2.1.12. Рівняння ізотерми хімічної реакції Вант-Гофа
- •2.1.13. Рівняння ізобари і ізохори хімічної реакції. Вплив температури, тиску і домішок інертних газів на рівновагу реакції.
- •2.1.14. Обчислення констант рівноваги із стандартних величин термодинамічних функцій за рівнянням Тьомкіна – Шварцмана.
- •2.2. Приклади розв'язання задач
- •2. При адіабатичному стисненні робота розраховується наступним чином:
- •Використовуючи отримане значення т2 визначаємо роботу адіабатичного стиснення
- •Визначаємо зміну ентропії для реакції при стандартних умовах (величини ентропій вихідних речовин та продуктів реакції відповідно даних з довідника):
- •Рівноважна 3-3/4·х 1-1/4·х х Константа рівноваги має такий вираз
- •Прореагувало і утворилося 3х х 4х
- •Тоді, константа рівноваги Кn складає:
- •Якщо тепловий ефект δн не залежить від температури, тоді тепловий ефект хімічної реакції визначаємо за наближеною формою рівняння ізобари:
- •2.3. Багатоваріантні задачі
- •3. Индивідуальне розрахунково-графічне завдання
- •3.1. Пояснення для вирішення завдання
- •3.1.1. Розрахунок константи рівноваги хімічної реакції
- •3.1.2 Розрахунки виходу продуктів реакції
- •3.1.3. Розрахунок залежності виходу аміаку від тиску та температури
- •3.1.4. Розрахунки рівноваги в реальних системах
- •3.2. Багатоваріантне графічно-розрахункове завдання
- •4. Перелік контрольних запитань
- •4.1. Перелік запитань для самоконтролю
- •4.2. Питання до екзаменаційних білетів
- •4.2.1. Теплоємність, перше начало термодинаміки, термохімія
- •4.2.2. Друге і третє начало термодинаміки
- •4.2.3. Хімічна рівновага
- •5. Нарахування рейтингових балів
- •5.1. Таблиця відповідності рейтингових балів за національною та європейською шкалами
- •5.2. Правила нарахування рейтингових балів
- •5.3. Таблиця відповідності оцінок та балів за європейською і національною шкалами
- •6. Список рекомендованої літератури Основна література
- •Перелік позначень
3.1.3. Розрахунок залежності виходу аміаку від тиску та температури
Задача: Розрахувати вихід аміаку при наступних значеннях температури та тиску:
Т, К |
298 |
373 |
573 |
773 |
973 |
Р·10-5, Па |
1,0133 |
2 |
5 |
10 |
20 |
Розрахунок:
Синтез аміаку проводиться за реакцією:
-
N2
+
3H2
=
2NH3
Вихідний вміст речовин (t=0)
1
3
-
До моменту встановлення рівноваги прореагувало та утворилось
x
3·x
2·x
Рівноважний вміст
1-x
3(1-x)
2·x
Відповідно рівнянням (3.18) – (3.22) запишемо:
n = 2 - 3 - 1 = -2
= 1 – x + 3 – 3x + 2х = 4 - 2х
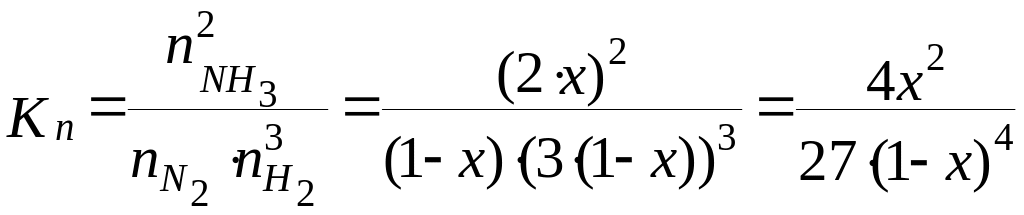
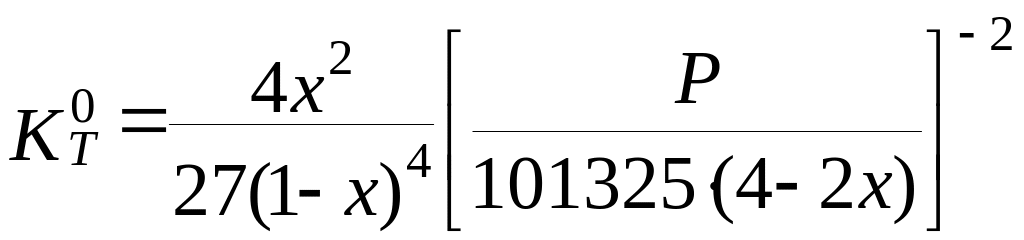 (3.25)
(3.25)
Заносимо в таблицю 3.1.1 вихідні дані та значення ΔΖ, що розраховані за рівнянням реакції.
Таблиця 3.1.1
Речовина |
Ζ |
Стехіо-метричні коефіці-єнти |
|||||
Стандартна
теплота утворення
|
Стандартна
ентропія
|
Коефіцієнти ступеневого ряду, Дж/моль∙К |
|||||
а |
b∙103 |
c∙106 |
c´∙10-5 |
||||
N2 |
0 |
191,5 |
27,88 |
4,27 |
- |
- |
1 |
H2 |
0 |
130,52 |
27,88 |
3,26 |
- |
0,5 |
3 |
NH3 |
-45940 |
192,66 |
29,8 |
25,48 |
- |
-1,67 |
2 |
ΔΖ |
|
|
Δa |
Δb |
Δс |
Δс´ |
|
|
-91879 |
-196,74 |
-49,12 |
37,91 |
- |
-4,84 |
-2 |
За
рівняннями (3.14) – (3.17) розраховують
залежність
та
![]() від температури. Результати розрахунків
заносимо в таблицю 3.1.2.
від температури. Результати розрахунків
заносимо в таблицю 3.1.2.
Таблиця 3.1.2
Т, К |
298 |
373 |
573 |
773 |
973 |
- |
33250 |
18132 |
-24673 |
-69580 |
-115587 |
|
673734 |
346,1 |
5,6∙10-3 |
1,99∙10-5 |
6,2∙10-7 |
За рівнянням (3.25) розраховують долю перетворення x (таблиця 3.1.3).
Таблиця 3.1.3
Доля перетворення реакції синтезу аміаку
-
Р*10-5, Па
Т, К
298
373
573
773
973
1,0133
0,969
0,800
0,46
0,023
0,00552
2
0,979
0,857
0,84
0,062
0,0103
5
0,986
0,909
0,177
0,13
0,025
10
0,989
0,935
0,285
0,28
0,0499
20
0,993
0,954
0,415
0,52
0,1
Вихід продуктів реакції прийнято виражати в мольних процентах, % xі:
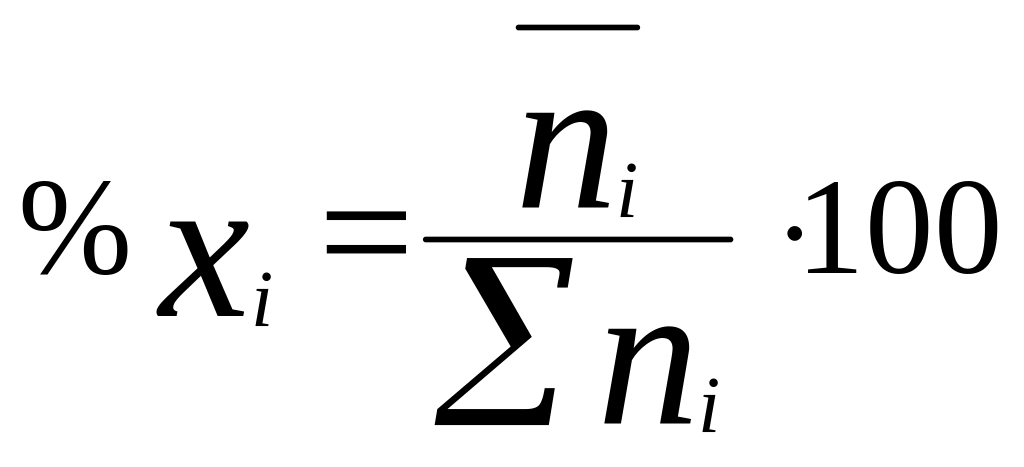
Так наприклад для аміаку
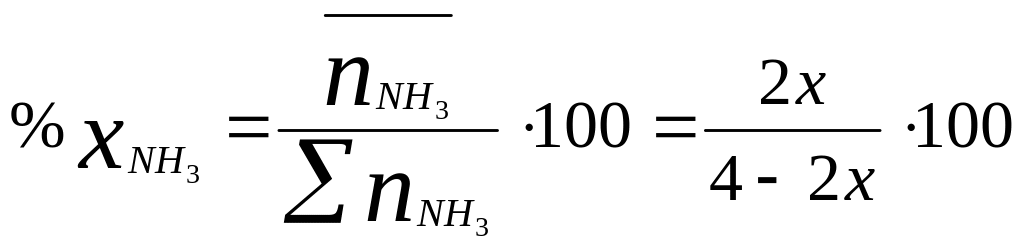
при Т = 298 К та Р = 1,0133∙105 Па доля перетворення складає х = 0,969, а вихід аміаку відповідно:
![]()
