
- •Научные основы современных сталеплавильных процессов
- •Посвящается в.И. Явойскому
- •Глава 1
- •Глава 2
- •2.1 Кинетика гетерогенных высокотемпературных процессов и методы выявления их ведущего звена
- •2.2 Исследование процессов окислительного рафинирования имеющих место в производстве стали
- •2.3 Условия протекания окислительного рафинирования в сталеплавильных агрегатах
- •2.4 Реакция окисления углерода
- •Внутридиффузионный режим лимитирования процесса
- •2.7 Окислительные процессы в многокомпонентных расплавах на основе железа
- •2.10 Окисление серы
- •2.11 Деванадация
- •2.13 Современные представления о ходе процессов окислительного рафинирования расплавов на основе железа
- •Окислительное рафинирование в условиях современных сталеплавильных агрегатов
- •2.15 Характеристика и газодинамика кислородных струй сталеплавильных агрегатов
- •Форма и геометрические размеры реакционной зоны
- •Глава 3.
- •3.1 Общие положения
- •3.2 Маcсоперенос примеси в экстрагирующей фазе
- •3.3 Сера в металле и его десульфурация
- •3.4 Кинетика процесса десульфурации металла
- •3.5 Кинетика десульфурации металла за счет твердых тел (порошкообразными десульфураторами)
- •Глава 4. Раскисление стали и неметаллические включения.
- •4.1 Кислород в стали и ее раскисление
- •4.2 Термодинамика раскисления
- •4.3 Кинетика осадочного раскисления
- •4.4 Плавление и растворение в металле вводимых раскислителей
- •4.5 Взаимодействие растворенного в металле кислорода с введенным в него раскислителем
- •4.6 Образование зародышей новой фазы продуктов раскисления в объеме жидкого металла
- •4.7 Рост образовавшихся продуктов раскисления
- •4.8 Удаление продуктов раскисления из сферы протекания этой реакции
- •4.9 Переход включений из металла в шлак или другие контактирующие фазы
- •4.10 Неметаллические включения в готовом металле
- •Глава 5 газы в стали
- •5.1 Взаимодействие азота и водорода с расплавленным и охлаждающимися сплавами железа
- •5.2 Термодинамика взаимодействия азота с расплавами на основе железа
- •5.3 Методы изучения взаимодействия азота с металлами
- •5.4 Кинетика растворения азота в железе и его сплавах
- •Глава 6 поведение водорода в сплавах на основе железа
- •6.1 Некоторые особенности взаимодействия водорода
- •Со сплавами на основе железа
- •6.2 Природа газообразного водорода и взаимодействие его с металлами
- •6.3 Термодинамика сорбирования водорода расплавленными и твердыми сплавами железа
- •6.4 Кинетика растворения и выделения водорода из расплавов на основе железа
- •6.5 Состояние водорода в готовой стали его влияние на механические свойства стали и распределение водорода в металле
- •6.6 Поведение водорода при выплавке металла и при его внепечной обработке
- •Глава 7 основы обработки стали в ковше
- •7.1 "Внеагрегатная" или "ковшевая" обработка стали
- •7.2 Вакуумирование металла
- •7.3 Применение инертных газов
- •Заключение
- •Библиографический список
- •Оглавление
- •Научные основы современных сталеплавильных процессов
Глава 5 газы в стали
5.1 Взаимодействие азота и водорода с расплавленным и охлаждающимися сплавами железа
Еще в начале ХХ-го века металлургам было известно о существенном влиянии растворенных в стали (в процессе ее выплавки) водорода и азота на эксплуатационные свойства металла, а иногда и на образование в нем тех или иных пороков. В то время дегазация стали рассматривалась как практически неразрешимая проблема и рекомендации сводились лишь к предотвращению, или, по крайней мере, понижению перехода газов в металл в процессе плавки.
В настоящее время во всех технически развитых странах наиболее ответственная, легированная сталь перед разливкой подвергается вакуумированию. Широко применяются также различные микролегирующие и модифицирующие элементы, ослабляющие или даже устраняющие вредное влияние газов на готовый металл. Определенное распространение приобрели и дегазирующие переплавы: вакуумно-дуговой, электронно-лучевой и др. Для выплавки сталей, высокочувствительных к присутствию газов, применяются особые методы плавки, например, такие как вакуумно-индукционная, плазменная и др.
Широкое развитие получили специальные методы термической обработки стали, обеспечивающие ее дегазацию, или, по крайней мере, устранение таких пороков, как "флокены". Все это создало условия для обеспечения в заводской практике той или иной, необходимой для данной марки стали, степени ее дегазации и остаточных концентраций [H] или [N]. В отдельных случаях для достижения тех или иных заданных свойств сталей определенных назначений некоторое распространение получило управляемое и строго лимитированное повышение в металле концентраций азота, а иногда даже и водорода.
В связи с вышеизложенным, в настоящее время чрезвычайно актуальной стала проблема взаимодействия газов и стали, решению которой посвящена обширная литература. Ряд обстоятельных, выполненных на высоком научном уровне работ [158…160, 162], посвящен вопросам теории взаимодействия газов и расплавленного металла: природе процесса растворения, поведению растворенных газов в процессе охлаждения металла, природе и механизму влияния газов на служебные свойства металла и на образование в нем тех или иных пороков. Поэтому мы, не претендуя на полноту изложения проблемы и учитывая ограниченность объема монографии, лишь кратко изложим физико-химические основы взаимодействия расплавов на основе железа и некоторые из результатов собственных исследований.
5.2 Термодинамика взаимодействия азота с расплавами на основе железа
Атмосферный азот представляет собой постоянную по составу смесь двух устойчивых его изотопов N14, составляющий в нем 99,62 % и N15 – соответственно 0,38 %. Благодаря особенностям строения электронных оболочек, соседние атомы азота попарно объединяются с образованием прочных ковалентных связей 2р-орбит, сопровождающимся выделением огромной энергии (940,81 Дж/моль). Степень диссоциации молекул азота- "", определяется уравнением:
Кр=(42/1–2)Р, (139)
где Кр – константа равновесия процесса диссоциации молекул азота;
Р – давление.
Она весьма невелика при температурах выплавки стали, включая даже дуговую и плазменную плавку. Поэтому металл фактически контактирует и взаимодействует с молекулярным азотом.
При нормальных условиях и при всех температурах, могущих интересовать металлургов, молекулярный азот химически мало активен и равновесное распределение его между газообразной фазой и жидким металлом всегда достигается очень нелегко – после длительных выдержек.
Как это впервые было доказано Сивертсом, в равновесных условиях концентрация азота в расплавленных железе и сплавах на его основе и в твердом металле связана с его парциальным давлением уравнением "квадратного корня".
[N]=KN![]() , (140)
, (140)
где KN – константа равновесия растворения азота, зависящая для сплава данного состава от температуры;
![]() – парциальное давление молекулярного
азота.
– парциальное давление молекулярного
азота.
Такая зависимость растворимости азота от давления позволяет считать, что азот растворяется во всех металлах, к которым применим "закон квадратного корня", в атомарном состоянии или в форме нитридов, характерной особенностью которых является существование лишь одного атома азота в каждой молекуле нитрида. Итак, растворение азота в металлах и сплавах представляет собой сложный процесс
I этап N2=2Nадс, Ндис+Надс
II этап 2Nадс=2[N] или, при образовании нитрида ме
талла 2Nадс+2n[Me]=2[MenN], Hраст
В связи с большой прочностью молекул азота, их диссоциация и адсорбирование на поверхности металла при каждой данной температуре определяется только природой самого металла и его "сродством" к азоту. Общий тепловой эффект обоих этапов процесса растворения азота (HS) для большинства сплавов железа и для многих, даже нитридообразующих, металлов отрицателен вследствие огромной энергии образования двухатомных молекул N2.
Он определяется в соответствии с уравнением Вант-Гоффа, которое в случае растворения двухатомного газа принимает форму:
dlnSN/dT=HS/2RT2, (141)
где SN
– растворимость азота при
![]() =0,1
Мпа;
=0,1
Мпа;
HS – суммарное изменение энтальпии системы при растворении молекулярного азота в металле, т.е.
HS=Ндис+Надс +Hраст
В зависимости от природы и строения растворяющего азот металла, HS может быть как положительной, так и отрицательной (когда Надс+Hраст очень значительны). В связи с этим растворимость азота, например, в расплавленном железе (при HS>0) увеличивается с повышением температуры. В других металлах, образующих прочные нитриды, например Са или Li (HS<0), растворимость азота понижается при понижении температуры.
Природа процесса растворения азота в расплавленных и твердых металлах полностью еще не выяснена. В большинстве случаев считают, что, подобно таким элементам как водород, кислород и углерод, азот склонен к образованию в металлах фаз внедрения. Особенно много общего следует ожидать в поведении азота и углерода: они являются соседями по таблице Д.И. Менделеева, обладают близкими атомными весами, размерами атомов и сходными структурами электронных оболочек. В связи с этим, геометрическое соответствие позволяет предполагать, что азот, как и углерод, растворяются в виде катионов с сохранением при этом наружной электронной оболочки 2s2. Расположение многозарядных катионов N3+ и C4+ в междоузлиях кристаллической решетки возможно только в тех случаях, когда эффективные размеры этих катионов не превышают размеры пор или "пустот" в кристаллической решетке, которые составляют 0,41 и 0,29 от размера атомов металла для октаэдрической и тетраэдрической пор соответственно.
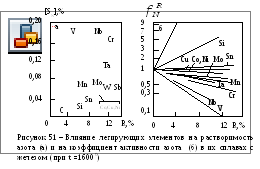
Расположение катионов N3+ и C4+ в кристаллической решетке приводит к поляризации их и к снижению их эффективного заряда. Хорошо известно сходное влияние азота и углерода на полиморфные превращения железа. С вышеописанным, однако, контрастирует резкое повышение растворимости азота в аустените уже не в атомарной форме, а в форме нитрида FeyN, где ему (азоту) принадлежит роль аниона (рис. 50).

Для
сталеплавильщиков большой интерес
представляет вопрос о влиянии примесных
и легирующих элементов на растворимость
азота в расплавах на основе железа. Он
исследовался рядом металлургов и сейчас
относится к числу хорошо изученных.
Широкую известность приобрели данные
о влиянии концентрации отдельных
компонентов бинарных сплавов на
растворимость в них азота при t=1600
С
[61] (рис. 51, а, б) и вычисленные по этим
экспериментальным данным значения
равновесных (с
![]() =0,1
МПа) при этой температуре активностей
азота в расплавах, а также параметре
взаимодействия первого порядка для
азота и элемента R,
т.е.
=0,1
МПа) при этой температуре активностей
азота в расплавах, а также параметре
взаимодействия первого порядка для
азота и элемента R,
т.е.
![]() . (142)
. (142)
Хотя
имеющиеся справочные данные по Шенку
[10] и Эллиотту [9]не полностью согласуются
между собой, в таблице 11 приведены
значения
![]() ,
опубликованные в работах [158,160] для
t=1600
и I200 °C.
,
опубликованные в работах [158,160] для
t=1600
и I200 °C.
Таблица
11 – Параметры взаимодействия первого
порядка
![]() для сплавов Fe-N
для сплавов Fe-N
|
Элемент |
1600 C |
1200 C |
|
Бор |
0,085 |
- |
|
Углерод |
0,13 |
0,11 |
|
Кислород |
0,00 |
0,00 |
|
Алюминий |
-0,028 |
- |
|
Кремний |
0,048 |
0,044 |
|
Фосфор |
0,050 |
0,074 |
|
Сера |
0,013 |
- |
|
Титан |
-0,045 |
- |
|
Ванадий |
-0,93 |
-0,18 |
|
Хром |
-0,045 |
-0,095 |
|
Марганец |
-0,020 |
-0,035 |
|
Кобальт |
0,011 |
0,0135 |
|
Никель |
0,010 |
- |
|
Медь |
0,006 |
- |
|
Мышьяк |
0,018 |
- |
|
Цирконий |
-0,63 |
- |
|
Ниобий |
-0,073 |
- |
|
Молибден |
-0,010 |
-0,05 |
|
Олово |
0,006 |
- |
|
Сурьма |
0,009 |
- |
|
Титан |
-0,033 |
- |
|
Вольфрам |
-0,002 |
- |
Из приведенных данных видно, что:
-
Полное отсутствие влияния кислорода на активность и растворимость азота как в жидком (при t=1600 °С), так и твердом (при t=1200 °С) железе;
-
Качественно одинаковый характер влияния легирующих и примесных элементов на растворимость азота в расплавленных и твердых сплавах железа;
-
Все нитридообразующе элементы повышают растворимость азота в расплавах на основе железа (т.е. имеют отрицательные значения
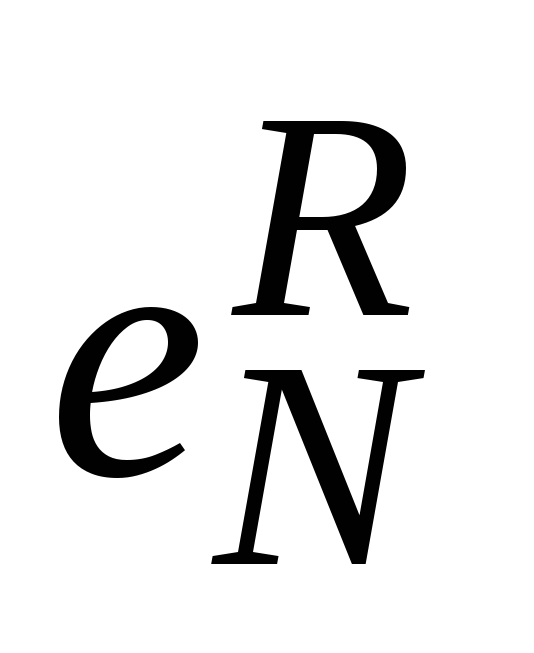 );
); -
Углерод, кремний и фосфор понижают растворимость азота в расплавленном железе. По данным работы [163] при концентрациях углерода, приближающихся к составу цементита (Fe3C) растворимость азота, даже при температурах расплава около 2500С, приближается к нулю;
-
Такие примесные элементы, как S, Cu, As, Sn, Sb также несколько понижают растворимость азота в расплавленном железе.
Применение параметров взаимодействия первого порядка обычно вполне достаточно для расчета растворимости азота в расплавах на основе железа. Лишь иногда – в случае высоколегированных сплавов – приходится пользоваться параметрами взаимодействия второго порядка:
 (143)
(143)
К
сожалению, значения
![]() вычислены далеко не для всех интересующих
металлургов компонентов сплавов железа.
вычислены далеко не для всех интересующих
металлургов компонентов сплавов железа.
Термодинамические характеристики нитридообразования для большинства встречающихся в сталях компонентов подробно проанализированы в работе [160]. Из таблицы 12 видно, что при Т=1900 К упругость диссоциации нитридов легирующих элементов несравненно выше соответствующей упругости диссоциации оксидов.
Таблица
12 – Параметры взаимодействия
![]() и
и
![]() и упругости диссоциации оксидов и
нитридов некоторых элементов при t=1900
К
и упругости диссоциации оксидов и
нитридов некоторых элементов при t=1900
К
|
Элемент |
B |
Al |
Si |
Ti |
V |
Cr |
Zr |
Nb |
Ce |
|
|
– 0,13 |
-1,0 0,006 |
-0,131 0,065 |
-5,0 -0,63 |
-0,11 -0,10 |
-0,041 -0,10 |
– – |
-0,14 -0,067 |
– – |
|
Оксид нитрид |
B2O3 BN |
Al2O3 AlN |
SiO2 Si3N4 |
Ti3O5 TiN |
V2O3 VN |
Cr2O3 CrN |
ZrO2 ZrN |
NbO2 NbN |
CeO2 CeN |
|
Оксид нитрид |
15,1 4,5 |
19,6 6,48 |
14,7 1,44 |
18,0 8,7 |
14,1 0,9 |
11,8 -1,42 |
20,4 10,4 |
12,75 – |
17,1 6,57 |
Это справедливо даже по отношению к церию и цирконию. Эти данные говорят о том, что нитриды даже "сильных" нитридообразующих элементов непрочны при температурах жидкого металла и позволяют предполагать образование нитридных неметаллических включений только при кристаллизации металла и при более низких температурах.
