- •I курса по профилю подготовки «Биология»
- •Введение
- •Общие правила работы в химической лаборатории.
- •Оформление лабораторной работы и лабораторного журнала
- •Лабораторная работа №1 определение молярной массы эквивалента металла по количеству выделившегося водорода Теоретическая часть.
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №2 взвешивание приготовление растворов. Титрование Теоретическая часть
- •Области перехода окраски некоторых рН-индикаторов
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №3 скорость химических реакций Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №4 буферные растворы. Буфетное действие Теоретическая часть
- •Расчет рН буферного раствора
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №5 гидролиз Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №6 окислительно-восстановительные реакци Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №7 химия элементов. Сера. Фосфор. Азот Теоретическая часть
- •Выполнение работы
- •Сера. Соединния серы
- •Азот. Соединения азота
- •Фосфор. Соединения фосфора
- •Контрольные вопросы
- •Лабораторная работа №8 химия соединений d – элементов Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Список рекомендуемой литературы
- •Содержание
Выполнение работы
Цель работы: Усвоение понятий эквивалент, молярная масса эквивалента, расчет эквивалентов простых и сложных веществ, знакомство с простейшим экспериментальным методом определения эквивалента элемента.
Меры предосторожности при выполнении работы:
1. Работать со стеклом аккуратно, не применяя чрезмерных усилий!
2. Раствор кислоты приливать аккуратно пользуясь для этого мерным цилиндром с носиком.
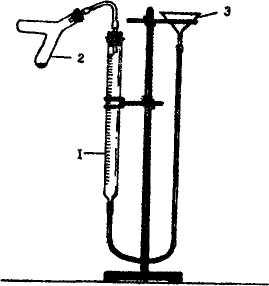
Прибор для определения молярной массы эквивалента металла изображен на рисунке.
|
|
|
Рисунок. Прибор для определения молярной массы эквивалента металла. |
Он состоит из бюретки на 50 мл (1), двухколенной пробирки Оствальда (2), открытой трубки, служащей в качестве уравнительного сосуда (3), стеклянного крана (или зажима) (4). Для укрепления прибора используется штатив с держателями и зажимами.
Собрать прибор в соответствии с рисунком, в уравнительный сосуд налить воду, которая заполнит бюретку и вытеснит из прибора воздух через открытый кран (4). Бюретку укрепить на штативе так, чтобы уровни воды в бюретке и открытой трубке совпадали с нулевым делением. Для удобства отсчета бюретку следует укрепить так, чтобы нулевое деление было на уровне глаз наблюдателя. Отсчеты уровня жидкости следует делать по нижнему краю мениска.
Получить навеску металла и поместить ее в одно из колен пробирки. В другое ее колено налить мерным цилиндром 24%-ый раствор соляной кислоты (HCl).
Прежде чем проводить реакции, следует убедиться в герметичности прибора (герметичность прибора - залог успеха опыта). Для этого плотно вставить пробки и закрыть кран тройника, уравнительный сосуд снять с держателя и опустить вниз на 15-20 см. Уровень воды в бюретке несколько снизится и остановится без изменения, если прибор герметичен. При возвращении сосуда на прежнее место вода, в нем и в бюретке должна остаться на том же нулевом уровне.
После того как установлена герметичность прибора, пробирку следует повернуть таким образом, чтобы кислота перелилась в то колено пробирки, где находится металл. Если реакция протекает медленно, то можно подогреть реакционную пробирку, погружая ее в стакан с горячей водой.
Водород, выделившийся в результате взаимодействия металла с раствором кислоты, вытесняет из бюретки воду. Уравнительный сосуд при этом надо опускать и во время опыта стараться держать воду в нем и бюретке на одном уровне, чтобы давление газа внутри прибора было все время близким к атмосферному.
Пока идет реакция, можно зарисовать в своей тетради установку, а также записать показания барометра – Р и термометра – °С.
Когда весь металл растворится, понижение уровня воды в бюретке прекратится. Окончательный точный отсчет показаний на бюретке следует сделать после охлаждения пробирки до комнатной температуры.
Результаты измерений и расчетов оформить в виде таблицы 1.
Таблица 1
|
№ |
Данные опыта |
Номер опыта | |
|
1 |
2 | ||
|
1 |
Масса навески металла, мг |
|
|
|
2 |
Атмосферное давление (по барометру), P атм. (кПа) |
|
|
|
3 |
Температура опыта, t º C |
|
|
Для приведения объема выделившегося водорода к нормальным условиям необходимо учесть, что водород, собранный над водой, содержит водяной пар и что общее давление газа в бюретке, равное атмосферному давлению, складывается из парциальных давлений водорода и водяного пара.
Таким образом, объем водорода при нормальных условиях определяется по уравнению:
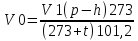
Используя закон эквивалентов, рассчитать молярную массу эквивалента исследуемого металла:
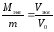
Вычисление величины ошибки проводят по формуле:
ΔM
= %
%
Опыт следует проводить 2-3 раза с одним и тем же металлом.
Таблица 2
Давление насыщенного пара при различных температурах.
|
Температура, °С |
Давление, мм.рт.ст. (h) |
Температура, 0С |
Давление, мм.рт.ст. (h) |
|
15 |
12,79 |
21 |
18,65 |
|
16
|
13,62 |
22 |
19,83 |
|
17 |
14,53 |
23 |
21,07 |
|
18 |
15,48 |
24 |
22,38 |
|
19 |
16,48 |
25 |
23,76 |
|
20 |
17,54 |
26 |
25,21 |