
- •I курса по профилю подготовки «Биология»
- •Введение
- •Общие правила работы в химической лаборатории.
- •Оформление лабораторной работы и лабораторного журнала
- •Лабораторная работа №1 определение молярной массы эквивалента металла по количеству выделившегося водорода Теоретическая часть.
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №2 взвешивание приготовление растворов. Титрование Теоретическая часть
- •Области перехода окраски некоторых рН-индикаторов
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №3 скорость химических реакций Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №4 буферные растворы. Буфетное действие Теоретическая часть
- •Расчет рН буферного раствора
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №5 гидролиз Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №6 окислительно-восстановительные реакци Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Лабораторная работа №7 химия элементов. Сера. Фосфор. Азот Теоретическая часть
- •Выполнение работы
- •Сера. Соединния серы
- •Азот. Соединения азота
- •Фосфор. Соединения фосфора
- •Контрольные вопросы
- •Лабораторная работа №8 химия соединений d – элементов Теоретическая часть
- •Выполнение работы
- •Контрольные вопросы
- •Список рекомендуемой литературы
- •Содержание
Контрольные вопросы
1. На примерах показать принципиальное различие трех типов окислительно-восстановительных реакций (примеры произвольные).
2. Пользуясь методом электронно-ионного баланса, закончить следующие уравнения:
а) MnO2 + HCl(конц) = Сl2 + …
б) KMnO4 + NaNO2 + H2SO4(разб) = MnSO4 + …
в) KMnO4 + Na2SO3 + H2SO4 (разб) = MnSO4 + …
г) J2 + Cl2 + H2O = HJO3 + …
д) Сl2 + KOH = KClO3 +
e) Cu + 4HNO3(разб) = …
ж) Mg + HNO3(разб) = …
з) S + Cl2 + … = H2SO4 + …
и) H2O2 + K2Cr2O7 = Cr+3O2 + O2 + KOH + H2O
3. Что произойдет, если к раствору иодида калия (KJ) добавить по каплям хлорную воду? Написать уравнение реакции. Указать окислитель и восстановитель.
4. Будет ли изменяться степень окисления азота при действии на подкисленный раствор нитрита натрия (NaNO2) соответственно раствора перманганата калия (KMnO4) и иодида калия (KJ)? Какие свойства, окислительные или восстановительные - проявляют при этом взаимодействующие компоненты?
5. В какой среде окислительные свойства перманганат-иона выражены сильнее?
6. Написать примеры уравнений реакций, в которых демонстрируются окислительные и восстановительные свойства пероксида водорода. Показать влияние среды на направление реакций.
7. Определите, как могут вести себя в окислительно-восстановительных реакциях следующие вещества: KNO2, J2, S, K2MnO4, H2O2. Какие из них могут быть только окислителями или только восстановителями, а какие способны быть и тем и другим в зависимости от условий?
Лабораторная работа №7 химия элементов. Сера. Фосфор. Азот Теоретическая часть
Р-элементами называют химические элементы, в атомах которых электрон с наивысшей энергией занимает р-орбиталь.
Каждый последующий р-элемент в группах в большей мере проявляет свойства неметалла, а его металлические свойства ослабевают. Орбитальные радиусы атомов с увеличением порядкового номера р-элемента в периоде уменьшаются, а энергия ионизации в общем возрастает.
Свойства р-элементов каждой подгруппы близки – все они являются электронными аналогами. В подгруппах с возрастанием порядкового номера р-элемента размеры атомов в общем увеличиваются, а энергия ионизации уменьшается. Электроотрицательность элементов при переходе в периоде от группы III к VII увеличивается, а в подгруппах сверху вниз уменьшается. Таковы общие тенденции изменения рассматриваемых констант.
Сера – химически активное вещество, особенно при повышенных температурах. Она непосредственно соединяется с многими простыми веществами, за исключением инертных газов, а так же азота N, теллура Te, йода I, платина Pt, золото Au. Однако соединения серы с азотом, теллуром, йодом, платиной и золотом синтезированы косвенными методами.
Для серы характерны окислительно-восстановительные реакции, при которых степень ее окисления изменяется по цепочке: минус 2, 0, +4, +6:
H2S-2 ⇄ S0 ⇄ S4+O2 ⇄ S6+O3
H2SO3 H2SO4
сульфиды сульфиты сульфаты.
Сера проявляет свойства окислителя при взаимодействии с простыми веществами – восстановителями (металлами, водородом, некоторыми неметаллами, имеющими меньшую электроотрицательность). При комнатной температуре сера окисляет щелочные и щелочноземельные металлы, медь, серебро и ртуть с образованием сульфидов:
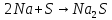 ,
,
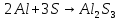 ,
,
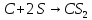 ,
,
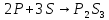 .
.
Восстановителем сера является по отношению к более сильным окислителям (кислороду, галогенам, кислотам-окислителям). Так, сера сгорает во фторе с образованием SF6. Реакция серы с хлором и бромом сильно ускоряется при нагревании:
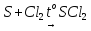 .
.
Взаимодействие со сложными веществами. Как восстановитель сера взаимодействует с кислотами-окислителями (HNO3, H2SO4):
 ,
,
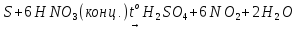 ,
,
 .
.
В воде сера не растворяется и даже не смачивается. Однако при высоких температурах сера диспропорционирует в атмосфере водяного пара:
 .
.
Проявляя свойства и окислителя, и восстановителя, сера вступает в реакции диспропорционирования с растворами щелочей при нагревании:
 .
.
Азот. Название элемента происходит от греческого «азот» − безжизненный, латинское название «nitrogenium» − рождающий селитру.
Молекула азота состоит из двух атомов N≡N, они прочно связаны друг с другом, чем и объясняется большая инертность азота при обычных условиях. Пассивность газообразного азота используют в технологии для создания инертной атмосферы для протекания химических реакций.
В химических реакциях азот может быть и окислителем и восстановителем.
Азот взаимодействует как окислитель:
а) при нагревании с литием Li, магнием Mg, кальцием Ca, титаном Ti с образованием нитридов:
 ;
;
б) при очень высокой температуре и в присутствии катализатора с водородом:
 .
.
Азот взаимодействует как восстановитель:
а) с кислородом при очень высокой температуре:
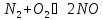 ;
;
другие оксиды азота при взаимодействии азота с кислородом не образуются;
б) с фтором:
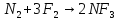 .
.
Фосфор обладает большим радиусом атома, чем азот, вследствие чего обладает меньшим сродством к электрону.
Фосфор химически более активен, чем азот. Химическая активность фосфора зависит от аллотропической модификации, в которой он находится. Так, наиболее активен белый фосфор, а наименее активен черный фосфор.
Фосфор непосредственно взаимодействует со многими простыми и сложными веществами. В химических реакциях фосфор, как и азот, может быть и окислителем, и восстановителем.
Как окислитель фосфор взаимодействует со многими металлами с образование фосфидов:
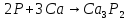 .
.
Как восстановитель фосфор взаимодействует с кислородом, галогенами, серой. При этом в зависимости от условий проведения реакции могут образоваться как соединения фосфора (III), так и соединения фосфора (V).
а) При медленном окислении или при недостатке кислорода образуется фосфористый ангидрид:
 ,
,
При сгорании фосфора в избытке кислорода образуется фосфорный ангидрид:
 .
.
б) В зависимости от соотношения реагентов при взаимодействии фосфора с галогенами и с серой образуются соответственно галогениды и сульфиды трех- и пятивалентного фосфора:
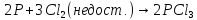 ,
,
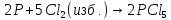 ,
,
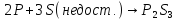 ,
,
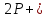 5S→
5S→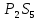 .
.
Следует отметить, что с йодом фосфор образует только соединение PI3.
Роль восстановителя фосфор играет в реакциях с кислотами-окислителями:
− с разбавленной азотной кислотой:
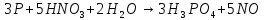 ;
;
− с концентрированной азотной кислотой:
 ;
;
− с концентрированной серной кислотой:
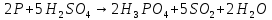 .
.
