
- •Специальные разделы курса
- •Моносахариды: образование простых и сложных эфиров, отношение эфиров к гидролизу; гликозидов (на примере d–маннозы); строение гликозидов, o–,n–,s–гликозиды, отношение гликозидов к гидролизу.
- •Моносахариды: окисление в гликоновые, гликаровые и гликуроновые кислоты; представители – d–глюконовая, d–глюкуроновая, d–галактуроновая кислоты; аскорбиновая кислота (витамин с).
- •Моносахариды: восстановление в полиолы; представители: d–сорбит, ксилит; открытая и циклические формы моносахаридов (на примере d–фруктозы и d–ксилозы).
- •Олигосахариды: принцип строения невосстанавливающих дисахаридов; сахароза; номенклатура; отношение к гидролизу, окислению катионами серебра (I) и меди (II).
- •Полисахариды: классификация; принцип строения гомополисахаридов на примере крахмала (амилоза, амилопектин), тип гликозидной связи; отношение крахмала к гидролизу.
- •Полисахариды: классификация; принцип строения на примерах декстранов, инулина, пектиновых веществ, типы гликозидной связи.
- •Полисахариды: строение целлюлозы; простые и сложные эфиры целлюлозы – ацетаты, нитраты, метил–, карбоксиметил– и диэтиламиноэтилцеллюлоза.
- •Производные пятичленных азотсодержащих ароматических гетероциклов: пиразолон и его таутомерия, лекарственные средства на основе пиразолона–3; гистидин, гистамин, бензимидазол, дибазол.
- •Шестичленные кислородсодержащие гетероциклы с одним гетероатомом: бензопироны – хромон, кумарин, флавон; флавоноиды – лютеолин, кверцетин; цианидиновая проба; катехины (вопр. 18).
- •Шестичленные гетероциклы с двумя гетероатомами: гидрокси– и аминопроизводные пиримидина (урацил, тимин, цитодин) – электронное строение, лактим–лактамная таутомерия.
- •Шестичленные гетероциклы с двумя гетероатомами: барбитуровая кислота – синтез, виды таутомерии, кислотные свойства; производные барбитуровой кислоты – барбитал, фенобарбитал.
- •Конденсированные гетероциклы: электронное строение, кислотно–основные свойства, таутомерия пурина; гидрокси– и аминопроизводные пурина – гипоксантин, ксантин, их таутомерия.
- •Конденсированные гетероциклы: мочевая кислота, ее электронное строение, лактим–лактамная таутомерия, кислотные свойства; соли мочевой кислоты (ураты); мурексидная проба.
- •Конденсированные гетероциклы: пурин – строение, ароматичность; производные пурина – аденин, гуанин, их таутомерия (вопр. 22).
- •Нуклеозиды: строение, классификация, номенклатура; отношение к гидролизу.
- •Нуклеотиды: строение, номенклатура, отношение к гидролизу.
- •Нуклеотидные коферменты: атф–строение, отношение к гидролизу.
- •Нуклеиновые кислоты: рнк и днк, первичная структура.
- •Алкалоиды: химическая классификация; основные свойства, образование солей. Представители: хинин, никотин, атропин.
- •Алкалоиды: метилированные ксантины (кофеин, теофиллин, теобромин); кислотно-основные свойства; их качественные реакции.
- •Алкалоиды: группа пиридина (никотин, анабазин) – строение, реакционная способность, общие реакции алкалоидов.
- •Алкалоиды: группа хинолина (хинин) – строение, талейохинная проба, основные свойства, образование солей.
- •Алкалоиды: группа изохинолина и фенантренизохинолина (папаверин, морфин, кодеин) – строение, основные свойства, характеристика реакционной способности.
- •Алкалоиды: группа тропана (атропин, кокаин) – строение, основные свойства, характеристика реакционной способности.
- •Липиды: триацилглицерины – принцип строения, номенклатура, реакционная способность (гидролиз, гидрогенизация, окисление), аналитические характеристики (иодное число, число омыления).
- •Липиды: фосфатидная кислота – строение; фосфолипиды (фосфатидилколамины, фосфатидилхолины) – состав, строение, гидролиз.
- •Терпены и терпеноиды: состав, химическое и пространственное строение производных ментана (ментол, терпин), их реакционная способность.
- •Терпены и терпеноиды: состав и строение бициклических монотерпенов (-пинен, борнеол, камфора), их реакционная способность.
- •Терпены и терпеноиды: классификация по числу изопреновых звеньев; дитерпены и тетратерпены (ретинол, ретиналь, β–каротин) – строение, реакционная способность.
- •Стероиды: родоначальные углеводороды (эстран, андростан, прегнан, холан, холестан); стереоизомерия, цис–транссочленение циклогексановых колец, –,β–стереохимические ряды.
- •Стероиды: производные холестана (стерины) – холестерин, эргостерин, витамин d2: номенклатура, строение, характеристика реакционной способности.
- •Производные холана (желчные кислоты): холевая и дезоксихолевая кислоты; гликохолевая и таурохолевая кислоты; их дифильный характер; строение, номенклатура, реакционная способность.
- •Производные прегнана (кортикостероиды): дезоксикортикостерон, гидрокортизон, преднизолон; строение, номенклатура, характеристика реакционной способности.
- •Производные эстрана (эстрогенные гормоны): эстрон, эстрадиол, эстриол; строение, номенклатура, характеристика реакционной способности.
- •Производные андростана (андрогенные гормоны): тестостерон, андростерон; строение, номенклатура, характеристика реакционной способности.
- •Агликоны сердечных гликозидов: дигитоксигенин, строфантидин; общий принцип строения и реакционная способность сердечных гликозидов.
-
Терпены и терпеноиды: классификация по числу изопреновых звеньев; дитерпены и тетратерпены (ретинол, ретиналь, β–каротин) – строение, реакционная способность.
Ди- и тетратерпеноиды. Молекулы дитерпеноидов содержат четыре изопреновых звена, молекулы тетратерпеноидов (каротиноидов) — восемь.
Ретинол (витамин А) и ретиналь образуются из каротиноидов. Оба соединения принимают участие в зрительном цикле.
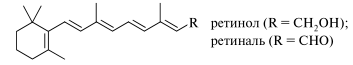
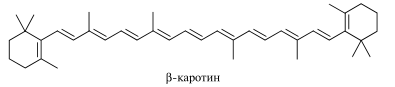
β-Каротин является наиболее значимым и распространенным каротиноидом. Он содержится в листьях растений, где совместно с хлорофиллом участвует в фотосинтезе, в большом количестве содержится в моркови, люцерне, гречихе и многих других растениях.
-
Стероиды: родоначальные углеводороды (эстран, андростан, прегнан, холан, холестан); стереоизомерия, цис–транссочленение циклогексановых колец, –,β–стереохимические ряды.
Стероиды представляют собой большую группу природных соединений как животного, так и растительного происхождения, объединяемую общностью углеродного скелета и путями биогенеза. В основе стероидов лежит полициклическая система гонана. Стероиды делятся на следующие группы:
• стерины;
• желчные кислоты;
• кортикостероиды (гормоны коры надпочечников);
• женские половые гормоны;
• мужские половые гормоны;
• агликоны сердечных гликозидов.
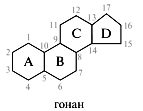

Стереоизомерия.
Для обозначения конфигурации асимметрических атомов углерода используется α,β-система. Суть ее состоит в том, что лиганды, расположенные перед условно плоским гонановым скелетом, обозначаются буквой β, а те, которые располагаются за плоскостью, — буквой α. Непременным условием является то, что при написании формулы кольца А и В при этом должны находиться в левом нижнем квадранте, а кольца С и D — в правом верхнем. Связи с β-лигандами обозначаются сплошными линиями, связи с α-лигандами — штриховыми. Необходимо отметить, что α- и β-заместители могут занимать в циклогексановых кольцах как аксиальные, так и экваториальные положения. Конфигурация хиральных центров в боковых цепях стероидов обозначается по R,S-системе.
В большинстве стероидов насыщенные циклогексановые кольца в гонановом скелете находятся в форме кресла. Кольца А, В, С и D имеют общие связи и могут быть сочленены двумя способами — по транс- и по цис-типу.
Порядок сочленения циклогексановых колец можно рассмотреть на простой модели, в качестве которой обычно используют декалин. Декалин существует в виде двух диастереомеров: транс- и цис-декалинов. В транс-декалине второе кольцо строится при участии двух экваториальных связей первого кольца; при этом атомы водорода у узловых третичных атомов углерода занимают относительно друг друга анти-положение и оказываются по разные стороны условно плоского углеродного скелета.
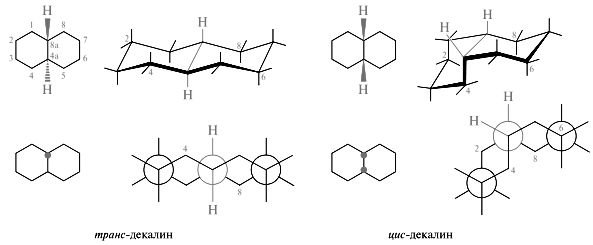
В цис-декалине построение второго кольца происходит за счет одной аксиальной и одной экваториальной связи первого кольца; при этом атомы водорода у атомов углерода С-4а и С-8а оказываются в синклинальном положении и по одну сторону условной плоскости, что хорошо видно из рассмотрения трехмерных стереохимических и сдвоенных проекционных формул Ньюмена.
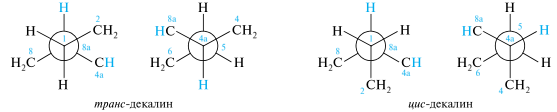
транс-Декалин является конформационно жесткой системой, в цис-декалине синхронно осуществляется инверсия циклогексановых колец.
В стероидах встречаются различные комбинации сочленения колец. Кольца А и В могут быть сочленены как по цис-, так и по транс-типу. Оба типа сочленения встречаются в природных стероидах. Кольца В и С почти всегда сочленены по транс-типу. Сочленение колец С и D обычно осуществляется по транс-типу, однако может встретиться и цис-сочленение, например в агликонах сердечных гликозидов. Чаще всего в основе природных стероидов лежат системы 5α- и 5β-гонана.
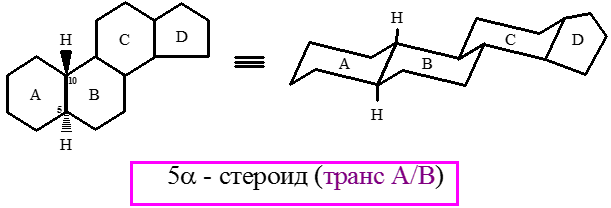
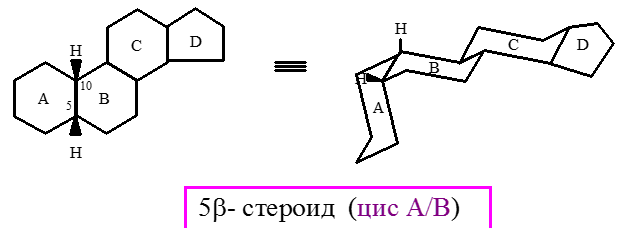
Как 5α-, так и 5β-гонаны представляют собой жесткие каркасные структуры, в которых не происходят конформационные превращения.
Номенклатура. Специфика номенклатуры стероидов состоит в том, что в основе их названий лежат стереородоначальные углеводородные структуры гомологов гонана: холан, холестан, прегнан и др. В полусистематических названиях указанных насыщенных углеводородов заложено не только строение, но и конфигурация асимметрических атомов в конденсированной системе и положение боковых цепей (α или β).
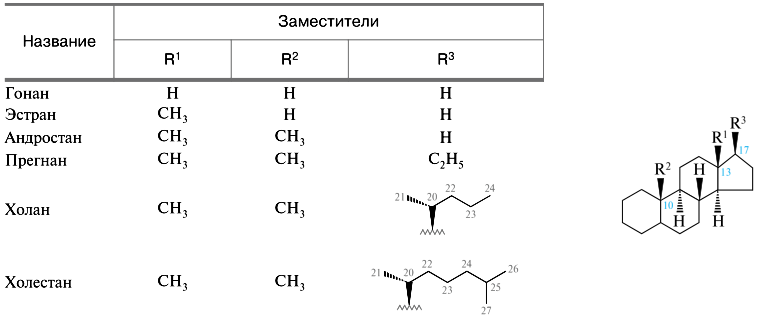
В названиях стероидов необходимо отражать порядок сочленения колец А и В, т. е. конфигурацию атома С-5. Конфигурация хиральных центров в полициклической системе обозначается помещением букв α или β перед соответствующими префиксами или после суффиксов. В остальном построение названий проводится по общим правилам заместительной номенклатуры.
