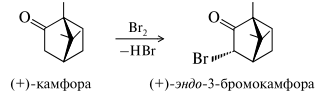- •Специальные разделы курса
- •Моносахариды: образование простых и сложных эфиров, отношение эфиров к гидролизу; гликозидов (на примере d–маннозы); строение гликозидов, o–,n–,s–гликозиды, отношение гликозидов к гидролизу.
- •Моносахариды: окисление в гликоновые, гликаровые и гликуроновые кислоты; представители – d–глюконовая, d–глюкуроновая, d–галактуроновая кислоты; аскорбиновая кислота (витамин с).
- •Моносахариды: восстановление в полиолы; представители: d–сорбит, ксилит; открытая и циклические формы моносахаридов (на примере d–фруктозы и d–ксилозы).
- •Олигосахариды: принцип строения невосстанавливающих дисахаридов; сахароза; номенклатура; отношение к гидролизу, окислению катионами серебра (I) и меди (II).
- •Полисахариды: классификация; принцип строения гомополисахаридов на примере крахмала (амилоза, амилопектин), тип гликозидной связи; отношение крахмала к гидролизу.
- •Полисахариды: классификация; принцип строения на примерах декстранов, инулина, пектиновых веществ, типы гликозидной связи.
- •Полисахариды: строение целлюлозы; простые и сложные эфиры целлюлозы – ацетаты, нитраты, метил–, карбоксиметил– и диэтиламиноэтилцеллюлоза.
- •Производные пятичленных азотсодержащих ароматических гетероциклов: пиразолон и его таутомерия, лекарственные средства на основе пиразолона–3; гистидин, гистамин, бензимидазол, дибазол.
- •Шестичленные кислородсодержащие гетероциклы с одним гетероатомом: бензопироны – хромон, кумарин, флавон; флавоноиды – лютеолин, кверцетин; цианидиновая проба; катехины (вопр. 18).
- •Шестичленные гетероциклы с двумя гетероатомами: гидрокси– и аминопроизводные пиримидина (урацил, тимин, цитодин) – электронное строение, лактим–лактамная таутомерия.
- •Шестичленные гетероциклы с двумя гетероатомами: барбитуровая кислота – синтез, виды таутомерии, кислотные свойства; производные барбитуровой кислоты – барбитал, фенобарбитал.
- •Конденсированные гетероциклы: электронное строение, кислотно–основные свойства, таутомерия пурина; гидрокси– и аминопроизводные пурина – гипоксантин, ксантин, их таутомерия.
- •Конденсированные гетероциклы: мочевая кислота, ее электронное строение, лактим–лактамная таутомерия, кислотные свойства; соли мочевой кислоты (ураты); мурексидная проба.
- •Конденсированные гетероциклы: пурин – строение, ароматичность; производные пурина – аденин, гуанин, их таутомерия (вопр. 22).
- •Нуклеозиды: строение, классификация, номенклатура; отношение к гидролизу.
- •Нуклеотиды: строение, номенклатура, отношение к гидролизу.
- •Нуклеотидные коферменты: атф–строение, отношение к гидролизу.
- •Нуклеиновые кислоты: рнк и днк, первичная структура.
- •Алкалоиды: химическая классификация; основные свойства, образование солей. Представители: хинин, никотин, атропин.
- •Алкалоиды: метилированные ксантины (кофеин, теофиллин, теобромин); кислотно-основные свойства; их качественные реакции.
- •Алкалоиды: группа пиридина (никотин, анабазин) – строение, реакционная способность, общие реакции алкалоидов.
- •Алкалоиды: группа хинолина (хинин) – строение, талейохинная проба, основные свойства, образование солей.
- •Алкалоиды: группа изохинолина и фенантренизохинолина (папаверин, морфин, кодеин) – строение, основные свойства, характеристика реакционной способности.
- •Алкалоиды: группа тропана (атропин, кокаин) – строение, основные свойства, характеристика реакционной способности.
- •Липиды: триацилглицерины – принцип строения, номенклатура, реакционная способность (гидролиз, гидрогенизация, окисление), аналитические характеристики (иодное число, число омыления).
- •Липиды: фосфатидная кислота – строение; фосфолипиды (фосфатидилколамины, фосфатидилхолины) – состав, строение, гидролиз.
- •Терпены и терпеноиды: состав, химическое и пространственное строение производных ментана (ментол, терпин), их реакционная способность.
- •Терпены и терпеноиды: состав и строение бициклических монотерпенов (-пинен, борнеол, камфора), их реакционная способность.
- •Терпены и терпеноиды: классификация по числу изопреновых звеньев; дитерпены и тетратерпены (ретинол, ретиналь, β–каротин) – строение, реакционная способность.
- •Стероиды: родоначальные углеводороды (эстран, андростан, прегнан, холан, холестан); стереоизомерия, цис–транссочленение циклогексановых колец, –,β–стереохимические ряды.
- •Стероиды: производные холестана (стерины) – холестерин, эргостерин, витамин d2: номенклатура, строение, характеристика реакционной способности.
- •Производные холана (желчные кислоты): холевая и дезоксихолевая кислоты; гликохолевая и таурохолевая кислоты; их дифильный характер; строение, номенклатура, реакционная способность.
- •Производные прегнана (кортикостероиды): дезоксикортикостерон, гидрокортизон, преднизолон; строение, номенклатура, характеристика реакционной способности.
- •Производные эстрана (эстрогенные гормоны): эстрон, эстрадиол, эстриол; строение, номенклатура, характеристика реакционной способности.
- •Производные андростана (андрогенные гормоны): тестостерон, андростерон; строение, номенклатура, характеристика реакционной способности.
- •Агликоны сердечных гликозидов: дигитоксигенин, строфантидин; общий принцип строения и реакционная способность сердечных гликозидов.
-
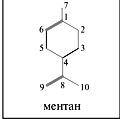
Терпены и терпеноиды: состав, химическое и пространственное строение производных ментана (ментол, терпин), их реакционная способность.
Ментол среди спиртов ряда ментана имеет наибольшее значение. Важнейшим источником является эфирное масло мяты перечной. Ментол следует рассматривать как вторичный спирт ряда циклогексана. В устойчивой конформации ментола все три заместителя находятся в экваториальном положении.
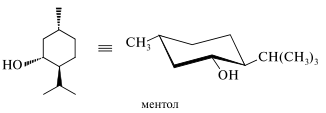
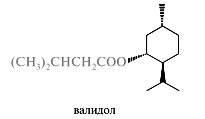
Ментол используется в пищевой и парфюмерной промышленности. Медицинское применение ментола весьма разнообразно: он входит в состав мазей, средств для ингаляции. В состав таких известных лекарственных средств, как валокордин, корвалол и валосердин, входит сложный эфир ментола и 2-бромо-3-метилбутановой (α-бромоизовалериановой) кислоты. Валидол является эфиром ментола и изовалериановой кислоты.
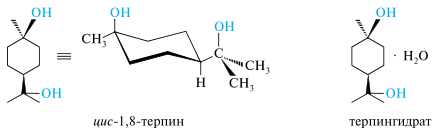
Терпин (ментандиол-1,8) в природных эфирных маслах не содержится, но образуется из других терпеноидов в момент выделения эфирных масел. Терпин существует в виде двух диастереомеров — цис- и транс-форм. Моногидрат цис-1,8-терпина называется терпингидратом и применяется в медицине в качестве отхаркивающего средства. При плавлении терпингидрат теряет кристаллизационную воду и превращается в цис-терпин, из которого на воздухе постепенно снова образуется терпингидрат. Получают терпингидрат синтетически из α-пинена.
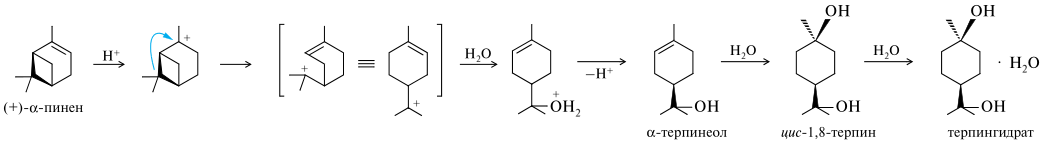
Терпин получают из α-пинена длительной (10-14 дн.) гидратацией разбавленной серной кислотой при температуре ниже комнатной. Вначале протонируется двойная связь, образующийся бициклический карбокатион перегруппировывается в карбокатион с углеродным скелетом ментана. Затем происходит присоединение воды, отщепление протона и образование α-терпинеола. Далее двойная связь α-терпинеола гидратируется по правилу Марковникова с образованием 1,8-терпина. На последнем этапе образуется гидратная форма терпина — терпингидрат.
-
Терпены и терпеноиды: состав и строение бициклических монотерпенов (-пинен, борнеол, камфора), их реакционная способность.
Бициклические монотерпеноиды также содержатся в эфирных маслах растений, строение их углеродного скелета может быть весьма разнообразным.
α-Пинен известен как один из самых распространенных в природе терпеноидов. Пинен входит в состав различных эфирных масел, является главным компонентом скипидаров хвойных растений. В основе пинена лежит бициклический насыщенный углеводород пинан.
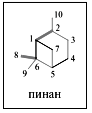
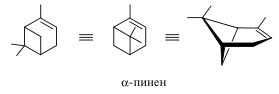
В структуре пинена имеется довольно напряженный четырехчленный цикл, поэтому многие реакции пинена по двойной связи сопровождаются перегруппировками углеродного скелета. Пинен, будучи наиболее доступным, используется в качестве исходного соединения для получения других терпеноидов, например терпингидрата и камфоры.
Миртеналь — компонент эвкалиптового масла, получается при окислении α-пинена оксидом селена(IV). Это пример региоселективного окисления алкенов по α-атому углерода относительно двойной связи C=C.


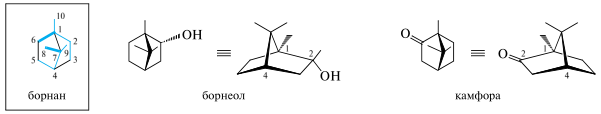
Борнеол и камфора — бициклические терпеноиды группы борнана.
Борнеол содержится в эфирном масле валерианы, тимьяна, борнейского лавра. В эфирном масле хвои сибирской пихты содержится до 40% левовращающего борнилацетата, который используют для синтеза камфоры. Камфора (борнанон-2) содержится в древесине камфарного лавра. В медицине камфору применяют в основном в качестве антисептического средства.
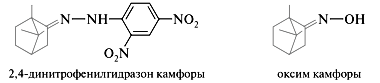
Камфора — типичный кетон, образует оксим, замещенные гидразоны, но не образует гидросульфитного производного. Образование гидросульфитного производного не происходит из-за пространственных затруднений. В молекуле камфоры кетонная группа соединена со вторичным и четвертичным атомами углерода, и именно последний сильно затрудняет подход к карбонильной группе такого объемного нуклеофила, как гидросульфит-ион. Образование оксима и динитрофенилгидразона используется в фармацевтическом анализе для количественного определения камфоры (качественная реакция).
При бромировании камфоры образуется эндо-3-бромокамфора, которая находит применение в медицине. Реакция протекает регио- и стереоселективно — замещение осуществляется в α-положение относительно кетонной группы и образуется эндо-изомер бромокамфоры.
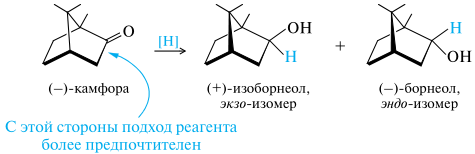
Восстановление камфоры. Камфора может быть восстановлена в борнеол различными методами.