
- •Специальные разделы курса
- •Моносахариды: образование простых и сложных эфиров, отношение эфиров к гидролизу; гликозидов (на примере d–маннозы); строение гликозидов, o–,n–,s–гликозиды, отношение гликозидов к гидролизу.
- •Моносахариды: окисление в гликоновые, гликаровые и гликуроновые кислоты; представители – d–глюконовая, d–глюкуроновая, d–галактуроновая кислоты; аскорбиновая кислота (витамин с).
- •Моносахариды: восстановление в полиолы; представители: d–сорбит, ксилит; открытая и циклические формы моносахаридов (на примере d–фруктозы и d–ксилозы).
- •Олигосахариды: принцип строения невосстанавливающих дисахаридов; сахароза; номенклатура; отношение к гидролизу, окислению катионами серебра (I) и меди (II).
- •Полисахариды: классификация; принцип строения гомополисахаридов на примере крахмала (амилоза, амилопектин), тип гликозидной связи; отношение крахмала к гидролизу.
- •Полисахариды: классификация; принцип строения на примерах декстранов, инулина, пектиновых веществ, типы гликозидной связи.
- •Полисахариды: строение целлюлозы; простые и сложные эфиры целлюлозы – ацетаты, нитраты, метил–, карбоксиметил– и диэтиламиноэтилцеллюлоза.
- •Производные пятичленных азотсодержащих ароматических гетероциклов: пиразолон и его таутомерия, лекарственные средства на основе пиразолона–3; гистидин, гистамин, бензимидазол, дибазол.
- •Шестичленные кислородсодержащие гетероциклы с одним гетероатомом: бензопироны – хромон, кумарин, флавон; флавоноиды – лютеолин, кверцетин; цианидиновая проба; катехины (вопр. 18).
- •Шестичленные гетероциклы с двумя гетероатомами: гидрокси– и аминопроизводные пиримидина (урацил, тимин, цитодин) – электронное строение, лактим–лактамная таутомерия.
- •Шестичленные гетероциклы с двумя гетероатомами: барбитуровая кислота – синтез, виды таутомерии, кислотные свойства; производные барбитуровой кислоты – барбитал, фенобарбитал.
- •Конденсированные гетероциклы: электронное строение, кислотно–основные свойства, таутомерия пурина; гидрокси– и аминопроизводные пурина – гипоксантин, ксантин, их таутомерия.
- •Конденсированные гетероциклы: мочевая кислота, ее электронное строение, лактим–лактамная таутомерия, кислотные свойства; соли мочевой кислоты (ураты); мурексидная проба.
- •Конденсированные гетероциклы: пурин – строение, ароматичность; производные пурина – аденин, гуанин, их таутомерия (вопр. 22).
- •Нуклеозиды: строение, классификация, номенклатура; отношение к гидролизу.
- •Нуклеотиды: строение, номенклатура, отношение к гидролизу.
- •Нуклеотидные коферменты: атф–строение, отношение к гидролизу.
- •Нуклеиновые кислоты: рнк и днк, первичная структура.
- •Алкалоиды: химическая классификация; основные свойства, образование солей. Представители: хинин, никотин, атропин.
- •Алкалоиды: метилированные ксантины (кофеин, теофиллин, теобромин); кислотно-основные свойства; их качественные реакции.
- •Алкалоиды: группа пиридина (никотин, анабазин) – строение, реакционная способность, общие реакции алкалоидов.
- •Алкалоиды: группа хинолина (хинин) – строение, талейохинная проба, основные свойства, образование солей.
- •Алкалоиды: группа изохинолина и фенантренизохинолина (папаверин, морфин, кодеин) – строение, основные свойства, характеристика реакционной способности.
- •Алкалоиды: группа тропана (атропин, кокаин) – строение, основные свойства, характеристика реакционной способности.
- •Липиды: триацилглицерины – принцип строения, номенклатура, реакционная способность (гидролиз, гидрогенизация, окисление), аналитические характеристики (иодное число, число омыления).
- •Липиды: фосфатидная кислота – строение; фосфолипиды (фосфатидилколамины, фосфатидилхолины) – состав, строение, гидролиз.
- •Терпены и терпеноиды: состав, химическое и пространственное строение производных ментана (ментол, терпин), их реакционная способность.
- •Терпены и терпеноиды: состав и строение бициклических монотерпенов (-пинен, борнеол, камфора), их реакционная способность.
- •Терпены и терпеноиды: классификация по числу изопреновых звеньев; дитерпены и тетратерпены (ретинол, ретиналь, β–каротин) – строение, реакционная способность.
- •Стероиды: родоначальные углеводороды (эстран, андростан, прегнан, холан, холестан); стереоизомерия, цис–транссочленение циклогексановых колец, –,β–стереохимические ряды.
- •Стероиды: производные холестана (стерины) – холестерин, эргостерин, витамин d2: номенклатура, строение, характеристика реакционной способности.
- •Производные холана (желчные кислоты): холевая и дезоксихолевая кислоты; гликохолевая и таурохолевая кислоты; их дифильный характер; строение, номенклатура, реакционная способность.
- •Производные прегнана (кортикостероиды): дезоксикортикостерон, гидрокортизон, преднизолон; строение, номенклатура, характеристика реакционной способности.
- •Производные эстрана (эстрогенные гормоны): эстрон, эстрадиол, эстриол; строение, номенклатура, характеристика реакционной способности.
- •Производные андростана (андрогенные гормоны): тестостерон, андростерон; строение, номенклатура, характеристика реакционной способности.
- •Агликоны сердечных гликозидов: дигитоксигенин, строфантидин; общий принцип строения и реакционная способность сердечных гликозидов.
-
Моносахариды: образование простых и сложных эфиров, отношение эфиров к гидролизу; гликозидов (на примере d–маннозы); строение гликозидов, o–,n–,s–гликозиды, отношение гликозидов к гидролизу.
Поскольку циклические формы моносахаридов — это внутренние полуацетали, то при взаимодействии со спиртами, в присутствии безводного хлороводорода, они будут взаимодействовать с одним эквивалентом спирта, образуя полный ацеталь или гликозид. В гликозидах различают сахарную часть (остаток глюкозы) и несахарную часть, остаток спирта, называемую агликоном. Для названия гликозидов характерно окончание -озид.
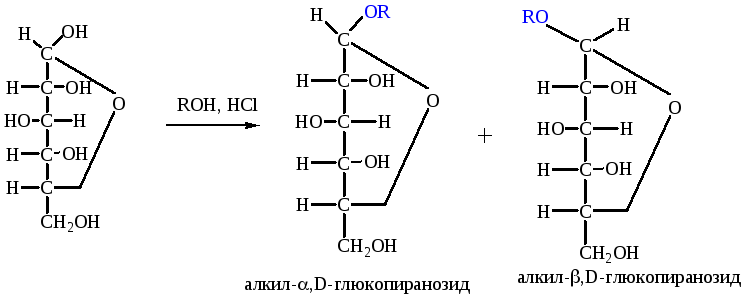
Гликозиды могут образовываться при взаимодействии со спиртами, фенолами, другими моносахаридами (О-гликозиды); при взаимодействии с аминами, азотистыми основаниями образуются N-гликозиды; существуют и S-гликозиды. Как и все ацетали, гликозиды гидролизуются разбавленными кислотами, проявляют устойчивость к гидролизу в щелочной среде. Гликозидная связь присутствует в полисахаридах, сердечных гликозидах, нуклеотидах, нуклеиновых кислотах.
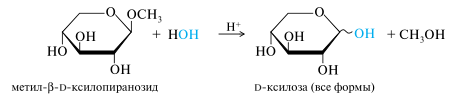
N-Гликозиды в зависимости от природы азотсодержащего агликона N-гликозиды подразделяются на три типа:
• гликозиламины — соединения, содержащие у аномерного центра аминогруппу или остаток алифатического или ароматического амина;
• гликозиламиды — соединения, в которых гликозильный остаток связан с амидным атомом азота, т. е. фрагментом —NНСОR;
• нуклеозиды — гликозильные производные гетероциклов.
В отличие от О- и N-гликозидов, S-гликозиды не получают прямой конденсацией моносахаридов с тиолами, так как в этом случае образуются преимущественно ациклические дитиоацетали.
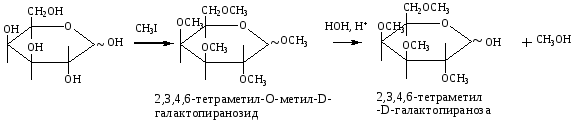
Простые эфиры получаются при взаимодействии спиртовых ОН-групп моноз с алкилгалогенидами (метилиодид и др.) Одновременно в реакцию вступает и гликозидный гидроксил, образуя гликозид. Простые эфиры не гидролизуются, а гликозидная связь расщепляется в кислой среде.
Сложные эфиры моносахаридов. Сложные эфиры образуются при взаимодействии моносахаридов с ацилирующими агентами, например, уксусным ангидридом.
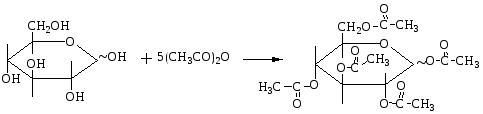
В метаболизме моносахаридов важную роль играют сложные эфиры фосфорной кислоты.
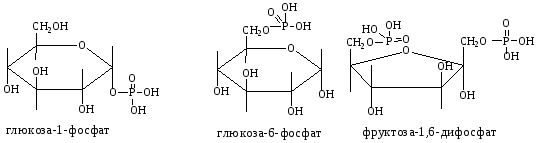
В синтетической практике применение находят ацетаты и в меньшей степени бензоаты сахаров. Они используются для временной защиты гидроксильных групп и для выделения и идентификации сахаридов.
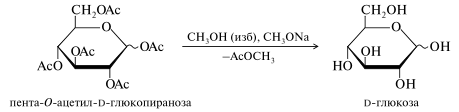
Сложные эфиры моносахаридов, подобно всем сложным эфирам, способны гидролизоваться как в кислой, так и в щелочной среде, высвобождая гидроксильные группы. Однако для удаления ацильных групп гидролиз никогда не используется. Более удобной в препаративном отношении является переэтерификация с низшим спиртом (обычно — метанолом), который служит и растворителем. Реакция протекает количественно при комнатной температуре в присутствии каталитических количеств алкоголята или триэтиламина.
-
Моносахариды: окисление в гликоновые, гликаровые и гликуроновые кислоты; представители – d–глюконовая, d–глюкуроновая, d–галактуроновая кислоты; аскорбиновая кислота (витамин с).
Глюкоза и другие альдомонозы дают реакции «серебряного зеркала», Троммера, Фелинга (качественная реакция). Эти реакции проводятся в щелочной среде, что способствует смещению таутомерного равновесия в сторону образования открытой формы. В данные реакции вступают не только альдозы, но и кетозы, которые в щелочной среде изомеризуются в альдозы.
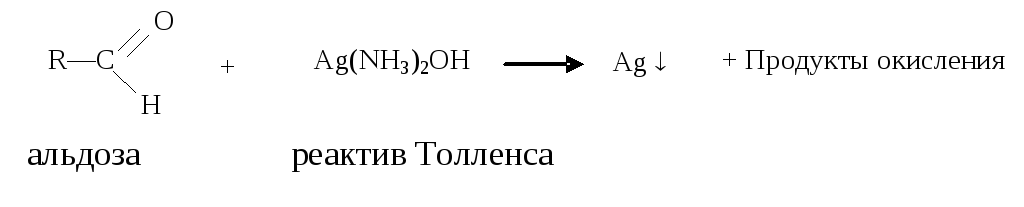
Реакция Фелинга является видоизмененной реакцией Троммера (с Cu(OH)2), так как реактив Фелинга представляет собой комплексное соединение Сu2+ с сегнетовой солью (К-, Na-винно-кислый).
CuSO4 + 2 NaOH → Cu(OH)2 + Na2SO4
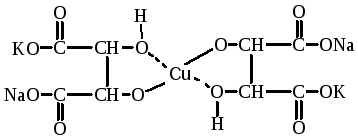
Комплекс устойчив, при нагревании его синий цвет не изменяется. Однако, если его нагреть в присутствии альдоз, то алкоголят гидролизуется, отщепляя сегнетову соль и Cu(OH)2, который и окисляет моносахарид.
2 Cu(OH)2 → [O] + H2O + 2 CuOH
2 CuOH → H2O + Cu2O
При действии на моносахариды слабых окислителей окисляется только альдегидная группа и образуются гликоновые кислоты. Так, из глюкозы образуется глюконовая кислота, а из галактозы — галактоновая.
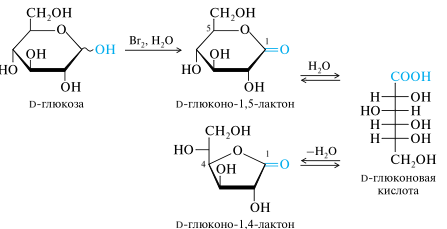
При действии сильных окислителей окислению подвергается не только альдегидная группа, но и первичная спиртовая группа. При этом образуются гликаровые (сахарные) кислоты.
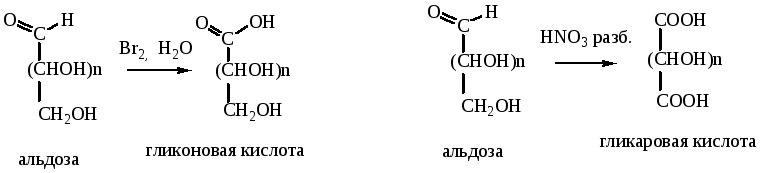
При окислении первичноспиртовой группы у последнего атома углерода альдогексоз без затрагивания альдегидной группы (путем ее защиты переводом в гликозид) образуются уроновые кислоты.
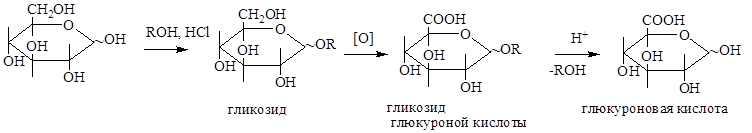
Уроновые кислоты (глюкуроновая, галактуроновая) входят в состав гетерополисахаридов, а также участвуют в детоксикации (связывании в виде гликозидов и выведении с мочой) ряда токсических соединений (фенолов, лекарственных веществ). Уроновые кислоты склонны к декарбоксилированию, в результате которого образуются соответствующие пентозы.
Представители.
D–Галактуроновая кислота (гексуроновая кислота) образуется в организмах окислением первичного гидроксила галактозы до карбоксильной группы. Галактуроновая кислота широко распространена в природе, являясь структурным компонентом ряда высших полисахаридов. Вместе с другими уроновыми кислотами, галактуроновая кислота легко образуется в тканях растений, входит в состав камедей, слизей и др.

Аскорбиновая кислота (витамин С) близка по структуре к моносахаридам и представляет собой -лактон 2-оксо-L-гулоновой кислоты. Проявляет довольно сильные кислотные свойства (рКа = 4,2), обусловленные ОН-группами ендиольного фрагмента. Аскорбиновая кислота синтезируется растительными и многими животными организмами. Исключение составляют морские свинки, некоторые птицы, обезьяны и человек. Поэтому в организм человека аскорбиновая кислота должна поступать с продуктами питания в количестве 75 мг в сутки. Витамин С является водорастворимым антиоксидантом, а также необходим для синтеза коллагена. При недостатке витамина С развивается цинга.
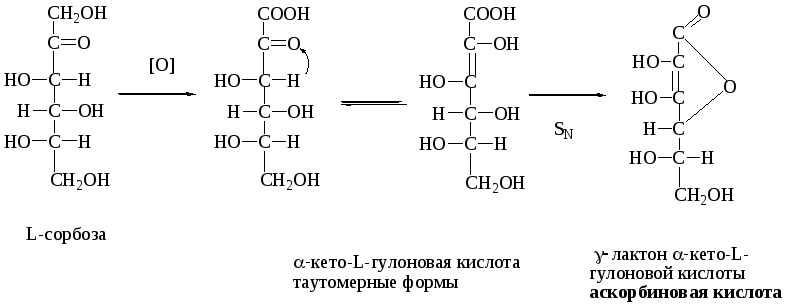
Аскорбиновая кислота окисляется в мягких условиях, и этот процесс обеспечивает некоторые окислительно-восстановительные реакции в организме, например, окисление α-аминокислоты пролина.

