
- •Методичні розробки
- •Частина 1
- •Ужгород – 2002
- •Передмова
- •Техніка експерименту в хімічній лабораторії
- •Загальні правила роботи в хімічній лабораторії
- •Предмет
- •Атомно-молекулярна теорія
- •Основні
- •Поняття
- •Прості та складні речовини
- •Хімічна символіка
- •Фізичні величини
- •Закон збереження маси
- •Закон еквівалентів
- •Закон сталості складу речовини
- •Закон кратних відношень
- •Газові закони
- •Закон Авогадро
- •Рівняння Менделєєва-Клапейрона
- •Хімічна термодинаміка
- •Термодинамічна система
- •Внутрішня енергія системи
- •Перший закон термодинаміки
- •Ентальпія системи
- •Тепловий ефект реакції
- •Закони термохімії
- •Термохімічні рівняння реакцій
- •Стандартний стан речовини
- •Термохімічні розрахунки
- •Поняття про ентропію
- •Другий закон термодинаміки
- •Хімічна кінетика
- •Поняття про швидкість хімічної реакції
- •Швидкість гомогенних реакцій
- •Швидкість гетерогенних реакцій
- •Залежність швидкості хімічної реакції від температури
- •Енергія активації хімічної реакції
- •Фотохімічні реакції
- •Ланцюгові реакції
- •З розгалуженими ланцюгами
- •Оборотні та необоротні реакції
- •Хімічна рівновага
- •Зміщення хімічної рівноваги
- •Фазові рівноваги
- •Каталіз
- •Розчини
- •Дисперсні системи
- •Розчини
- •Теорії розчинів
- •Розчинність речовин
- •Розчини
- •Розчини
- •Розчини твердих речовин
- •Способи вираження концентрації розчинів
- •Розчини неелетролітів
- •Тиск пари розчинів
- •Температура кипіння і температура замерзання розчинів
- •Розчини електролітів
- •Теорія електролітичної дисоціації
- •Ступінь електролітичної дисоціації
- •Ізотонічний коефіцієнт
- •Константа електролітичної дисоціації
- •Закон розведення
- •Властивості розчинів сильних електролітів
- •Добуток розчинності
- •Іонний добуток води
- •Водневий показник
- •Буферні розчини
- •Індикатори
- •Реакції у розчинах електролітів
- •Гідроліз солей
- •Ступінь гідролізу солі
- •Колоїдні розчини
- •Будова колоїдних часток
- •Окисно-відновні процеси електрохімічні процеси корозія
- •Ступінь окиснення елементу
- •Поняття про окисно-відновні реакції
- •Окисно-відновні властивості речовин
- •Класифікація окисно-відновних реакцій
- •Методи складання рівнянь окисно-відновних реакцій
- •У кислому середовищі:
- •У нейтральному середовищі:
- •В лужному середовищі:
- •Окисно–відновний потенціал
- •Еквівалент окисника і відновника
- •Електродний потенціал
- •Електричного шару
- •Гальванічний елемент
- •Стандартний електродний потенціал
- •Водневий електрод
- •Ряд стандартних електродних потенціалів металів
- •Електроди першого роду
- •Електроди другого роду
- •Окисно-відновні електроди
- •Іонселективні електроди
- •Електроліз
- •Корозія
- •Електрохімічна корозія
- •Захист металів від корозії
- •Загальні властивості полімерів
- •Полімери як високомолекулярні речовини
- •Структура полімерів
- •Реакція полімеризації
- •Механізми полімеризації
- •Властивості полімерів
- •Каучуки
- •Структура каучуків
- •Синтетичні каучуки
- •Вулканізація каучуків
- •Реакція поліконденсації
- •Пластмаси
- •Література для самостійної роботи студентів
Прості та складні речовини
Хімічна символіка
Символ елементу – це одна або дві перші букви латинських назв хімічних елементів. Хімічний символ елементу відображає один атом хімічного елементу. Знаючи символ елементу, можна, використовуючи періодичну таблицю елементів, назвати його, вказати число протонів в його атомі, а також величину відносної атомної маси.
Хімічна формула – це позначення складу сполуки за допомогою символів атомів елементів, з яких вона складається, та індексів – цифр, проставлених справа і трохи нижче від символу певного елементу, які вказують на число атомів цього елементу в сполуці (індекс 1 не ставиться). Використовують різні види хімічних формул:
Молекулярна формула відображає якісний склад речовини; кількісний склад речовини; одну молекулу речовини. Знаючи молекулярну формулу, можна встановити співвідношення мас елементів, які входять до складу речовини, а також молекулярну масу речовини.
Емпіричні формули базуються на результатах дослідів і відображають якісний склад речовин; стехіометричне співвідношення атомів елементів у речовині; одну умовну частку речовини.
Електронні формули схематично зображають механізм утворення хімічних зв’язків у молекулах. Вони записуються за допомогою хімічних символів та крапок, якими позначають електрони зовнішнього енергетичного рівня атомів, що приймають участь в утворенні хімічних зв’язків.
Графічні формули схематично зображають порядок сполучення атомів у молекулах. Графічні формули не відображають просторову будову молекули. Для зображення просторової будови користуються моделями молекул – кулестержневими.
Хімічні рівняння – це зображення перебігу хімічної реакції за допомогою хімічних символів, формул та коефіцієнтів. Коефіцієнти – це великі цифри, що стоять перед формулами речовин і показують число окремих атомів або молекул. Розрізняють такі види хімічних рівнянь: молекулярні, іонні, електронні та електронно-іонні рівняння напівреакцій, термохімічні:
молекулярні рівняння описують всі зміни в реакційній системі в цілому, при цьому речовини зображають молекулярними або емпіричними формулами:
2FeCl3+2KI+3H2SO4 2FeSO4+I2+6HCl+K2SO4;
іонні рівняння відображають реакції між іонами; в них не вказують іонів, що не беруть участь в реакції:
H++OH– H2O ;
10Cl–+2MnO4–+16H+ 5Cl2+2Mn2++8H2O ;
3) електронні рівняння напівреакцій описують процеси окиснення чи відновлення, які відбуваються під час окисно-відновних реакцій, тобто процеси переходу електронів:
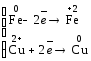 ;
;
в електронно-іонних рівняннях, окрім процесу переходу електронів вказують і іони, що беруть участь в окисно-відновних процесах
|
2 |
MnO4–+5 |
|
5 |
2Cl–
– 2 |
4) термохімічні рівняння – це рівняння, в яких вказується тепловий ефект хімічної реакції та агрегатний стан речовин: S(кр.) + O2(газ) SO2(газ) + 297 кДж
