
- •Методичні розробки
- •Частина 1
- •Ужгород – 2002
- •Передмова
- •Техніка експерименту в хімічній лабораторії
- •Загальні правила роботи в хімічній лабораторії
- •Предмет
- •Атомно-молекулярна теорія
- •Основні
- •Поняття
- •Прості та складні речовини
- •Хімічна символіка
- •Фізичні величини
- •Закон збереження маси
- •Закон еквівалентів
- •Закон сталості складу речовини
- •Закон кратних відношень
- •Газові закони
- •Закон Авогадро
- •Рівняння Менделєєва-Клапейрона
- •Хімічна термодинаміка
- •Термодинамічна система
- •Внутрішня енергія системи
- •Перший закон термодинаміки
- •Ентальпія системи
- •Тепловий ефект реакції
- •Закони термохімії
- •Термохімічні рівняння реакцій
- •Стандартний стан речовини
- •Термохімічні розрахунки
- •Поняття про ентропію
- •Другий закон термодинаміки
- •Хімічна кінетика
- •Поняття про швидкість хімічної реакції
- •Швидкість гомогенних реакцій
- •Швидкість гетерогенних реакцій
- •Залежність швидкості хімічної реакції від температури
- •Енергія активації хімічної реакції
- •Фотохімічні реакції
- •Ланцюгові реакції
- •З розгалуженими ланцюгами
- •Оборотні та необоротні реакції
- •Хімічна рівновага
- •Зміщення хімічної рівноваги
- •Фазові рівноваги
- •Каталіз
- •Розчини
- •Дисперсні системи
- •Розчини
- •Теорії розчинів
- •Розчинність речовин
- •Розчини
- •Розчини
- •Розчини твердих речовин
- •Способи вираження концентрації розчинів
- •Розчини неелетролітів
- •Тиск пари розчинів
- •Температура кипіння і температура замерзання розчинів
- •Розчини електролітів
- •Теорія електролітичної дисоціації
- •Ступінь електролітичної дисоціації
- •Ізотонічний коефіцієнт
- •Константа електролітичної дисоціації
- •Закон розведення
- •Властивості розчинів сильних електролітів
- •Добуток розчинності
- •Іонний добуток води
- •Водневий показник
- •Буферні розчини
- •Індикатори
- •Реакції у розчинах електролітів
- •Гідроліз солей
- •Ступінь гідролізу солі
- •Колоїдні розчини
- •Будова колоїдних часток
- •Окисно-відновні процеси електрохімічні процеси корозія
- •Ступінь окиснення елементу
- •Поняття про окисно-відновні реакції
- •Окисно-відновні властивості речовин
- •Класифікація окисно-відновних реакцій
- •Методи складання рівнянь окисно-відновних реакцій
- •У кислому середовищі:
- •У нейтральному середовищі:
- •В лужному середовищі:
- •Окисно–відновний потенціал
- •Еквівалент окисника і відновника
- •Електродний потенціал
- •Електричного шару
- •Гальванічний елемент
- •Стандартний електродний потенціал
- •Водневий електрод
- •Ряд стандартних електродних потенціалів металів
- •Електроди першого роду
- •Електроди другого роду
- •Окисно-відновні електроди
- •Іонселективні електроди
- •Електроліз
- •Корозія
- •Електрохімічна корозія
- •Захист металів від корозії
- •Загальні властивості полімерів
- •Полімери як високомолекулярні речовини
- •Структура полімерів
- •Реакція полімеризації
- •Механізми полімеризації
- •Властивості полімерів
- •Каучуки
- •Структура каучуків
- •Синтетичні каучуки
- •Вулканізація каучуків
- •Реакція поліконденсації
- •Пластмаси
- •Література для самостійної роботи студентів
Вулканізація каучуків
Гума – наповнений полімер, що має просторову будову. Гума більш еластична і стійка до зміни температури і дії розчинників (нерозчинна в бензині), ніж невулканізований каучук. Це пояснюється тим, що в гумі між лінійними макромолекулами крім міжмолекулярних сил існують також сили хімічних зв’язків. Каучук з масовою часткою сірки до 32% називають ебонітом. Ебоніт – тверда речовина з властивостями ізолятора.

Формальдегід полімеризується, утворюючи поліформальдегід – полімер лінійної структури:
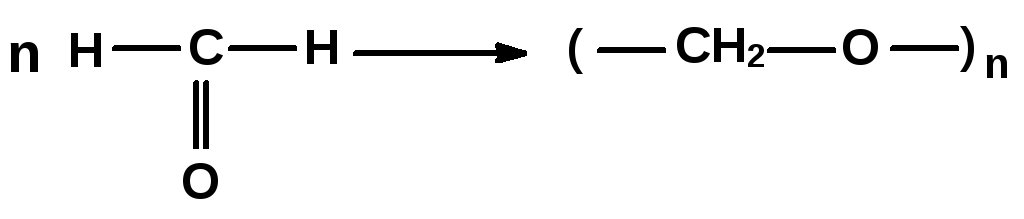
Формаьлдегід Поліформальдегід
З поліформальдегіду виготовляють оптичні деталі та деталі, якими замінюють металічні.
Реакція поліконденсації
Реакцією поліконденсації називається реакція утворення високомолекулярної сполуки, в процесі якої виділяються побічні низькомолекулярні продукти – вода, аміак, хлороводень тощо. Щоб зрозуміти зміст реакції, згадаємо, що у бензольному ядрі молекули фенолу атоми водню дуже рухливі (в положеннях 2, 4, 6), а формальдегід здатний до реакції приєднання за місцем подвійного зв’язку С=О:
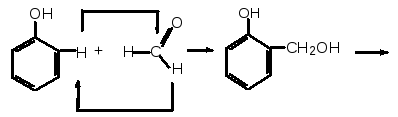
Сполука, що утворюється, є одночасно фенолом і ароматичним спиртом. Вона вступає в реакцію з другою молекулою фенолу:
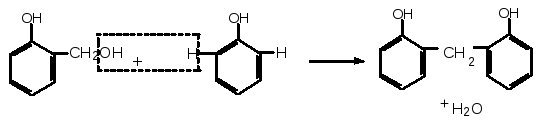
Утворена молекула містить два бензольних ядра і знову сполучається з наступною молекулою формальдегіду. Крім того, молекула формальдегіду може приєднуватись і в пара-положення
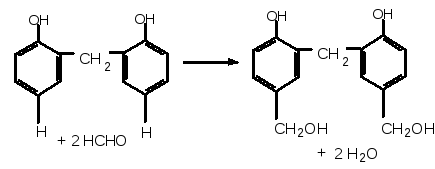
Потім знову відбувається взаємодія з молекулою фенолу і т.д. Будову утворених молекул можна зобразити такою формулою:
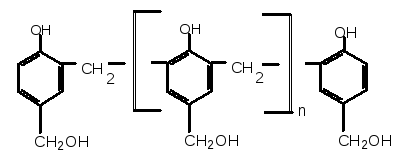
Утворюються резольні смоли, що мають лінійну будову і здатні розчинятися в органічних розчинниках. При подальшій поліконденсації утворюються резитоли, які при підвищеній температурі тільки розм’якшуються. А при подальшому нагріванні останні переходять у неплавкі резити, що мають просторову будову:
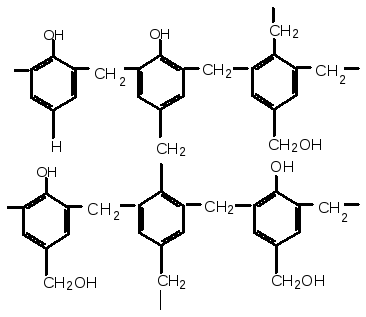
Фенолформальдегідні смоли відносяться до термореактивних. З фенолформальдегідних смол виробляють термостійкі пластмаси – фенопласти, текстоліт, які застосовують як теплозахисні, теплоізоляційні, антикорозійні матеріали.
До поліфункціональних сполук (що містять дві і більше функціональних групи) відносяться також двохатомні спирти, двохосновні карбонові кислоти, амінокислоти, вуглеводи та інші. Вони також здатні вступати у реакції поліконденсації, внаслідок яких утворюються полімери з високими технічними якостями.
Поліконденсацією терефталевої – двохосновної ароматичної карбонової кислоти з етиленгліколем – двохатомним спиртом одержують поліетилентерефталат
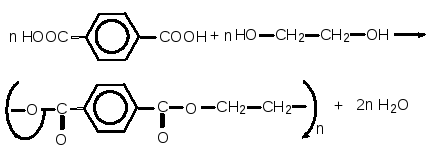
Поліетилентерефталат має високу механічну міцність, термостійкість, відмінні електроізоляційні властивості і знаходить застосування в металоплівкових конденсаторах, для виготовлення синтетичного волокна (лавсан), тари (РЕТ-пляшки) тощо.
Амінокислоти
містять дві фунціональні групи –
карбоксильну і аміногрупу. Для амінокислот
характерна реакція поліконденсації з
утворенням поліпептидів. В результаті
цієї реакції утворюється група атомів
 ,
яка називається пептидною, або амідною,
а зв’язок між атомами карбону та
нітрогену в ній – пептидним . Речовини,
які містять пептидні групи –поліпептиди.
За допомогою пептидних зв’язків залишки
α–амінокислот сполучаються і
утворюють молекули білків.
,
яка називається пептидною, або амідною,
а зв’язок між атомами карбону та
нітрогену в ній – пептидним . Речовини,
які містять пептидні групи –поліпептиди.
За допомогою пептидних зв’язків залишки
α–амінокислот сполучаються і
утворюють молекули білків.
Під час конденсації -амінокапронової кислоти утворюється капрон:
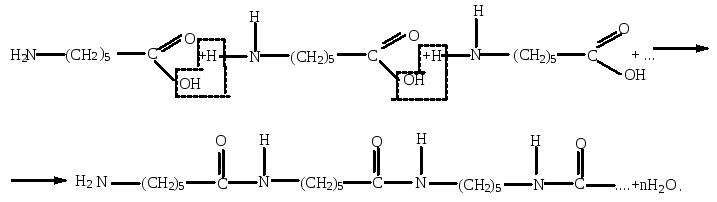
Молекули капрону мають лінійну структуру. Молекулярна маса макромолекул становить 16000–22000. У промисловості капрон одержують полімеризацією капролактаму (внутрішній циклічний амід ε-амінокапронової кислоти) у автоклаві (270 С, 1,5 – 2 МПа) у присутності невеликої кількості води. Одержаний продукт плавиться при 215ºС. Капрон витягують у волокно, яке не поглинає воду, не втрачає міцність, не гниє у вологому стані і не псується міллю. Воно більш стійке до стирання, ніж усі натуральні волокна. З капрону виготовляють механічні деталі, що замінюють металеві. Висока міцність капрону обумовлена утворенням численних водневих зв’язків між його макромолекулами в результаті взаємодії груп –NH– та –СО–. Але капрон має також істотні недоліки – його молекули гідролізуються під дією кислот в місцях амідних зв’язків, за температури 215 оС він плавиться.
Взаємодією гексаметилендиаміну з адипіновою кислотою одержують інший поліамід – найлон. Реакція поліконденсації :
