
- •4. Качественный химический анализ. Основные понятия. Предмет и средства. Чувствительность, специфичность, селективность.
- •Типы аналитических реакций:
- •1. Микрокристаллоскопический
- •2. Капельный
- •5. Классификация катионов и анионов на группы. Аналитические группы катионов. Обзор реакций.
- •6. Количественный анализ. Предмет и методы.
- •7. Весовой анализ. Принципы и методы объемного анализа. Растворы в объемном анализе.
- •8. Метод нейтрализации. Кислотно-основные индикаторы. Смешанные индикаторы. Кривые титрования. Титрование в неводных средах.
- •9. Комплексометрия. Реакции, применяемые в комплексометрии. Кривые титрования. Этилендиаминтетрауксусная кислота, как реагент в комплексометрии.
- •10. Редоксметрия. Перманганатометрическое титрование. Иодометрическое титрование. Электроды в редоксметрии.
- •11. Физико-химические и физические методы анализа. Общая характеристика методов.
- •12. Методы адсорбционного фотометрического анализа.
- •13. Хроматографический анализ. Классификация методов.
- •Классификация методов хроматографии
- •14. Жидкостная адсорбционная, ионообменная хроматография. Хроматография в тонком слое. Гель-хроматография.
- •15. Спектральные методы исследования органических соединений (уф-, ик- и ямр-спектроскопия).
- •16. Электронная спектроскопия органических соединений (уф-спектроскопия).
- •17. Законы поглощения света веществом. Коэффициент молярной экстинции.
- •18. Спектры поглощения органических соединений.
- •19. Возможности электронной спектроскопии в установлении строения органических соединений.
- •20.Спектры испускания (флуоресценция, фосфоресценция.)
- •21. Действие ик-излучения на молекулы органических соединений. Возможности ик-спектроскопии при изучении органических соединений.
- •22. Спектроскопия ядерного магнитного резонанса. Ядерный магнитный резонанс (ямр) и условия его возникновения.
- •23. Масс-спектрометрия органических соединений. Происхождение масс-спектров (ионизация молекул органических соединений при бомбардировке электронами, лазерного излучения и др.).
- •24. Рентгеноструктурный анализ органических соединений. Преимущества и недостатки метода рентгеноструктурного анализа в исследовании органических соединений.
- •2) Что такое активность? Как связана активноть иона и его равновесная концентрация? Что такое ионная ила ратвора, коэффициент активности?
- •3.Что такое мольная доля?
- •4.Как формулируется закон действия масс? Что такое термодинамичекая канстанта равноввессия? Какие факторы влияют на ее величину?
- •6)Что такое условная константа равновесия? Какие факторы влияют на ее величину?
- •8) В чем суть условия материального баланса? Сформулируйте принцип решения уравнения материального баланса.
- •9. Что такое константа диссоциации и степень диссоциации.
- •11. Как влияет введение одно- и разноименных ионов на степень диссоциации слабого электролита?
- •2. Что такое окислитель, восстановитель, окисление и восстановление?
- •3. Что называется электродным потенциалом?
- •4. Как влияет ионная сила на величину электродного потенциала?
- •5. Как влияет рН среды на величину потенциала? Выведите формулу зависимости потенциала от рН для полуреакции, протекающей с участием ионов водорода или гидроксида.
- •6. Как определить направление реакции окисления-восстановления и полноту ее протекания?
- •8. Приведите примеры использования окислительно-восстановительных реакций для растворения малорастворимых соединений.
- •9. Назовите основные окислители и восстановители, используемые для разделения и обнаружения ионов. Напишите соответствующие полуреакции.
- •12. Почему избыток хлорид-ионов мешает обнаружению ионов марганца по реакции образования перманганата?
- •13. Почему не удается обнаружить ион марганца (II) действием окислителя на концентрированные растворы солей марганца (II) ?
- •14. Напишите реакции взаимодействия бромид- и иодид-ионов с хлорной водой и объясните, в какой последовательности они протекают.
- •15. В каких условиях нитрат-ион можно восстановить до: а) аммиака; б) нитрит-иона?
- •1.Какие системы называются гетерогенными? Приведите примеры.
- •2. Выведите формулу константы растворимости.
- •3. Как выражают константу растворимости для идеальных и реальных систем? От чего зависит величина константы растворимости для этих систем?
- •4. Как связаны термодинамическая, реальная и условная константы растворимости?
- •5. Как влияет одноименный ион на растворимость осадка?
- •6. Почему при выделении осадка следует избегать большого избытка осадителя?
- •7. Как влияют электролиты на растворимость осадка?
- •8. Что называется растворимостью и молярной растворимостью?
- •9. Выведите формулу для расчета растворимости соединения АmВn.
- •10. В каких случаях по величинам констант растворимости можно сравнивать растворимость малорастворимых соединений?
- •11. Сформулируйте условия образования и растворения осадка.
- •12. Как влияет температура на растворимость осадка?
- •13. Каковы причины растворимости малорастворимых соединений: а) в кислотах; б) в щелочах?
- •16. Как перевести сульфаты катионов II группы в карбонаты?
- •1. Дайте определение следующим понятиям: разделение, концентрирование, абсолютное и
- •2. Приведите примеры классификаций методов разделения и концентрирования. На чем они основаны?
- •3. Осаждение и соосаждение как методы разделения и концентрирования.
- •4. Перечислите факторы, от которых зависит коэффициент распределения.
- •5. Какие из перечисленных параметров (концентрация, рН раствора, маскирующие вещества, температура) влияют на значение коэффициента распределения?
- •8. В чём сущность методов экстракции? Какие задачи решаются с помощью этих методов?
- •10. Какие процессы определяют скорость экстракции?
- •11. Классификация экстракционных систем.
- •12. Назвать органические растворители, наиболее часто используемые в методах экстракции.
- •13. Назвать основные типы соединений, в виде которых экстрагируются ионы металлов. Привести примеры.
- •14. Каковы достоинства и недостатки методов экстракции?
- •15. В чем сущность методов хроматографии?
- •16. Как классифицируются методы хроматографии по агрегатному состоянию фаз; механизму процесса разделения; технике выполнения и по цели проведения?
- •18. Каковы области применения, достоинства и недостатки методов адсорбционной хроматографии?
- •19. В чём сущность метода ионообменной хроматографии?
- •20. Назвать основные типы ионитов. Что называется обменной ёмкостью ионита?
- •21. Каковы области применения, достоинства и недостатки метода ионообменной хроматографии.
- •22. Пояснить сущность метода осадочной хроматографии. Назвать варианты этого метода анализа.
- •23. На чём основан качественный анализ методами осадочной и распределительной хроматографии на бумаге?
- •24. Как количественно оценивают способность различных веществ к разделению на бумаге?
- •28. В чем сущность тонкослойной хроматографии?
- •29. Каковы преимущества тонкослойной хроматографии перед другими хроматографическими методами?
- •1.Что такое комплексное соединение
- •2. Какие факторы влияют на устойчивость комплексных соединений
- •3.Какие принципы могут быть положены в основу классификации комплексных соединений?
- •4. Назовите основные типы комплексных соединений. Приведите примеры.
- •5. Дайте определение следующим понятиям: комплексообразователь, лиганды, координационное число, дентатность лиганда, заряд комплексного иона.
- •6. Что называется внутрикомплексным соединением? Приведите примеры
- •7. Какие равновесия имеют место в растворах комплексных соединений? Как можно охарактеризовать эти равновесия?
- •8.Что такое ступенчатые и общие константы устойчивости комплексных соединений?
- •9.Дайте теоретическое обоснование возможности использования комплексных соединений для избирательного растворения и осаждения малорастворимых соединений.
- •10.Какие свойства комплексных соединений имеют наиболее важное значение для обнаружения и разделения ионов?
- •11. Приведите примеры использования реакций комплексообразования для растворения:
- •13. Приведите примеры использования реакций комплексообразования для маскирования мешающих ионов.
- •14. Приведите примеры использования реакций комплексообразования для идентификации ионов.
16. Электронная спектроскопия органических соединений (уф-спектроскопия).
Электронная спектроскопия является очень чувствительным и удобным методом для определения спектров поглощения, пропускания или отражения, изучения кинетики реакции, сопровождающейся спектральными изменениями.
Электронные спектры поглощения наблюдаются в результате поглощения ультрафиолетового и видимого излучения; при этом происходит переход (возбуждение) валентного электрона с занимаемого им уровня на уровень с более высокой энергией. По типу поглощаемого излучения электронную спектроскопию часто называют спектроскопией в ультрафиолетовой и видимой области, или УФ-спектроскопией. Из всего спектра электромагнитного излучения глаз человека способен воспринимать лишь его небольшую «видимую» часть с длинами волн от 400 до 800 нм. Ультрафиолетовая область спектра простирается от 1 до 400 нм, однако, поскольку компоненты земной атмосферы поглощают излучение с длиной волны ниже 200 нм, под термином «ультрафиолетовые лучи» обычно понимают излучение с длиной волны 200-400 нм . Для изучения области спектра от 1 до 200 нм необходимо использовать вакуумные устройства («область вакуумного ультрафиолетового излучения», «дальняя ультрафиолетовая область»). Термины «ближняя и дальняя области» характеризуют положение по отношению к видимой области электромагнитного спектра. Солнечная радиация состоит в основном из опасного для жизни «вакуумного ультрафиолетового излучения», поэтому поглощение атмосферой излучения с длиной волны ниже 200 нм сохраняет жизнь на поверхности Земли.
17. Законы поглощения света веществом. Коэффициент молярной экстинции.
При прохождении излучения через раствор светопоглощающего вещества поток излучения ослабляется тем сильнее, чем больше энергии поглощают частицы данного вещества. Понижение интенсивности зависит от концентрации поглощающего вещества и длины пути, проходимого потоком.
коэффициентом пропускания:
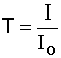 ,
,
где Io - интенсивность падающего потока света, I - интенсивность потока света, прошедшего через раствор.
Взятый с обратным знаком логарифм Т называют оптической плотностью А:
Уменьшение интенсивности излучения при прохождении его через раствор подчиняется закону Бугера - Ламберта - Бера:
-
lg T = A =
![]()
![]() С
, (5.3.)
С
, (5.3.)
где
![]() -
молярный коэффициент поглощения,
-
молярный коэффициент поглощения,![]() -
толщина поглощающего слоя, см; С -
концентрация раствора, моль / л.
-
толщина поглощающего слоя, см; С -
концентрация раствора, моль / л.
Следовательно, молярный коэффициент поглощения равен оптической плотности одномолярного раствора с толщиной слоя 1см. Молярный коэффициент поглощения - индивидуальная характеристика вещества, он зависит от природы вещества и длины волны и не зависит от концентрации и длины кюветы.
18. Спектры поглощения органических соединений.
Спектр поглощения — зависимость показателя поглощения вещества от длины волны (или частоты, волнового числа, энергии кванта и т. п.) излучения. Он связан с энергетическими переходами в веществе. Для различных веществ спектры поглощения различны.
Спектрометры, предназначенные для измерения поглощения электромагнитного излучения образцом, содержат источник излучения, кювету с веществом, через которую пропускают излучение, и детектор. Частоту излучения непрерывно меняют, а интенсивность света, попадающего на детектор, сравнивают с интенсивностью источника. Когда частота падающего света достигает определенного значения, происходит поглощение излучения веществом. Детектор отмечает снижение интенсивности прошедшего через образец (кювету) света. Зависимость между частотой света и поглощением, записанная на бумаге в виде линии, называется спектром.
При исследовании органических соединений обычно используют поглощение ИК-излучения.
