
- •П.А. Киселев, с.Б. Бокуть курс лекций по коллоидной химии
- •1. Коллоидная химия
- •1.1. Классификация коллоидных систем
- •1.2.Свойства коллоидных растворов
- •1.3. Методы приготовления коллоидных растворов
- •1.4. Оптические свойства и методы исследования коллоидных растворов
- •1.5.Рассеяние света (опалесценция)
- •1.6.Нефелометрия
- •1.7. Абсорбция (поглощение) света коллоидами и окраска коллоидных растворов
- •2. Молекулярно-кинетические свойства коллоидных растворов
- •2.1. Броуновское движение
- •2.2. Кинетическая устойчивость дисперсионных систем и седиментационное равновесие
- •2.3. Осмотическое давление
- •2.4. Равновесие Гиббса-Доннана
- •2.5. Электрические свойства коллоидных растворов. Электроосмос и электрофорез
- •2.6. Строение коллоидных частиц
- •3. Устойчивость дисперсных систем
- •3.1. Основные положения
- •3.2. Коагуляция гидрофобных коллоидов
- •3.3.Адсорбционно-сольватный барьер как фактор стабилизации коллоидных систем
- •3.4. Электрокинетический потенциал
- •3.5.Обратимость коагуляции. Пептизация
- •3.6. Студни и гели
- •4. Свойства растворов высокомолекулярных соединений
- •4.1. Набухание и растворение вмс
- •4.2. Термодинамические свойства растворов вмс
- •4.3. Вязкость растворов вмс
- •4.4. Растворы полимерных электролитов. Изоэлектрическая точка
- •5. Характеристика некоторых широко применяемых дисперсных систем
- •5.1. Общая характеристика эмульсий
- •5.2. Устойчивость эмульсий
- •5.3. Разрушение и обращение эмульсий
- •5.4. Пены
- •5.5. Суспензии
- •5.6. Аэрозоли
- •6. Характеристика некоторых спектральных методов исследования растворов вмс
- •6.1. Абсорбционная спектроскопия
- •6.2. Факторы, влияющие на абсорбционные свойства хромофора
- •6.3. Инфракрасная спектроскопия
- •6.4. Спектроскопия комбинационного рассеяния
- •6.5. Флуоресцентная спектроскопия
- •6.6. Изучение белков путем измерения их собственной флуоресценции
- •6.7. Поляризация флуоресценции
- •Содержание
3.5.Обратимость коагуляции. Пептизация
Лиофобные системы значительно различаются по свойствам в зависимости от степени их лиофилизации. Особенно ярко проявляется это различие при изучении их обратимости – способности коагулированных систем к пептизации. Пептизацией или дезагрегацией называется процесс, обратный коагуляции, а именно – переход коагулята в золь.
Пептизация тем более вероятна, чем более лиофилизирован исходный золь и чем меньше времени прошло с момента коагуляции, ибо с течением времени при ближнем взаимодействии постепенно происходит срастание частиц с уменьшением дисперсности и поверхностной энергии. В этом случае коагуляция принимает необратимый характер, и пептизация исключается. Практически пептизацию проводят в зависимости от причин, вызывающих коагуляцию. В случае концентрационной коагуляции, наступающей при С > Скр, следует, очевидно, отмыть коагулянт от электролита (используя декантацию, фильтрацию или диализ). В случае адсорбционной коагуляции, связанной с уменьшением электрического потенциала, следует повысить поверхностный заряд и потенциал частицы путем добавления электролита, содержащего потенциалобразующие ионы.
3.6. Студни и гели
Большинство лиофильных и некоторые лиофобные золи в определенных условиях превращаются в желатиноподобные массы, получившие название студней и гелей. Процесс желатинообразования – один из видов коагуляции, который не приводит к образованию осадка, а связывает растворитель и переходит в полужидкое – полутвердое состояние.
По своим свойствам студни делятся на хрупкие и эластичные. Название гелиобычно применяют для обозначения хрупких студней. Если из них выделить растворитель, то они сохраняют свою первоначальную форму и объем и могут поглотить ту или иную жидкость, подобно пористым телам.
Эластичные студни(клей, желатин, каучук и др.) при выделении жидкой фазы уменьшаются в объеме и могут поглощать не любую жидкость, а только жидкость определенного химического состава: желатин – воду, каучук – некоторые органические растворители, т.е. процесс является специфичным.
Поглощение сопровождается увеличением объема и называется набуханием.
Студни способны к набуханию при соприкосновении не только с жидкой фазой, но и соответствующим паром.
4. Свойства растворов высокомолекулярных соединений
4.1. Набухание и растворение вмс
При растворении ВМС, в отличие от НМС, обычно вначале происходит набухание, т.е. проникновение небольших и подвижных молекул растворителя в полимер. Молекулы растворителя ослабляют связи между молекулами ВМС ("раздвигают" молекулы ВМС). При растворении можно выделить четыре стадии существования системы (рис. 4.1).
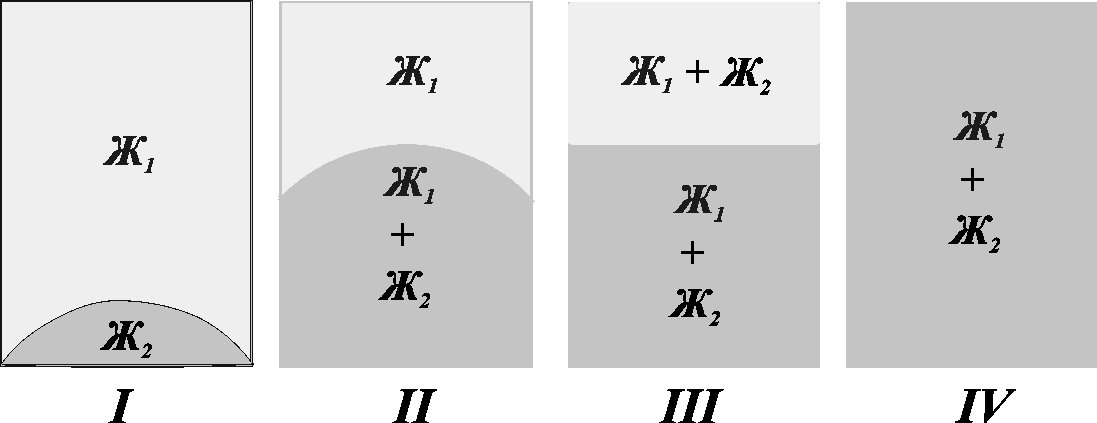
Рис.4.1. Изображение различных стадий набухания и растворения ВМС
В исходном состоянии система состоит из двух индивидуальных веществ – растворителя и полимера (I). Далее происходит набухание полимера и образование студнеобразного раствора низкомолекулярного растворителя в полимере ж1/ж2, погруженного в чистый растворитель ж1(II). В дальнейшем вследствие увеличения расстояния между макромолекулами и ослабления связей между ними происходит отрыв макромолекул и переход их в раствор. Образуются два раствора: жидкий – полимера в растворителе – ж1/ж2и студнеобразный – растворителя в полимере –ж2/ж1(III). В этом случае говорят об ограниченном набухании. В пределе наблюдается равномерное распределение молекул ВМС по всему объему низкомолекулярного растворения с образованием истинного раствора (IV).
Способность к набуханию в различных растворителях измеряется степенью набухания . Величина– это отношение массы, поглощенной низкомолекулярной жидкости к массе исходного полимера:=m-mo/mo, гдеmoиm– масса полимера до и после набухания. Часто о набухании судят не по привесу, а по увеличению объема образца.
На рис. 4.2 изображены типичные кинетические кривые для процессов ограниченного (1,2) и неограниченного (3) набухания.

Рис. 4.2. Типичные кинетические кривые набухания
Кривая 2 соответствует случаю частичного растворения полимера. Нередко такое ограниченное набухание при нагревании переходит в неограниченное (желатин в воде до 30 оС набухает ограниченно и неограниченно приt30оС).
Степень и скорость набухания зависят от сродства полимера к данному растворителю и от формы и строения его макромолекул. Неполярные полимеры, имеющие гибкие молекулы, неограниченно растворяются в неполярных жидкостях (каучук – в углеводородах). Появление поперечных связей приводит к ограниченному набуханию (резина, вулканизированный каучук – в тех же углеводородах).
Сильно полярные полимеры с жесткими цепями (целлюлоза) с неполярными жидкостями вообще не взаимодействуют, а в полярных только ограниченно набухают. Соединения, макромолекулы которых имеют глобулярную структуру, растворяются без набухания. Если набухающий полимер поместить в сосуд, то этот полимер может оказывать на стенки значительное давление, называемое давлением набухания. Величина давления набухания оказывается максимальной на начальных стадиях процесса и может достигать десятков мегапаскалей.
