
- •2)Оновные этапы развития фармхимии.Современные проблемы и перспективы.
- •5.Принципы класс-ии лс
- •6. Использование природных соединений в качестве лс
- •7. Получение лс путём химмодификац и полного хим синтеза
- •8. Применение микробиол метод и генной инженер для получ лс
- •10. Стандарты надлежащих практик.
- •11. Система контроля качества лекарственных средств в рб
- •12. Проблема фальсификации лс
- •13. Нормативная документация, регламентирующая качество лс. Гос.Фармакопея. Фармакопейные статьи.
- •14. Международная и национальные фармакопеи
- •15. Стабильность и сроки годности лс
- •16. Факторы окружающей среды, влияющие на стабильность лс
- •17. Типы химических реакций на стабильность приводящих к изменению лв…
- •18. Кинетические закономерности разрушения лс. Способы повышения стабильности
- •21. Фармацевтический анализ как составная часть фарм. Химии и раздел прикладной аналитич. Химии…..
- •22. Виды фармацевтического анализа:……
- •23. Основные принципы фармакопейного анализа…..
- •24. Предпосылки для выбора метода кол. Определения лв….
- •25. Отбор пробы и пробоподготовка при анализе…..
- •26. Особенности анализа многокомпонен. Лф
- •27. Особенности контроля качества лс аптечного изготовления….
- •19. Долгосрочные, ускоренные и стрессовые испытания стабильности лс…
- •20. Требования к контейнерам для хранения и условиям….
- •28.Нормативно-правовые акты регламентирующие контроль качества лс аптечного изготовления
- •29Сравнительная оценка хроматографических,спектрометрических,белковосвязывающих и др методов ,применяемых для определения лв в биологических
- •31.Исследования фармакокинетики лс.Основные фармакокинетические параметры:биодоступность,объем распределения…и т.Д
- •32.Метаболизм лв.Основные фазы метаболизма:несинтетическая(р-ции ок-я,восс-я,гидролиза) и синтетическая(р-ции конъюгации)
- •33.Биоэквивалентные иссследования генерических лс.Понятия терапевтической…и т.Д.
- •34.Особенности аналитического этапа биоэквивалентных исследований генерических лс
- •35.Связь между концентрацией Лс в биологических жидкостях и его действием.Терапевтический мониторинг лс
- •36.Валидация аналитических методик,используемых в фармацевтическом анализе
- •37. Гравиметрия. Кислотно-основное титрование в водных…
- •38. Окислительно-восстановительное титрование: иодометрия, хлориодометрия и т.Д
- •39.Комплексометрическое (комплексонометрия, меркуриметрия) и осадительное (аргентометрия) титрование. Применение
- •40. Атомно-абсорбционная и атомно-эмиссионная спектрометрия. Применение в фарм анализе
- •43. Спектрофотометрия ядерно-магнитного резонанса.
- •44.Флуориметрия. Применение в фарм анализе.
- •45. Спектрометрия комбинационного рассеяния, нефелометрия, турбидиметрия.
- •49.Вольтамперометрия и амперометрическое титрование.
- •48.Кондуктометрия,потенциометрия.
- •51.Тонкослойная хроматография.
- •50.Газовая хроматография
- •52.Жидкостная хроматография
- •53.Эксклюзионная хроматография
- •54Электрофорез
- •56.Термические методы анализа: термогравиметрия, дифференциальный термический анализ, дифферинциальная сканирующая калориметрия.Применение в фармацевтическом анализе.
- •57.Белоксвязывающие методы анализа: иммунохимические и рецепторные. Биологические методы анализа. Применение в фармацевтическом анализе.
- •60.Методы идентификации,исп в фармакопейном анализе. 1 и 2 идентификация. Применение инструментальных методов для идентификации фарм субстанций.
- •61. Общая фармакопейная статья гф рб «Реакции подлинности ( идентификации) на ионы и функциональные группы». Примеры реакций идентификации катионов.
- •62. Общая фармакопейная статья гф рб «Реакции подлинности ( идентификации) на ионы и функциональные группы». Примеры реакций идентификации анионов.
- •63.Общая фармакопейная статья гф рб «Реакции подлинности ( идентификации) на ионы и функциональные группы». Примеры реакций идентификации функциональных групп.
- •64)Определение температуры плавления, затвердевания, каплепадения, темпер пределов перегонки и темп кипения.
- •22 Температура каплепадения
- •65)Определение плотности и вязкости жидкостей. Виды вязкости
- •66)Определение удельного вращения и показателя преломления.
- •67)Потенциометрическое определение pH.
- •68)Природа и характер посторонних в-в в фарм субстанциях. Влияние примесей на качественный и количественный состав лс и его фарм активность. Допустимые и недопустимые примеси.
- •69)Общие и частные методы обнаружения примесей. Общая фарм статья гф рб:Испытания на предельное содержание примесей.
- •70)Определение окраски жидкостей, прозрачности и степени мутности жидкостей.
- •71)Определение летучих в-в и воды, потери в массе при высушивании, общей золы и сульфатной золы. Химический метод определения воды: акваметрия (Метод Карла Фишера)
- •72)Идентификация остаточных растворителей и контроль их количества. Определение микробиологической чистоты фарм субстанций.
- •72. Микробиологическая чистота субстанций и вспомогательных
- •73.Фарм. Контроль качества воды очищенной и для иньекций.
54Электрофорез
Под действием электрического поля заряженные частички, растворенные или диспергированные в растворе электролита, передвигаются в направление к электроду противоположной полярности, а молекулы с положительными и отрицательными зарядами передвигаются в направлении их суммарного заряда. Скорость передвижения прямо пропорциональна суммарному заряду частицы и обратно пропорциональна ее размеру, либо молекулярной массе.
Электрофоретическая подвижность является величиной, характерной для данного вещества. Различают абсолютную и относительную электрофоретическую подвижность. Абсолютная электрофоретическая подвижность под влиянием градиента потенциала 1 В на 1 см измеряется в сантиметрах в секунду. Относительная электрофоретическая подвижность есть отношение подвижности исследуемого вещества к подвижности другого вещества, принятого за стандарт.В гель-электрофорезе движение частиц замедляется взаимодействием с окружающей матрицей геля, что действует как молекулярное сито. Встречные взаимодействия электрической силы и молекулярного сита приводят к диференциации скорости передвижения частиц в зависимости от их размеров, форм и зарядов. В ходе электрофореза из-за различия физико-химических свойств, разные макромолекулярные смеси передвигаются с разной скоростью и, таким образом, разделяются на дискретные фракции.
Существует два различных метода электрофореза: фронтальный и зональный. Фронтальный электрофорез проводят в свободной незакрепленной среде, и он является единственным способом определения абсолютной электрофоретической подвижности. Зональный электрофорез проводят в закрепленной среде, роль которой состоит в стабилизации электрофоретических зон.КАПИЛЛЯРНЫЙ ЭЛЕКТРОФОРЕЗ Капиллярный электрофорез - это физический метод анализа, основанный на миграции внутри капилляра заряженных аналитов, растворённых в растворе электролита, под влиянием постоянного электрического поля. Скорость миграции аналита под влиянием электрического поля с напряжённостью E определяется электрофоретической подвижностью аналита и электроосмотической подвижностью буферного раствора внутри капилляра. Электрофоретическая подвижность вещества (pep) зависит от его свойств (электрический заряд, размер и форма молекул) и от свойств буферного раствора, в котором происходит процесс миграции (тип и ионная сила электролита, рН, вязкость и наличие добавок). Электрофоретическая скорость (vep) вещества, частицы которого принимаются за сферические, описывается уравнением:
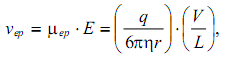
где: q - эффективный заряд вещества, n - вязкость раствора электролита, r -Стоксовский радиус частиц вещества, V - приложенное напряжение, L - общая длина капилляра.
При помещении капилляра, заполненного буферным раствором, в электрическое поле внутри капилляра начинается перемещение растворителя, называемое электроосмотическим потоком. Скорость электроосмотического потока зависит от электроосмотической подвижности, которая, в свою очередь, зависит от плотности заряда на внутренней стенке капилляра и свойств буферного раствора. В зависимости от заряда вещества электрофоретическая подвижность аналита и электроосмотическая подвижность могут быть направлены одинаково или противоположно. В условиях нормального капиллярного электрофореза анионы перемещаются в направлении, противоположном направлению электроосмотического потока, а их скорости меньше электроосмотической скорости. Катионы мигрируют в направлении, совпадающем с направлением электроосмотического потока, а их скорости превышают электроосмотическую скорость. В условиях, когда электроосмотическая скорость превышает электрофоретическую, катионы и анионы могут быть разделены в течение одного анализа.
Время (t), необходимое веществу для миграции на расстояние (/) от конца капилляра, в который вводится вещество, до точки детекции (эффективная длина капилляра), определяется выражением:
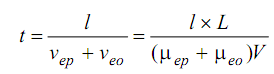
В общем, при рН более 3 капилляры с немодифицированной поверхностью, изготовленные из плавленого кварца, имеют отрицательный заряд, обусловленный ионизацией силанольных групп, расположенных на внутренней стенке капилляра. Соответственно, электроосмотический поток направлен от анода к катоду. Разделение двух полос (выражаемое как разрешение, Rs) может быть достигнуто при изменении электрофоретич. подвижности аналитов либо электроосмотической подвижности, а также при увеличении эффективности полосы для каждого аналита.
55.Масс-спетрометрия.Сочетание масс-спектрометрии с хроматографическими методами (ГХ-МС,ЖС-МС).Применение в фармацевтическом анализе.
Масс-спектрометрия основана на прямом измерении отношения массы к числу элементарных положительных или отрицательных зарядов ионов (m/z), полученных из анализируемого вещества и находящихся в газовой фазе. Данное отношение выражается в атомных единицах массы (1 а.е.м. = одной двенадцатой массы нуклида 12С) или в дальтонах (1 Да = массе атома водорода).
Ионы, образовавшиеся в ионном источнике, ускоряются и перед попаданием
в детектор разделяются с помощью масс-анализатора. Все эти действия
происходят в камере, в которой насосная система поддерживает вакуум от 10−3 до 10−6 Па.
Результирующий масс-спектр является графиком зависимости
относительного количества различных ионов от отношения m/z. Сигнал,
отвечающий иону, представлен несколькими пиками, соответствующими
статистическому распределению различных изотопов этого иона. Такой сигнал называется изотопным профилем, а пик (по крайней мере, для небольших молекул), представляющий наиболее распространённые изотопы для каждого атома, - моноизотопным пиком.
Масс-спектрометрический анализ даёт важную качественную (определение
молекулярных масс; информация, касающаяся структуры определяемых
фрагментов) и количественную (с использованием внешнего или внутреннего стандартов) информацию с пределом обнаружения от пикомоля до фемтомоля.
Первой стадией анализа является ввод образца в прибор без значительного
нарушения вакуума. В широко распространённом методе, называемом прямым вводом жидкости, образец помещается на конец цилиндрического штока (в кварцевом тигле, на проволоке или на металлической поверхности). Этот шток через вакуумный шлюз, в котором поддерживается первичный промежуточный вакуум между атмосферным давлением и вторичным вакуумом прибора, вводится в спектрометр.
Другие системы ввода позволяют проанализировать компоненты смеси, так
как они разделяются с помощью соответствующего прибора, соединённого с масс- спектрометром.
Газоваяхроматография/масс-спектрометрия. При использовании подходящих колонок (капиллярных или полукапиллярных) возможно непосредственное введение конца колонки в ионный источник прибора без сепаратора.
Жидкостнаяхроматография/масс-спектрометрия. Такая комбинация особенно полезна для анализа полярных соединений, которые являются недостаточно летучими либо слишком термолабильными, для того чтобы их можно было проанализировать методом газовой хроматографии в сочетании с масс-спектрометрией. Данный метод осложняется трудностью получения ионов в газовой фазе из жидкой фазы, что требует применения специальных интерфейсов, таких как:
- прямой жидкостный ввод: подвижная фаза распыляется и растворитель испаряется перед ионным источником прибора,
- интерфейс с пучком частиц: подвижная фаза, скорость которой может достигать 0,6 мл/мин, распыляется в десольватационной камере, в результате в ионный источник прибора попадают лишь анализируемые вещества в нейтральной форме; данный способ может быть использован для соединений с относительно низкой полярностью и молекулярными массами меньше 1000 Да,
- интерфейс с движущейся полосой: подвижная фаза, скорость которой может достигать 1 мл/мин, наносится на поверхность движущейся полосы; после выпаривания растворителя анализируемые вещества переносятся к ионному источнику прибора, где подвергаются ионизации; данный способ плохо подходит для очень полярных или термолабильных соединений.
Другие виды интерфейсов (электрораспыление, термораспыление, химическая ионизация при атмосферном давлении) могут рассматриваться как самостоятельные методы ионизации и описаны в разделе, посвящённом способам ионизации.
