
- •Физическая и коллоидная химия
- •240134 Переработка нефти и газа
- •Содержание
- •2 Рабочая программа учебной дисциплины
- •2.1 Паспорт рабочЕй программы учебной дисциплины Физическая и коллоидная химия
- •2.1.1 Область применения рабочей программы
- •2.1.3 Цели и задачи учебной дисциплины – требования к результатам освоения учебной дисциплины:
- •2.1.4 Рекомендуемое количество часов на освоение рабочей программы учебной дисциплины: Физическая и коллоидная химия
- •2.2 Структура и содержание учебной дисциплины
- •2.2.1 Объем учебной дисциплины и виды учебной работы
- •2.2.2 Тематический план и содержание учебной дисциплины _____Физическая и коллоидная химия_______
- •2.3 Условия реализации учебной дисциплины
- •2.3.1 Требования к минимальному материально-техническому обеспечению
- •2.3.2 Информационное обеспечение обучения
- •Еремин в.В., Каргов с.И. И др. Основы физической химии. Теория и задачи. - м.: Экзамен, 2005. - 480 с.
- •3 Методические указания по изучению учебного материала по теме Введение
- •Вопросы для самоконтроля
- •Методические указания по теме 1.1 Молекулярно-кинетическая теория агрегатных состояний вещества
- •Вопросы для самоконтроля
- •Методические указания по теме 1.2 Основы химической термодинамики
- •Вопросы для самоконтроля
- •Методические указания по теме 1.3 Химическая кинетика
- •Вопросы для самоконтроля
- •Методические указания по теме 1.4 Катализ
- •Вопросы для самоконтроля
- •Методические указания по теме 1.5 Химическое равновесие
- •Решение. Используем формулу
- •Вопросы для самоконтроля
- •Методические указания по теме 1.6 Фазовое равновесие
- •Вопросы для самоконтроля
- •Методические указания по теме 1.7 Растворы
- •Вопросы для самоконтроля
- •Методические указания по теме 1.8 Электрохимия
- •Вопросы для самоконтроля
- •Методические указания по теме 2. 1 Дисперсные системы
- •Вопросы для самоконтроля
- •Литература: [1], с.214-216, с.230-259, с. 263-271; [2], с.329-373; [3], с.209-214; [4], с.165-170
- •Вопросы для контрольной работы №1
- •5 Список вопросов к экзамену
Вопросы для контрольной работы №1
Уравнение состояния идеального газа. Универсальная газовая постоянная, ее физический смысл, численное значение и размерность.
Определить массу паров свинца в камере объемом 12 м3 при 1640° С. Давление паров свинца при этой температуре 8941 Па.
Выведите основное уравнение молекулярно-кинетической теории газов.
Что называется приведением газа к нормальным условиям?
При н.у. объем газа равен 82 м 3. Какой объем займет этот же количество газа при -15 о С и 99280 Па?
Молекулярно-кинетическая теория идеального газа. Основные допущения. Законы идеального газа, их математическое и графическое изображение.
Газ при нормальных условиях занимает объем 100 л. Определить, как изменится его давление, если этот газ нагреть до 20° С, не изменяя объема.
Отклонения реальных газов от идеальных. Причины этих отклонений. Уравнение состояния реальных газов. Для чего вводятся поправки?
По уравнению Ван-дер-Ваальса вычислить температуру, при которой объем 1 кмоль сероводорода под давлением 6,66 . 10 6 Па станет равным 500 л.
Закон Дальтона.
Смесь состоит из 95 г водорода и 80 г метана. Определить парциальные давления каждого из газов и общее давление смеси, если газы находятся сосуде, емкость которого равна 60 л, а температура смеси равна 27 0С.
Сжижение газов.
Какой объем аммиака может быть получен при разложении 1 кг нитрида кальция? Условия нормальные.
Особенности жидкостей. Современные взгляды на структуру жидкости.
Определить поверхностное натяжение толуола при 50° С, если при медленном его выпускании из сталогмометра масса 38 капель равна 1,4864 г, а при выпускании из того же сталогмометра воды при той же температуре масса 25 капель ее оказалась равной 2,6570 г. Величина поверхностного натяжения воды при 50°С равна 67,91103 Н/м.
Вязкость жидкостей и ее зависимость от внешних условий. Измерение вязкости жидкостей с помощью вискозиметра.
Плотность гептана при 20°С равна 684 кг/м3, а плотность воды 998 кг/м3. Некоторое количество гептана протекает через вискозиметр за 83,9 с, а для того же объема воды при тех же условиях требуется 142,1 с. Определить абсолютную вязкость гептана при 20°С, если вязкость воды при этой же температуре равна 1,00510-3 Пас.
Поверхностное натяжение жидкостей. Измерение поверхностного натяжения жидкостей с помощью сталагмометра.
Из сталагмометра при 40° С выпускали последовательно воду и бензол в воде. При этом общая масса выпущенных жидкостей соответственно была равна 2,6352 и 1,4572, а число капель — 23 и 40. Вычислить поверхностное натяжение бензола. (Поверхностное натяжение воды равно 72,75∙10-3 Н/м).
Особые свойства кристаллических веществ. Что называется кристаллической решеткой? Виды кристаллических решеток.
Плазма. Общая характеристика.
Сжатый воздух в баллоне имеет температуру 15о С. Во время пожара температура воздуха в баллоне поднялась до 450о С. Взорвется ли баллон, если при этой температуре он может выдержать давление не более 9,8·106 Па? Начальное давление 4,8·10 6 Па.
Закон сохранения энергии и первый закон термодинамики, его содержание, формулировки. Аналитическое выражение первого закона термодинамики, в том числе для изобарных и изохорных процессов.
Какое количество теплоты выделится при изотермическом сжатии 10 л идеального газа, взятого при 27° С и нормальном атмосферном давлении, если объем его уменьшится в 10 раз?
Что называется теплоемкостью вещества?
Температурная зависимость истинной молярной теплоемкости воздуха выражается уравнением Ср = 27,2 + 0,0042 Т . Вычислить истинную молярную и массовую теплоемкости воздуха при постоянных давлении и объеме при 400 о С, если соотношение Ср / Сv для воздуха равно 1,4.
Теплоемкость газов. Взаимосвязь между Сv и Ср. Уравнение Майера. Коэффициент Пуассона.
Средняя
массовая теплоемкость паров бензола в
пределах температур 85 – 115о
С ( при
нормальном атмосферном давлении ) равна
1,257 кДж / кг·К. Вычислить средние
теплоемкости бензола при постоянных
давлении и объеме, и их соотношение Ср
/ С v.
Что такое тепловой эффект реакции? Изохорный и изобарный тепловой эффект. Определить тепловой эффект реакции:
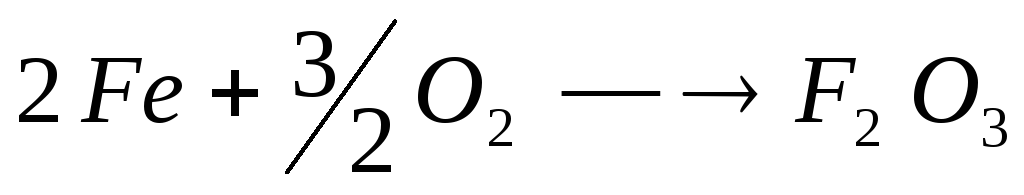
при постоянном объеме и 180С, если изобарный термохимический тепловой эффект этой реакции при той же температуре равен 823,З кДж/моль.
Зависимость теплового эффекта реакции от температуры. Закон Кирхгофа.
Закон Гесса и следствия из него. Значение закона Гесса.
Определить тепловой эффект реакции этерификации между этиловым спиртом и уксусной кислотой, если теплота сгорания спирта равна 1374 кДж/молъ, уксусной кислоты 871,6 кДж/моль и полученного эфира 2256 кДж/моль.
Что называется теплотой образования? Как определяется теплота образования неорганических веществ?
Определить теплоту сгорания фосфористого водорода, используя следующие данные:
2Р + 3Н2 2 РН3 – 48,69 кДж/моль
2Р + 5/2 О2 Р2О5 + 1508,4 кДж/моль
Н2 + ½ О2 Н2О + 285,0 кДж/моль
Как рассчитывается теплота образования органических веществ? Что такое стандартные условия?
Определить теплоту сгорания этилового спирта, используя следующие данные:
С + О2 СО2 + 391,0 кДж/моль
Н2 + ½ О2 Н2О + 285,0 кДж/моль
2С + 3Н2 + ½ О2 С2 Н5 ОН + 278,2 кДж/моль
Что называется теплотой сгорания? Как определяется теплота сгорания веществ и при каких условиях?
Определить теплоту образования нафталина, при постоянном давлении и 180С используя следующие данные:
С10Н8 (тв.) + 12 О2 10 СО2 + 4 Н2О + 5162 кДж/моль
С + О2 СО2 + 391,0 кДж/моль
Н2 + ½ О2 Н2О + 285,0 кДж/моль
Содержание и формулировки второго закона термодинамики, его физическая сущность.
Основной термодинамический цикл - цикл Карно, его КПД.
Рассчитать к. п. д. идеальной машины Карно, получающей пар при 240° С и выпускающей его при 205° С.
Энтропия: физический смысл, значение, характеристика.
Определить разность энтропии 1 г воды при 0 и 100°С (давление нормальное), считая теплоемкость воды постоянной и равной 4,19 дж/г-град.
Свободная энергия системы. Изобарно-изотермический и изохорно-изотермический потенциалы (энергии Гиббса и Гельмгольца).
Определить возможность протекания реакции: 2H2S(г) + 302 = 2Н2О + 2S02 (г) в стандартных условиях и при температуре 500 К. Для расчета воспользоваться табличными значениями ∆Н° и S°.
Термодинамика пара. Стадии получения и применение перегретого водяного пара.
Что называется цепной реакцией? Каковы ее стадии? Механизм цепной реакции.
Роль цепных реакций в органической химии и нефтехимии. Взрывные процессы.
Что называется скоростью химической реакции? Графическая зависимость скорости реакции от времени для обратимой и необратимой реакций (график пояснить).
Во сколько раз увеличится скорость реакции: 2 NO+ О2= 2 NО2 ,
протекающей в закрытом сосуде, если увеличить концентрацию оксида азота (II) в три раза без изменения температуры?
Зависимость скорости реакции от температуры. Уравнение Аррениуса и его практическое применение.
Константа скорости реакции инверсии тростникового сахара при 25°С равна 9,6710 -3,а при 40°С – 73,410 –3 мин -1. Определить константу скорости этой реакции при 35°С.
Температурный коэффициент скорости химической реакции и его практическое применение.
Во сколько раз увеличится время, необходимое для завершения реакции, если понизить температуру на 45°C? Температурный коэффициент принять равным 3.
Молекулярность и порядок реакций. Вывести кинетическое уравнение реакций 1-го порядка.
Период полураспада радиоактивного изотопа азота равен 9,93 мин. Определить, сколько процентов и какая часть азота разложится в течение 50 мин.
Энергия активации и ее физический смысл (привести рисунок и пояснить). Что такое активация? Методы активации молекул.
Константа скорости реакции инверсии тростникового сахара при 250С равна 9,6710 –3, а при 400С – 7,3410 –2. Определить энергию активации.
Химическое равновесие. Обратимые и необратимые реакции. Закон действия масс. Сформулировать принцип Ле Шателье и пояснить его на конкретных примерах.
Даны реакции:
2 SO2 + O2 2 SO3 + 176,8 кДж
CO2 + С 2 СО – 160,5 кДж
Какими факторами можно сдвинуть равновесие этих реакций вправо?
Вывести константу равновесия КС и КР для гомогенной реакции. Вывести взаимосвязь между константами равновесия КС и КР.
Константа равновесия Кс реакции: SO2 +Сl2 SO2Сl2
при 92° С равна 15,43. Определить значение Кр при данной температуре.
Химическое сродство. Уравнение изотермы химической реакции и его практическое применение для определения направления процесса.
Вычислить константу равновесия реакции: СО2 + Н2 ↔ СО + Н2О(г)
при 25° С и нормальном атмосферном давлении, используя табличные значения термодинамических функций при стандартных условиях. В каком направлении может протекать реакция при заданных условиях?
Уравнение изохоры и его практическое применение для определения смещения равновесия при изменении внешних условий.
Найти соотношение констант равновесия при Т1=500 К и Т2= 600 К для реакции:
2 СО+ O2 2 CO2 ,
если изохорный тепловой эффект этой реакции составляет 16,8 кДж.
Уравнение изобары и его практическое применение для определения смещения равновесия при изменении внешних условий.
Константа равновесия Кр при 700 К равна 5,4∙ 10-12 для системы:
N2 + ЗН2 ↔ 2NH3 + 92,51 кДж.
Определить Кр при 850 К.
Катализ и автокатализ. Особенности каталитических реакций. Положительный и отрицательный катализ. Роль каталитических процессов в нефтепереработке и нефтехимии.
Гомогенный и гетерогенный катализ. Специфичность каталитических реакций.
Фаза, компонент, число степеней свободы.Правило фаз Гиббса.
Определить число степеней свободы в системе, содержащей насыщенный водный раствор глюкозы, кристаллы глюкозы и насыщенный водяной пар при постоянном давлении.
Термический анализ / построение диаграммы плавкости по кривым охлаждения/.
Привести диаграмму состояния воды и разобрать ее с точки зрения правила фаз.
Привести диаграмму состояния серы и разобрать ее с точки, зрения правила фаз.
Привести диаграмму состояния 2-х компонентной конденсированной системы и разобрать ее с точки зрения правила фаз.
Гидратная теория растворов Менделеева.
Какова концентрация в масс. долях 4,05 н. раствора НС1, плотность которого 1,08 г/см3?
Осмос.
Найти молекулярную массу мочевины, если водный раствор, содержащий 0,368г мочевины в 2ОО см3 имеет осмотическое давление 74630 Н/м2
Закон Вант-Гоффа для не электролитов и электролитов. Для чего вводится изотонический коэффициент в уравнение Вант - Гоффа?
Найти осмотическое давление раствора сахарозы при 0С, если при 20С осмотическое давление этого же раствора равно 1,066 105 Па.
Закон Рауля.
Сколько г глицерина необходимо растворить в 90 г воды при 30С, чтобы понизить давление пара на 266,5 Н/м2?
Первый закон Коновалова, его графическое изображение. Перегонка жидких смесей, подчиняющихся этому закону.
Криоскопия.
При какой температуре будет замерзать 45%-ный раствор метилового спирта в воде?
Эбулиоскопия.
Сколько г глюкозы нужно добавить к 100 г воды, чтобы раствор закипел при 102,5 ° С?
Второй закон Коновалова, его графическое изображение. Перегонка жидких смесей, подчиняющихся этому закону.
Перегонка с водяным паром.
При 95°С давление пара нафталина равно 2066 Па. Какое количество дистиллята необходимо собрать, перегоняя нафталин с водяным паром, чтобы получить 20 г чистого нафталина, если давление паров воды при указанной температуре равно 84512,9 Па .
Две несмешивающиеся жидкости. Закон распределения.
Коэффициент распределения нормальной масляной кислоты между хлороформом и водой равен 0,52 при температуре 25°С . Сколько масляной кислоты можно извлечь из 100 см 3 0,5М раствора масляной кислоты в хлороформе при встряхивании его однократно со 100 см 3 и при четырехкратном встряхивании, используя каждый раз по 25 см 3 воды?
Экстракция из растворов/ привести формулу и пояснить/.
Удельная и эквивалентная электропроводности. Их взаимосвязь.
Удельная электрическая проводимость 0,509 н КСl при 18°С 4,54 См/м. Вычислить кажущуюся степень диссоциации KCl в данном растворе.
Опытное определение удельной электропроводности электролитов.
Сопротивление раствора сульфата натрия в электролитическом сосуде 26,86 Ом. Вычислить удельную электрическую проводимость раствора, если площадь электродов 5,38 см2, а расстояние между ними 0,82 см.
Что такое гальванический элемент? Принцип работы элемента Якоби.
При 25°С потенциал медного электрода, погруженного в раствор с активностью ионов меди 0,0202 равен 0,29 В. Вычислить нормальный электродный потенциал меди по отношению к нормальному водородному электроду.
Принцип работы концентрационной и окислительно-восстановительной цепи.
Водородный электрод. Каломельный электрод.
Определить ЭДС гальванического элемента при 25 С
(- ) Са Са SО 4 Zn SО 4 Zn (+)
0,1 М 0,2 М
Определение ЭДС элемента и электродного потенциала.
0пределить ЭДС гальванического элемента при 25°:
(+) Аg Аg NО 3 Рв ( N О 3) 2 Р в (-)
0 ,1 М 0,005 М
Кажущаяся степень диссоциации Рв(NО3)2равна 75 % , а для АgNО3– 81%.
Электролиз. Законы Фарадея.
Сколько меди выделиться при электролизе раствора медного купороса, если пропускать ток в 0,2 А в течение 1 часа 25 мин .и при выходе по току в 90%?
Слабые электролиты. Закон разбавления Оствальда и условия его применения.
Эквивалентная электрическая проводимость для раствора уксусной кислоты при 18°С и разведении 32 М /кг-экв равна 0.82 Смм 2 кг-экв –1 . Вычислить константу диссоциации КСl .
Коррозия металлов и методы защиты от коррозии.
Поверхностные явления и адсорбция. Количественная характеристика адсорбции, её виды.
Адсорбция на поверхности твердого тела. Изотерма адсорбции. Уравнение Фрейндлиха и Ленгмюра.
Построение изотермы адсорбции по экспериментальным данным
Хроматография.
Дисперсные системы. Основные признаки дисперсных систем, их классификация.
Методы получения коллоидных растворов
Строение коллоидных мицелл.
Золь бромида серебра получен смешиванием 25см3 0,008 н КВг и 18см3 0,0096н AgNO3. Определить знак заряда частиц и составить формулу мицеллы золя.
Устойчивость коллоидных растворов. Коагуляция.
Оптические свойства коллоидных растворов.
Золь серы был получен путем добавления 5 мл раствора серы в спирте к 10 мл дистиллированной воды. Каким методом получен данный золь? Какую окраску имеет данный золь в проходящем и отраженном свете и чем объясняется разная окраска?
Кинетические и электрокинетические свойства коллоидных растворов.
Эмульсии. Получение эмульсий, их типы. Обращение фаз эмульсий. Деэмульгирование.
Пены, аэрозоли, суспензии.
Общая характеристика растворов ВМС. Определение молекулярной массы ВМС.
