
- •Раздел 1. Введение в курс биохимии Лекция 1. Введение в дисциплину
- •1. Предмет и задачи биохимии
- •2. Краткая история развития биохимии
- •3. Основные биополимеры и их мономеры
- •4. Общая характеристика метаболических процессов
- •Раздел 2. Белковые вещества Лекция 2. Общая характеристика белков и аминокислот. Строение, классификация и свойства аминокислот
- •1. Общая характеристика аминокислот
- •2. Классификация протеиногенных аминокислот
- •3. Биологическая роль аминокислот
- •4. Уровни организации белковых молекул (структура белков)
- •Биологический смысл образования четвертичной структуры
- •5. Классификация белков
- •Лекция 3. Основные свойства белков и методы разделения белков и аминокислот
- •1. Основные свойства белков
- •2. Выделение белков из биологического материала
- •3. Методы разделения белков и аминокислот
- •4. Определение первичной структуры белка
- •Раздел 3.Нуклеотиды и нуклеиновые кислоты Лекция 4. Строение и функции нуклеотидов
- •1. Общая характеристика нуклеотидов
- •2. Строение и функции моно- и динуклеотидов
- •3. Строение и функции нуклеиновых кислот
- •4. Основные биохимические функции нуклеотидов
- •Раздел 4.Ферменты Лекция 5. Строение, механизм действия и классификация ферментов
- •1. Строение и основные свойства ферментов
- •2. Механизм действия ферментов
- •3. Номенклатура и классификация ферментов
- •4. Кинетика ферментативных реакций
- •5. Регуляция ферментативных процессов в клетке
- •Ингибирование
- •Раздел 5.Углеводы и их обмен Лекция 6. Химическое строение и свойства углеводов
- •1. Общая характеристика и классификация углеводов
- •2. Строение, свойства и функции моносахаридов
- •3. Строение, свойства и функции олигосахаридов
- •4. Строение, свойства и функции полисахаридов
- •5. Углеводы зерна и продуктов его переработки
- •Лекция 7. Основные пути распада и синтеза углеводов. Гликолиз и брожение
- •1. Процессы распада олиго- и полисахаридов
- •Фосфоролиз
- •Гидролиз
- •2. Синтез олиго- и полисахаридов
- •3. Анаэробные процессы расщепления моносахаридов. Гликолиз
- •4. Брожение и его основные типы
- •Молочнокислое брожение
- •Молочнокислое брожение у аэробных организмов
- •Маслянокислое брожение
- •Лекция 8. Аэробное дыхание
- •2. Окислительное декарбоксилирование пирувата (пвк)
- •Следует отметить, что в результате реакции окисления пвк в образующейся молекуле ацетилкоэнзима а возникают макроэргические связи, которые способствуют его энергетическому обмену в дальнейшем.
- •3. Цикл Кребса (цикл ди- и трикарбоновых кислот, цикл лимонной кислоты)
- •4. Окислительное фосфорилирование
- •Лекция 9. Фотосинтез как основной источник органических веществ на Земле
- •1. Значение фотосинтеза
- •2. Общие представления о химизме фотосинтеза
- •3. Характеристика фотосинтетического аппарата
- •4. Световая фаза фотосинтеза
- •5. Темновая фаза фотосинтеза
- •Раздел 6.Липиды и их обмен Лекция 10. Классификация липидов, их свойства и биологическая роль
- •1. Классификация липидов
- •2. Характеристика основных групп липидов Жирные кислоты
- •Нейтральные жиры
- •Фосфолипиды
- •Стероиды
- •Терпены
- •3. Основные функции липидов
- •4. Липиды зерна и продуктов его переработки
- •В зерне пшеницы около 30% всех липидов составляют липиды, связанные с белками и углеводами, и не экстрагируемые диэтиловым эфиром.
- •В зерне пшеницы, ржи и ячменя содержится в среднем 2% жира. В зерне овса жира несколько больше – около 5%. Именно поэтому овсяные мука и крупа очень легко прогоркают при хранении.
- •Лекция 11. Обмен липидов
- •1. Катаболизм (распад) триацилглицеринов
- •Гидролитическое расщепление триацилглицеринов
- •Катаболизм жирных кислот
- •Катаболизм глицерина
- •2. Синтез жирных кислот и триацилглицеринов Синтез жирных кислот
- •Биосинтез триацилглицеринов
- •3. Обмен фосфолипидов
- •Раздел 7. Витамины и минеральные вещества Лекция 12. Характеристика витаминов и минеральных веществ и их роль в организме человека
- •1. Особенности биологического действия витаминов
- •2. Классификация витаминов
- •3. Патологии, вызванные избытком или недостатком витаминов
- •4. Витамины зерна и продуктов его переработки
- •5. Общая характеристика минеральных веществ и их роли в организме человека
- •Раздел 8.Обмен азота Лекция 13.Ферментативный распад и синтез белков
- •1. Распад белков
- •2. Синтез белков (реализация наследственной информации)
- •Репликация днк
- •Транскрипция
- •Трансляция
- •Лекция 14.Ферментативный распад и синтез аминокислот
- •1. Пути превращения аминокислот
- •2. Распад аминокислот
- •Декарбоксилирование
- •Дезаминирование
- •2. Биосинтез аминокислот
- •Раздел 9.Взаимосвязь между процессами обмена
- •2. Основные этапы катаболизма и анаболизма Этапы катаболизма
- •Этапы анаболизма
- •3. Регуляция биохимических процессов
- •4. Особенности гормональной регуляции Химическая структура гормонов
- •Особенности биологического действия гормонов
- •5. Основные принципы регуляции биохимических процессов
- •Раздел 10.Роль биохимических процессов при
- •2. Биохимические процессы, происходящие при прорастании и созревании зерна
- •3. Биохимические процессы, происходящие при хранении продовольственного сырья
- •4. Роль биохимических процессов в переработке продовольственного сырья
4. Определение первичной структуры белка
Наиболее ответственной процедурой при установлении первичной структуры белков является определение последовательности аминокислотных остатков. В настоящее время эту работу ведут преимущественно либо фенилизотиоцианатным методом Эдмана.
Метод Эдмана реализуется в специально созданном для этой цели приборе, получившем название секвенатор (от sequence – последовательность). Метод Эдмана сводится к обработке фенилизотиоцианатом белка или пептида, присоединенного через С-концевую аминокислоту к инертному носителю (полистиролу или пористому стеклу) в колонке секвенатора. После промывки колонки растворителями (метанол, дихлорэтан) образовавшийся фенилтиокарбамилпептид подвергают воздействию безводной трифторуксусной кислоты, в результате чего высвобождается анилинотиозолинон и в его составе N-концевая аминокислота, а укороченный на один аминокислотный остаток пептид или белок остается связанным с носителем.
Раздел 3.Нуклеотиды и нуклеиновые кислоты Лекция 4. Строение и функции нуклеотидов
1. Общая характеристика нуклеотидов
Нуклеотиды – сложные органические вещества, состоящие из 3-х обязательных компонентов:
азотистого основания;
пятиуглеродного сахара;
остатка фосфорной кислоты.
Сложные органические соединения, состоящие только из азотистого основания и сахара-пентозы, называются нуклеозидами. Следовательно, нуклеотиды – фосфорнокислые эфиры нуклеозидов.
Азотистые основания
Азотистые основания являются производными двух гетероциклических соединений – пурина и пиримидина:
пуриновые азотистые основания:


Аденин Гуанин
пиримидиновые азотистые основания:



Урацил Цитозин Тимин
Пятиуглеродные сахара:


β-рибоза β-дезоксирибоза
Фосфорная кислота

В состав нуклеотидов обязательно входит остаток фосфорной (ортофосфорной) кислоты.
Помимо указанных выше трех обязательных компонентов, в состав молекул нуклеотидов могут входит и другие функциональные группы.
При образовании нуклеозидов первый атом рибозы (дезоксирибозы) связывается с N-1 атомом пиримидинового или N-9 атомом пуринового основания.
С рибозой соединяются аденин, образуя аденозин; гуанин, образуя гуанозин; цитозин, образуя цитидин; урацил, образуя уридин.
С дезоксирибозой соединяются аденин, гуанин, цитозин и тимин, образуя соответственно дезоксиаденозин, дезоксигуанозин, дезоксицитидин, тимидин.
Наиболее распространено в природе присоединение по 5 положению сахара и оно не указывается.
В организме нуклеотиды являются мономерами нуклеиновых кислот, либо функционируют самостоятельно. В зависимости от того, в каком количестве в нуклеотидах представлены их основные компоненты, все нуклеотиды подразделяют на мононуклеотиды, динуклеотиды и полинуклеотиды (полинуклеиновые кислоты).
2. Строение и функции моно- и динуклеотидов
Моно- и динуклеотиды не входят в состав нуклеиновых кислот; они функционируют самостоятельно. В состав самостоятельных нуклеотидов в качестве сахара всегда входит рибоза.
К мононуклеотидам относятся АТФ, АДФ, АМФ, коэнзим А и другие нуклеотиды.
АТФ – аденозинтрифосфорная кислота:

АТФ – энергетический эквивалент клетки, она является посредником между реакциями, идущими с выделением энергии (экзергоническими) и реакциями, идущими с поглощением энергии (эндергоническими). Иными словами, в форме АТФ клеткой запасается энергия, которая затем используется для процессов жизнедеятельности.
Химические связи между различными атомами в органических соединениях делятся на 2 типа:
нормальные
макроэргические
Нормальные связи – связи, при возникновении или распаде которых изменение уровня свободной энергии соединений составляет 12,5 Дж/моль.
Макроэргические связи – связи, при возникновении или распаде которых уровень свободной энергии соединения составляет 25-50 кДж/моль вещества.
Понятие «макроэргическая связь» учитывает энергетический эффект преобразованной связи посредством химической реакции вещества с нормальными свойствами.
Связи между остатками фосфорной кислоты являются макроэргическими – при их гидролизе выделяется энергия. Такие связи принято обозначать волнистой черточкой.
Энергия 1-й молекулы АТФ может служить только для 1-й реакции. АДФ и АМФ – не способны быть источником энергии.
В живых клетках имеются 3 способа образования АТФ:
Субстратное фосфорилирование.
Окислительное фосфорилирование.
Фотосинтетическое фосфорилирование.
Коэнзим А (КоА). КоА является переносчиком ацильных групп; участвует во многих процессах. В его состав входит аденин, рибоза, пирофосфат, пантотеновая кислота (витамин В3) и тиоламин. Упрощенно коэнзим А представляют в виде следующей формулы: HS-KoA. При взаимодействии коэнзима А с уксусной кислотой образуется ацетилкоэнзим А, в молекуле которого появляется макроэргическая (высокоэнергетическая):

Ацетилкоэнзим А
Ацетилкоэнзим А является ключевым метаболитом, благодаря которому осуществляется не только распад и синтез различных веществ, но и взаимосвязь между процессами обмена белков, липидов и углеводов.
К динуклеотидам относятся НАД, НАДФ, ФАД и др.
НАД – никотинамидадениндинуклеотид;
НАДФ – никотинамидаденин динуклеотид фосфат.
В состав этих динуклеотидов входит никотинамид (амид никотиновой кислоты, являющееся важным витамином - витамином В5). Молекула НАДФ идентична по структуре НАД с той лишь разницей, что у НАДФ у С-3 атома рибозы ОН-группа замещена остатком молекулы фосфорной кислоты.
Молекулы НАД и НФДФ способны к обратимому окислению и восстановлению (благодаря окислительно-восстановительной способности никотинамида), поэтому они участвуют в качестве переносчиков водорода; в реакциях биологического окисления НАД и НАДФ являются кофакторами ферментов дегидрогеназ.
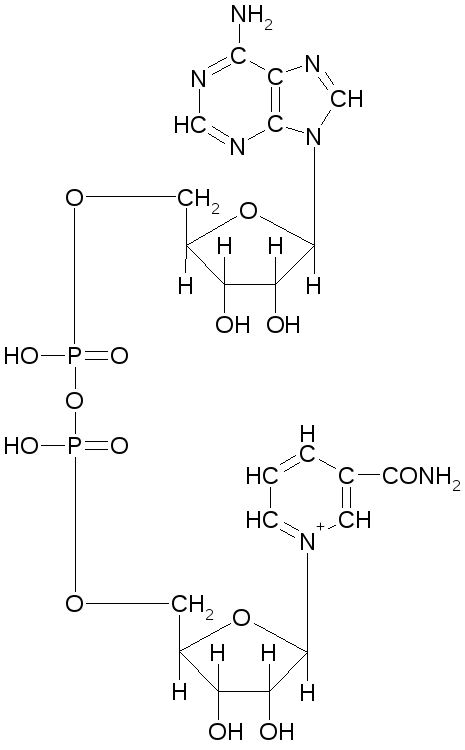
Структура НАД (окисленная форма)
ФАД – флавинадениндинуклеотид. В его состав входит рибофлавин (витамин В2).

Структура ФАД (окисленная форма)
ФАД, как и другие динуклеотиды, способен обратимо окисляться и восстанавливаться, присоединяя к своей молекуле 2 атома водорода, поэтому он участвует в биологическом окислении в качестве переносчика водорода. Является кофактором дегидрогеназ, так же, как и НАД и НАДФ.
