
- •Министерство образования и науки российской федерации
- •Рецензент:
- •6. Теоретические основы современных методов контроля качества продовольственных товаров
- •6.1. Оптические методы
- •6.1.1. Электромагнитное излучение
- •6.1.2. Происхождение атомных спектров
- •6.1.3. Классификация оптических методов анализа
- •Вопросы для самоконтроля
- •6.2. Поглощение излучения
- •6.2.1. Ультрафиолетовая и видимая области
- •6.2.2. Цвет раствора
- •6.2.3. Фотометрические методы анализа
- •6.2.4. Спектрофотометрия
- •Характеристические полосы поглощения некоторых хромофоров
- •6.2.5. Инфракрасная спектроскопия
- •Вопросы для самоконтроля
- •6.3. Молекулярная люминесценция: флуориметрия, фосфорометрия
- •Вопросы для самоконтроля
- •6.4. Спектры комбинационного рассеяния (Рамановская спектроскопия)
- •Вопросы для самоконтроля
- •6.5. Атомная спектроскопия
- •Конус зона
- •Вопросы для самоконтроля
- •6.6. Фотоакустическая спектроскопия
- •Вопросы для самоконтроля
- •6.7. Рентгено-спектральный анализ
- •Вопросы для самоконтроля
- •6.8. Электронная и ионная спектроскопия
- •Вопросы для самоконтроля
- •6.9. Спектроскопия магнитного резонанса (Радиочастотные спектральные методы)
- •Вопросы для самоконтроля
- •6.10. Масс-спектрометрия
- •Вопросы для самоконтроля
- •6.11. Ядерно-физические методы анализа
- •6.11.2. Величины и единицы измерения радиоактивности
- •6.11.3. Α-распад
- •6.11.4. Β-превращения
- •6.11.5. Γ-излучение
- •6.11.6. Детекторы радиоактивности
- •Вопросы для самоконтроля
- •6.12. Термические свойства потребительских товаров
- •6.12.1. Термические методы анализа
- •6.12.2. Термометрия
- •6.12.3. Термотитрометрия
- •6.12.4. Термогравиметрический анализ (тга)
- •6.12.5. Дифференциальный термический анализ (дта)
- •6.12.6. Дифференциальная термогравиметрия (тгп)
- •6.12.7. Дифференциальная сканирующая калориметрия (дск)
- •Вопросы для самоконтроля
- •6.13. Цвет и свет
- •6.13.1 Основные колориметрические и фотометрические величины
- •6.13.2 Основы измерения цвета
- •Вопросы для самоконтроля
- •6.14. Микроскопия
- •Примерные диапазоны применения различных методов исследования растительных объектов
- •Вопросы для самоконтроля
- •6.15. Хроматографические методы разделения и идентификации веществ
- •Важнейшие виды хроматографии
- •Вопросы для самоконтроля
- •7. Статистическая обработка результатов измерения
- •Оценка правильности результатов измерений(определений)
- •Оформление контрольной работы
- •Контрольная работа
- •Тематика рефератов (по указанию преподавателя)
- •Рекомендованная литература
6.1.2. Происхождение атомных спектров
При изменении хотя бы одного квантового числа атом получает или отдает энергию. Это может произойти при взаимодействии атома с ЭМИ, при непосредственном обмене энергией с другими атомами, например, при столкновениях или при химических реакциях. В отсутствии внешних воздействий атом находится в основном состоянии, т.е. обладает наименьшей энергией. При получении энергии извне атом возбуждается.
Е3
Е2
i

Е1
k
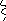

Е0
Рис. 11. Энергетические переходы в атоме
Атом не может получить или отдать любое количество энергии. Энергетический обмен осуществляется только конечными порциями, в частности квантами ЭМИ, т.е. атом может находится друг от друга на конечную величину.
Один атом за один акт поглощает или испускает только один фотон с определенной энергией. Вещество состоит из множества одинаковых атомов, способных переходить на разные энергетические уровни, выпуская или поглощая кванты разных частот. Совокупность всех фотонов одной и той же частоты составляет спектральную линию, при поглощении ее называют абсорбционной, при испускании - эмиссионной. Совокупность всех абсорбционных или всех эмиссионных линий называют абсорбционным или эмиссионным спектром вещества.
Спектр поглощения получают, помещая исследуемое вещество в поток ЭМИ, а для получения спектра испускания атомы вещества предварительно переводят в возбужденное состояние, что достигается подведением какой-либо энергии (тепловой, химической, электроразряда и т.п.). После возбуждения атомы через 10-9 – 10-7с возвращаются в основное состояние, испуская фотоны.
Частота испускаемого или поглощаемого излучения определяется разностью энергии между электронными орбиталями ΔЕ:
V =ΔE/h
Внешние легковозбудимые электроны называют оптическими, переходы с их участием дают оптический спектр. Наиболее вероятны переходы с первого возбужденного уровня на основной Е0, соответствующие им спектральные линии называют резонансными. Поскольку интенсивность линии пропорциональна числу фотонов в секунду, то более частым переходам соответствует интенсивная линия, а редким - менее интенсивная. Наиболее интенсивны резонансные линии, так как вероятность перехода Е1→Е0 очень велика.
Испускание - самопроизвольный процесс, так как атом всегда стремится перейти из нестабильного состояния, возбужденного, в более стабильное состояние с меньшей энергией. Поглощение - вынужденный процесс, увеличивающий энергию атома за счет поглощаемого фотона.
6.1.3. Классификация оптических методов анализа
Методы анализа, основанные на изменениях энергетического состояния атомов веществ входят в группу оптических (атомно-спектроскопических методов), различающихся по способу получения и регистрации аналитического сигнала.
Оптические методы анализа (ОМА) используют энергетические переходы внешних электронов (валентных). Общим для них является необходимость предварительной атомизации (разложение на атомы) вещества.
Атомно-эмиссионная спектроскопия основана на испускании излучения атомами, возбужденными кинетической энергией плазмы, дугового или искрового разряда и т.п.
Атомно-флуоресцентная спектроскопия использует испускание излучения атомами, возбужденными электромагнитным излучением от внешнего источника.
Атомно-абсорбционная спектроскопия основана на поглощении атомами излучения от внешнего источника.
Рентгеновские методы основаны на энергетических переходах внутренних электронов атомов. В зависимости от способа получения и регистрации сигнала различают рентгеноэмиссионную, рентгеноабсорбционную, рентгенофлуоресцентную спектроскопию и их разновидности (электронная спектроскопия, электронно-зондовый анализ и др.). Используют их в основном для исследования строения вещества. Рентгеновские методы не требуют атомизации вещества и позволяют исследовать твердые пробы без их предварительной подготовки.
Ядерные методы основаны на возбуждении ядер атомов. По происхождению аналитического сигнала различают следующие молекулярно-спектроскопические методы: абсорбционная молекулярная спектроскопия основана на энергетических переходах валентных электронов, сигналы от которых проявляются в видимой и УФ-областях. Абсорбционная молекулярная спектроскопия в ИК-области основана на колебательных переходах, сигналы от которых проявляются в области от 800нм до 10 или в приемлемых единицах от 2,5мкм до 40мкм.
Люминесцентная спектрометрия базируется на испускании излучения после возбуждения молекул светом.
Магнитная резонансная спектрометрия основана на получении сигналов от молекул, помещенных в магнитное поле.
Фотоакустическая спектрометрия основана на измерении теплоты, выделяемой при безизлучательных переходах.
Рентгеновская спектроскопия основана на возбуждении внутренних электронов молекулы.
