
Архит._материал._-_Шеина_Ч1
.pdf
Министерство образования и науки РФ Федеральное государственное бюджетное образовательное
учреждение высшего профессионального образования «Самарский государственный архитектурно-строительный университет»
Т.В. Шеина
АРХИТЕКТУРНОЕ
МАТЕРИАЛОВЕДЕНИЕ
Учебное пособие
Часть I
Самара 2011
1
УДК 691:72.02 (075.8)
Шеина, Т.В. Архитектурное материаловедение: учебное пособие / Т.В. Шеина; Самарск. гос. арх.-строит. ун-т. – Самара, 2011. – 360 с.
ISBN
В первой части учебного пособия изложены основы архитектурного материаловедения, показана взаимосвязь элементного, химикоминералогического, фазового и вещественного состава, макро-, микро- и ультрамиктроструктуры и функциональных свойств строительных материалов. Кратко описаны основные и декоративные свойства горных пород и природных каменных материалов, древесины, материалов и изделий на ее основе, декора- тивно-облицовочной и конструкционной керамики и стекла, а также металлов и сплавов, применяемых в строительстве, архитектуре и дизайне.
Включены новейшие данные о нанообъектах, наноматериалах и области их применения в строительстве, архитектуре и дизайне. Приведены сведения о традиционных, умных и интеллектуальных композитах.
Предназначено для студентов специальности 290100 «Архитектура», дисциплина «Архитектурное материаловедение» (I курс, II семестр).
Табл. 65. Ил. 285. Библиогр.: 43 назв.
Печатается по решению редакционно-издательского совета университета
Рецензенты: проф., д.т.н. Н.Г. Чумаченко проф., д.т.н. А.И. Хлыстов
Редактор |
Г.Ф. Коноплина |
|
Учебное издание |
Пописано в печать 06.09. 2011 г. Формат 60х84 1/16. |
|
Бумага офсетная. Печать оперативная. |
|
Уч.-изд.л. |
. Усл. печ. л. . Тираж 100 экз. |
443001 Самара, ул. Молодогвардейская, 194 Самарский государственный архитектурно-строительный университет.
ISBN |
© Самарский государственный архитектурно- |
|
строительный университет, 2011 |
|
© Шеина, Т.В. 2011 |
2
ОГЛАВЛЕНИЕ
1 Основы архитектурного материаловедения………………………………5
2 Взаимосвязь состава, структуры и свойств строительных материалов…………………………………………………..5
2.1Элементный, химико-минералогический, фазовый
ивещественный составы материалов…………………………….5
2.2Макро-, микро- и ультрамикроструктура материалов…..….…..11
2.3Пространственные решетки кристаллов………………….……….18
2.4Дефекты строения в кристаллах……………………………………22
3 Механические свойства строительных материалов………………….…25
3.1Прочность и ее разновидности……………………………………..25
3.2Динамическая, длительная и усталостная прочность…….………29
3.3Деформационные характеристики…………………………………30
3.4Твердость…………………………………………………………….32
3.5Истираемость и износ……………………………………………….34
4 Физические свойства материалов.…………………………………………36
4.1Параметры физические состояния………………………………….36
4.2Структурные характеристики……………………………………....37
4.3Поверхностные свойства…………………………………………….39
4.4Гидрофизические свойства…………………………………………..41
4.5Теплофизические свойства…………………………………………..47
4.6Химические свойства………………………………………………...51
4.7Дисперсные системы…………………………………………………54
5 Технологические свойства материалов.…………………………………..56
6 Декоративные свойства материалов………………………………………57
7 Композиционные материалы……………………………………………….62
7.1Классификация композиционных материалов……………………...62
7.2Состав и строение композита………………………………………...64
7.3Оценка матрицы в формировании свойств композита……………..68
7.4Композиционные материалы на основе органической матрицы………………………………………………..70
7.5Композиционные материалы на основе неорганической матрицы……………………………………………..76
8Наноматериалы в строительстве и архитектуре………………………....88
8.1Нанообъекты и область их применения……………………………..90
8.2Диагностика наноматериалов……………………………………….104
9Материалы, получаемые обработкой камня……………………………109
9.1Краткие сведения из геологии.
Понятие о минералах и горных породах…………………………...109
9.2Состав и свойства породообразующих минералов………………..111
9.3Генетическая классификация горных пород……………………….116
9.4Поделочные камни.……………………………………………….…124
9.5Монументальный камень……………………………………………126
9.6Месторождения облицовочного камня в России…………………...127
9.7Основные критерии оценки горных пород как
3
декоративно-облицовочного камня…………………………………128
9.8Обработка и область применения декоративного камня………….135
9.9Способы предохранения камня от коррозии……………………….141
9.10Камнеобрабатывающие оборудование
исопутствующие материалы……………………………………….143
10 Лесоматериалы………………………………………………………….….146
10.1Классификация основных пород древесины……………………….147
10.2Строение и состав древесины………………………………….…….146
10.3Химические, физические и механические
свойства древесины…………………………………………….……152
10.4Пороки древесины……………………………………………………165
10.5Материалы и изделия из древесины………………………………...169
11 Архитектурно-строительная керамика………………………………...199
11.1История керамики……………………………………………………199
11.2Сырьевые материалы и их свойства………………………………...209
11.3Производство керамических изделий……………………………….216
11.4Классификация керамических материалов
иизделий……………………………………………………………...222
12 Стекло в архитектуре и дизайне………………………………………...239
12.1История стекла………………………………………………………..239
12.2Технология получения стекла.…………..…..………………………246
12.3Производство стеклянных изделий…………………………………250
12.4Свойства стекла………………………………………………………263
12.5Декоративные материалы из стекла………………………………...267
12.6Функциональные покрытия на листовом стекле…………………...279
12.7Конструкционные стеклоизделия…………………………………...289
13Металлы и сплавы ………………………………………………….……..295
13.1История металлов…………………………………………………….295
13.2Общие сведения и классификация…………………………………..311
13.3Атомно-кристаллическое строение металлов………………………316
13.4Диаграмма состояния железо – цементит
вфазовом виде……………………………………………………….317
13.5Свойства металлов и сплавов……………………………………….321
13.6Виды чугунов………………………………………………………...325
13.7Производство чугуна………………………………………………...329
13.8Виды сталей…………………………………………………….…….330
13.9Производство стали………………………………………………….346
13.10Коррозия металлов и способы защиты……………………………349
13.11Способы обработки металлов……………………………………..350
13.12Цветные металлы…………………………………………….…..…361
13.13Сплавы цветных металлов…………………………………………367 Библиографический список……………………………………………….……373
4
1 ОСНОВЫ АРХИТЕКТУРНОГО МАТЕРИАЛОВЕДЕНИЯ
Любая конструкция воспринимает те или иные нагрузки и подвергается действию окружающей среды.
Нагрузки вызывают деформации и внутренние напряжения в материале, поэтому проектирование зданий и сооружений требует точных характеристик прочностных и деформационных свойств, называемых механическими свой-
ствами.
Кроме прочности, строительные материалы должны обладать стойкостью, т.е. способностью сопротивляться физическим и химическим воздействиям среды: воздуха и содержащихся в нем паров воды и газов, воды и растворенных в них веществ, колебаниям температуры и влажности, совместному действию воды и мороза при многократном замораживании и оттаивании.
Исходя из условий работы материала в зданиях и сооружениях, строительные материалы можно разделить по назначению на две основные группы.
Первую группу составляют материалы универсального типа, пригодные для несущих конструкций: искусственные каменные материалы, получаемые на основе вяжущих веществ без обжига (бетоны, строительные растворы) и обжигом минерального сырья (керамика, стекло, ситаллы, металлы); конструкционные пластмассы; лесные и природные каменные материалы.
Вторая группа объединяет строительные материалы специального назначения, необходимые для защиты конструкций от вредных влияний окружающей среды и для повышения эксплуатационных характеристик зданий и сооружений, а также для создания комфорта: теплоизоляционные и акустические; гидроизоляционные, кровельные и герметизирующие; отделочные и антикоррозионные материалы.
2 ВЗАИМОСВЯЗЬ СОСТАВА, СТРУКТУРЫ И СВОЙСТВ СТРОИТЕЛЬНЫХ МАТЕРИАЛОВ
2. 1 Элементный, химико-минералогический, фазовый и вещественный состав материалов
Для строительных материалов, представляющих собой смесь различных компонентов (например, портландцемент, сухая растворная смесь и другие), свойства во многом зависят от процентного содержания каждого компонента
(вещественного состава).
Вещество – это часть материи, представляющая собой химическое соединение, состав которого можно выразить простой химической формулой. Оно имеет определенную структуру и следующие физические и химические свойства: плотность, твердость, теплоемкость, коэффициент термического расширения, температуру плавления, растворимость, химическую активность, адсорбционную способность, электрические характеристики, цвет и цвет черты.
Так, для портландцемента вещественный состав характеризуют процентным содержанием клинкера, природного гипса, а также видом и количеством активных минеральных или органических добавок.
5
Важно также уделить внимание составу вещества, который, несомненно, влияет на свойства материала вне меньшей степени.
Элементарный состав показывает, какие химические элементы и в каком количестве входят в состав вещества. Например, элементарный состав битума колеблется в следующих пределах %: С – 70…85; Н – 9…16; S – 2…9; О – 1…5; N – 0…2. Гетероатомы О, S, N образуют активные функциональные группы СООН, ОН, NН2, SН, SО3Н, которые являются реакционноспособными, т.е. интенсифицируют адгезию (прилипание) битума к каменным материалам. Естественно, чем их больше, тем больше адгезия битума, а значит и водостойкость асфальтобетонов. Чем меньше атомное отношение С:Н и больше гетероатомов в битуме, тем выше его молекулярная масса и, соответственно, вязкость и температура размягчения, а значит и теплоустойчивость асфальтобетонов.
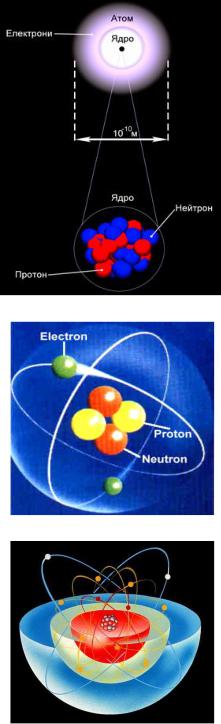
Физико-химические свойства вещества определяются также и электронным строением атомов химических элементов, из которых он состоит (рисунок 1). Особенности каждого химического элемента определяются, прежде всего, количеством протонов в ядре. В ядре атома платины 78 протонов, если добавить еще один протон, получится золото. Число протонов также влияет на количество и расположение электронов, вращающихся по своим орбитам. Периодическая таблица Д.И. Менделеева очень точно указывает на способность элементов вступать в химические реакции, о которой говорит валентность атомов или количество электронов на внешней орбите. Зная этот показатель, можно заранее предсказать, как именно поведет себя химический элемент во время конкретной реакции. Поэтому, при разработке материалов и процессов их получения необходимо четко представлять, как различные элементы отдают и принимают электроны, как изменение электронного состояния влияет на свойства элементов.
Рисунок 1 – Структура атома. Она была открыта вначале XX в. Э. Резерфордом, а в 20-х гг. интерпретирована Н. Бором – маленькое положительно заряженное ядро в центре, окруженное еще более мелкими (примерно 2000 раз меньше
массы протона и нейтрона) отрицательно заряженными электронами, вращающимися по своим орбитам. Ядро атома состоит из протонов и нейтронов, которые имеют общее название нуклоны. Нейтроны удерживают положительно заряженные протоны, стремящиеся оттолкнуться друг от друга. В 70-х гг. было установлено, что внутри каждого протона и нейтрона имеется по три кларка. Они обмениваются глюонами (от англ. Glue – клей), способными преодолеть силы отталкивания, или частицами, которые являются квантами цветового поля. Атом не имеет электрического заряда, поскольку число протонов и электронов в нем одинаково.
6
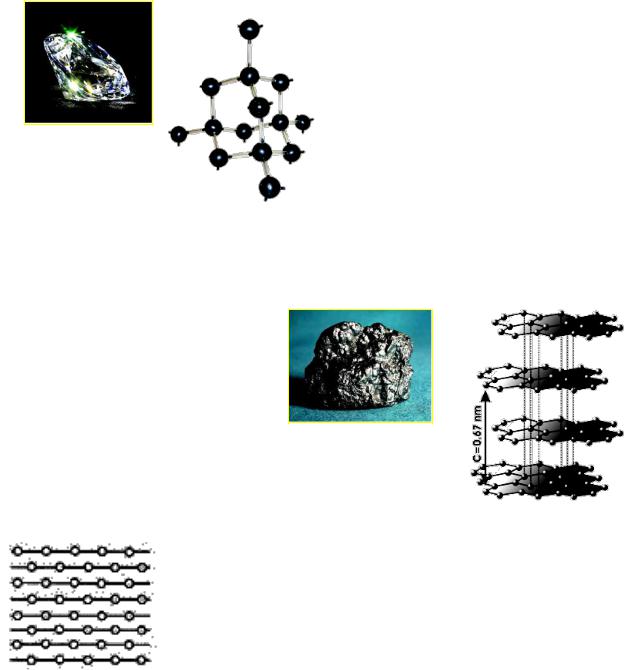
В редких случаях изменение физико-химических свойств веществ зависит не от элементного состава, а от строения. Так, элементный состав алмаза, графита, карбина, фуллерена, лонсдейлита (кристаллическая форма) и пироуглерода, пирографита, стеклоуглерода, сажи, кокса (аморфные и частично кристаллическими переходные формы) представлен углеродом. Однако свойства этих веществ разительно отличаются друг от друга.
Алмаз представляет собой пространственный трехмерный полимер с тетраэдрическим расположением валентных связей. Это изотропный атомный кристалл, атомы углерода которого находятся в состоянии sp3-гибридизации, связи между атомами углерода ковалентные и одинаковые по длине (рисунок 2).
Рисунок 2 – Кристаллическая структура алмаза
Графит является «паркетным» полимером. Он имеет гексагональное строение (рисунок 3). В плоскостях слоев между атомами существуют ковалентные sp2-гибридные связи, а между слоями – вандерваальсово взаимодействие, что пред-
определяет сильную анизотропию свойств вдоль параллельных и перпендикулярных направлений к плоскостям слоев. Слабостью сил ван-дер-ваальса объясняется и возможность использования графита для письма и сухой смазки – связи по ним разрываются, и чешуйки графита в виде слоев, составленных из шестиугольных колец углерода, остаются на бумаге.
Рисунок 3 – Кристаллическая структура графита
Карбин – углеродный полимер с линейной структурой. В молекулу карбина входит до 2000 атомов. Длина полимерных нитей колеблется от 50 до 250 нм. Плот-
ность карбина 1900...3200 кг/мз. Карбин химически инертен, обладает полупроводниковыми свойствами – при облучении светом его проводимость резко возрастает (рисунок 4).
Рисунок 4 – Структура карбина
Строение пироуглерода – графитовые сетки, объединенные по несколько штук в пакеты или кристаллы и расположенные параллельно поверхности осаждения. При нагреве выше 1800
°С наблюдается упорядочение турбостратного строения с образованием графита, свыше 2400 °С образуется пирографит (рисунок 5).
Стекловидный углерод (стеклоуглерод) – сетчатый полимер углерода, имею-
7

щий надмолекулярное строение в виде клубков (глобул). При этом глобулы представляют собой беспорядочное переплетение лентовидных молекул.
Изделия из пироуглерода
Стеклоуглеродные тигли
Рисунок 5 – Изделия из пиро- и стеклоуглерода
Минералогический состав показывает, какие минералы и в каком количестве содержатся в вяжущем веществе или горной породе. Например, в портландцементе содержание трехкальциевого силиката (3СаОSiО2) составляет 45…60 %, причем при большем его количестве ускоряется твердение, повышается прочность цементного камня.
Минералогический состав горных пород в значительной мере предопределяет физико-механические, технологические и эстетические свойства облицовочного камня и с этой точки зрения представляет повышенный интерес для технологии его обработки и соответственно для камнеобработчиков. Такие минералы как кварц и слюда придают граниту характерный блеск, а полевые шпаты окрашивают его в серый или розовый цвет. В то же время граниты с преобладанием кварца отличаются высокой прочностью и долговечностью, слюда же наоборот существенно снижает эти показатели.
Химический состав строительных материалов позволяет судить о некоторых его свойствах: огнестойкости, биостойкости, электропроводности, механических и других технических характеристиках. Например, наличие в глине оксида алюминия повышает ее огнеупорность, а отсутствие оксида железа придает ей белый цвет. Оксиды бериллия, магния, кальция и бария способствуют снижению коэффициента термического расширения стекла. Термическое же расширение стекла растет, если в нем присутствуют оксиды лития, натрия и калия.
Химический состав неорганических вяжущих (цемента, извести и каменных материалов) удобно выражать количеством содержащихся в них оксидов.
Кислые (SiO2), амфотерные (Al2O3, Fe2O3) и основные (CaO, MgO, Na2O, K2O)
оксиды в природных условиях или в процессе высокотемпературной обработки химически взаимодействуют с образованием комплексных соединений, свойства которых различны и зависят от химического состава.
Фазовый состав. В материале выделяют твёрдые вещества (твёрдую фазу), образующие стенки пор, т.е. «каркас» материала, а также поры, заполненные воздухом и водой, – газообразные и жидкие вещества (газообразная и жидкая фазы).
Процентное содержание этих фаз разительно изменяет свойства материалов, а значит и область их применения. Так, в теплоизоляционных материалах
8
количество газообразной фазы может достигать 98 %, а в гидроизоляционных материалах оно приближается к нулю.
Если вода, являющаяся компонентом материала, замерзает (происходит фазовый переход из жидкого в твердое состояние), то образовавшийся в порах лед изменяет его механические и теплофизические свойства. Увеличение же объема замерзающей в порах воды вызывает в материале внутренние напряжения, способные его разрушить при повторных циклах замораживания и оттаивания. Процесс твердения цементобетона при положительных температурах сопровождается испарением воды с образованием открытых пор, что в конечном итоге снижает его такие эксплуатационные показатели как водо- и морозостойкость.
На свойства материалов существенное влияние оказывает и структура твердой фазы, которая может быть кристаллической или аморфной.
Вещества с кристаллической структурой имеют ряд особенностей. Ато-
мы в них располагаются в строго определенном порядке, образуя пространственную решетку, за счет которой имеют вид правильных многогранников. Такая форма, в частности, присуща кристаллам кальцита, кварца, апатита. Многие из них обладают неоднородностью свойств – анизотропностью по разным направлениям. Это механическая прочность, теплопроводность, скорость растворения, электропроводность и другие, вызванные дальним порядком (упорядочением) расположения атомов.
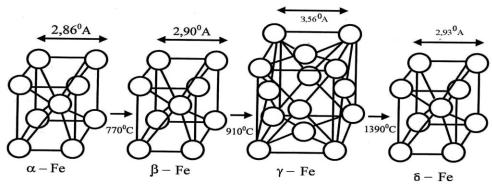
Они имеют строго определенную температуру плавления (при постоянном давлении). Для них свойственно явление полиморфизма, характеризующееся скачкообразным изменением кристаллической решетки в твердом состоянии при определенной температуре. Например, полиморфные превращения железа или кварца, сопровождающиеся изменением объема (рисунки 6, 7).
Рисунок 6 – Полиморфные
превращения железа
Кремнезем SiО2 в обычных условиях чаще всего встречается в виде минерала β-кварца с p = 2,656 г/см3, при температуре 573 оC превращается в α-кварц с плотностью 2,56 г/см3, а объем кристалла увеличивается примерно на 3,5 %. При дальнейшем медленном повышении температуры до 870 оС может превратиться в α-тридимит, обладающий плотностью 2,2 г/см3, объем которого может увеличиться на 19 %.
Вещества с аморфной структурой имеют обычно форму натеков, как например, лимонит (или бурый железняк). Атомы в них расположены беспоря-
9

дочно, т.е. имеют ближний порядок, где закономерность существует только в расположении соседних частиц.
Такие вещества не обладают определенной температурой плавления, поэтому при нагревании они постепенно размягчаются, пока окончательно не расплавятся (стекло, янтарь, обсидиан, твердые смолы, полимеры). В аморфном веществе различные свойства (теплопроводность, упругость, прочность) не зависят от направления. Такие вещества называются изотропными.
Рисунок 7 – Полиморфные превращения кварца
Так как кристаллическая форма более устойчива, то для того чтобы вызвать химическое взаимодействие между кварцевым песком и известью, в технологии силикатного кирпича применяют автоклавную обработку отформованного сырца насыщенным водяным паром с температурой 175 оС и давлением 0,8 МПа. Между тем, трепел (аморфная форма SiО2) вместе с известью после затворения водой образует гидросиликат кальция при температуре 15...25 оС.
Кристаллические и аморфные формы нередко являются лишь различными состояниями одного и того же вещества (например, кристаллический кварц и различные формы кремнезема – трепел).
Аморфная форма веществ может перейти в более устойчивую кристаллическую форму. Опал – аморфная форма кремнезема, со временем, старея, кристаллизуется и переходит в кристаллическую форму – халцедон и его разновидности: агат, оникс, яшму, используемые в качестве полудрагоценных камней.
Для аморфных веществ (например, трепел, диатомит и опока) характерна меньшая плотность, твердость, но большая химическая активность и растворимость, чем для кристаллических веществ (кварцевый песок). Первые три используются в качестве активных минеральных добавок, последний – инертный заполнитель в растворах и бетонах.
Четвертым агрегатным состоянием веще- |
|
||
ства часто считают плазму. |
|
||
Плазма – частично или полностью ионизи- |
|
||
рованный газ, в котором концентрации положи- |
|
||
тельных и отрицательных зарядов практически |
|
||
равны. Ионизация газа может быть вызвана тем- |
|
||
пературным |
воздействием, электромагнитным |
Рисунок 8 – Плазма |
|
излучением |
или бомбардировкой заряженными |
||
|
|||
частицами (рисунок 8).
10
