
- •Глава 13
- •13.1. Классификация, номенклатура и Строение спиртов
- •13.1.1. Классификация спиртов
- •13.1.2. Номенклатура спиртов
- •13.1.3. Строение спиртов
- •13.1.4. Изомерия
- •13.2. Физические свойства спиртов
- •13.2.1. Спектроскопия спиртов
- •13.3. Получение одноатомных спиртов в промышленности
- •13.4. Методы синтеза одноатомных спиртов в лаборатории
- •13.5. Химические свойства одноатомных спиртов
- •13.5.1. Разрыв связи с–он
- •13.5.2. Разрыв связи о–н
- •13.6. Отдельные представители одноатомных спиртов
- •13.7. Непредельные спирты и их эфиры
- •13.7.1. Енолы
- •13.7.2. Получение производных енолов
- •13.7.3. Аллиловый спирт
- •13.7.4. Высшие непредельные спирты
- •13.7.5. Ацетиленовые спирты и простые эфиры
- •13.8. Гликоли
- •13.8.1. Физические свойства гликолей
- •13.8.2. Методы синтеза гликолей
- •13.8.3. Химические свойства гликолей
- •А) реакции окисления с сохранением углеродной цепи;
- •13.8.4. Применение гликолей
- •13.9. Многоатомные спирты
- •13.9.1. Получение глицерина
- •13.9.2. Химические свойства глицерина
- •13.9.3. Применение глицерина
- •13.9.4. Многоатомные спирты
- •13.9.5. Жиры и масла
13.9. Многоатомные спирты
Из многоатомных спиртов простейшим и наиболее важным представителем является глицерин (пропантриол-1,2,3). Он был открыт в 1779 г. знаменитым шведским химиком К. Шееле.
13.9.1. Получение глицерина
Гидролиз жиров. Глицерин был получен гидролизом жиров, которые являются сложными эфирами глицерина и высших гомологов уксусной кислоты и их олефиновых изологов. При гидролизе жиров перегретым паром глицерин остается в водном растворе, который отделяют от слоя расплавленных жирных кислот.
При щелочном гидролизе жиров получают натриевые соли высших жирных кислот – мыла. Отсюда процесс гидролиза сложных эфиров при действии щелочей называется омылением. В настоящее время этот процесс лежит в основе получения глицерина для косметических и фармацевтических целей.
Синтез на основе пропилена.
Первый синтез глицерина осуществили Ш. Фридель и М. Сильва в 1872 г. по следующей схеме:
 .
.
В настоящее время глицерин получают из пропилена, выделяемого при крекинге нефти:

Недостатком этого метода является большой объем сточных вод, содержащих минеральные соли и органические вещества, которые требуют трудоемкой утилизации, и непроизводительный расход хлора.
Способ, не связанный с применением хлора, основан на окислении пропилена до акролеина с последующим его восстановлением до аллилового спирта и гидроксилированием последнего до глицерина:
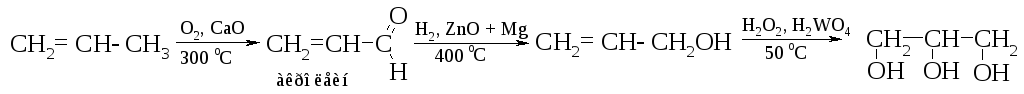
Синтез на основе пропаргилового спирта. Для этого используют конденсацию ацетилена с формальдегидом в пропаргиловый спирт, который селективным гидрированием переводят в аллиловый спирт. Затем по методу, описанному в предыдущей схеме, получают глицерин:
![]()
Некоторое количество глицерина образуется при отдельных видах брожения сахаров.
Очень перспективный технический синтез глицерина разработали в Польше Я. Береш и Л. Якубович. Восстановлением простейшего непредельного альдегида акролеина, полученного в условиях кротоновой конденсации по Оппенауэру, синтезируют аллиловый спирт, который превращают в глицерин:
![]()
![]()
Разработанные и внедренные в производство способы получения глицерина позволили сократить расход пищевых жиров на технические цели.
13.9.2. Химические свойства глицерина
Кислотные свойства. Химические свойства глицерина обуславливаются присутствием и взаимным влиянием трех гидроксильных групп; его кислотность выше, чем кислотность одноатомных и двухатомных спиртов, поэтому он образует растворимые в воде соединения – глицераты не только с щелочными металлами, но и оксидами металлов, например оксидом кальция.

Этерификация. Взаимодействием глицерина с одноосновными органическими кислотами синтезируют полные или неполные сложные эфиры. С двухосновными карбоновыми кислотами образуются полиэфирные волокна и смолы, идущие на лакокрасочные или пленкообразующие композиции.
При взаимодействии глицерина с неорганическими кислородсодержащими кислотами образуются полные и неполные сложные эфиры, например:
![]()
Полный азотнокислый эфир глицерина – глицеринтринитрат (обычно неправильно называемый нитроглицерином) – взрывчатое вещество, применяемое для изготовления динамита; 1%-ный раствор под названием нитроглицерин – лекарственное средство.
Реакции замещения.
При действии соляной кислоты на глицерин получается смесь монохлоргидринов, содержащая больше α-монохлоргидрина СН2ОН-СНОН-СН2Cl и меньше β-изомера СH2OH-CHCl-CH2OH. При обработке щелочью оба изомера дают один и тот же глицидный спирт:
![]() .
.
При обработке глицерина в более жестких условиях образуются два дихлорглицерина: CH2Cl-CHCl-CH2OH и CH2Cl-CHOH-CH2Cl. При обработке щелочью они дают эпихлоргидрин глицерина:
![]() .
.
Аналогичные результаты получают при взаимодействии глицерина с бромистоводородной кислотой.
В реакции с иодоводородом все три гидроксила замещаются на иод, но образующийся 1,2,3-трииодпропан далее восстанавливается до 2-иодпропана.
![]()
При действии хлоридов и бромидов фосфора в глицерине замещаются на галоген все три гидроксила:
![]()
а при взаимодействии с иодом и фосфором первоначально образующийся 1,2,3-трииодпропан распадается до аллилиодида:
![]()
При дегидратации глицерина с водоотнимающими средствами или при нагревании в свободном состоянии, а также в виде жиров, он превращается в акролеин:
![]()
Окисление глицерина дает в зависимости от условий реакции и окислителя целый набор продуктов.

