
Метаболиты эстрадиола и патологические процессы
пролиферацию внутреннего слоя эпителиальных клеток протоков молочной железы, впоследствии также подвер гающихся апоптозу. Всего в течение приблизительно 40-летнего репродуктивного периода в организме женщи ны осуществляется несколько сотен подобных циклов.
Регулярно повторяющиеся циклы эстроген-индуциро- ванного клеточного деления могут двояко влиять на ра звитие опухолевого процесса в гормон-зависимых тканях. Во-первых, пролиферировать под действием эстрогенов могут уже малигнизированные (подвергнувшиеся дей ствию внешнего канцерогена или имеющие набор терми нальных мутаций) клетки, пролиферация которых приво дит к формированию «опухолевого клона» и впослед ствии к наследственному раку. Кроме того, периодически повторяющиеся циклы клеточного деления неизбежно повышают частоту появления новых, спонтанных мутаций.
Очевидно, что вероятность появления «генетических поломок» в органах репродуктивной системы будет неиз бежно возрастать с увеличением возраста женщины. Вопервых, просто в силу временного фактора (увеличение времени экспозиции клеток-мишеней с эстрогенами — промоторами пролиферации и индукторами генотокических поврежедений), а во-вторых, по причине накопления в анамнезе возрастных и системных заболеваний, допол нительно ослабляющих иммунитет, а также продолжи тельного воздействия других факторов риска онкозабо леваний.
В самом деле, согласно данным статистики, первый пик заболеваемости раком молочной железы (80-100 случаев на 100 000 женщин) приходится на репродуктивный пе риод женщины — от 30 до 45 лет. Второй и третий пики отмечаются соответственно в возрасте 50-60 лет (180 слу-
ГЛАВА 3
использование тканями в качестве энергетического мате риала насыщенных жирных кислот вместо глюкозы. По добные сдвиги встречаются при нормальном старении, болезнях компенсации (терминология автора) — атеро склерозе, гипертонической болезни, ожирении, диабете, климаксе, возрастной психической депрессии, а также при хроническом стрессе и переедании (избытке в пита нии жиров, белков или углеводов). Например, при перее дании или нерациональном питании в крови увеличивает ся уровень инсулина и холестерина — индукторов деле ния соматических клеток.
Таким образом, канкрофилия — это сумма гормо нально-метаболических условий-сдвигов, повышаю щих вероятность злокачественной трансформации клетки.
В отношении гормон-зависимых опухолей теория канкрофилии справедлива в наибольшей степени. Ведь уве личение пула-совокупности пролиферирующих (деля щихся) клеток (а, следовательно, частота возникновения потенциально онкогенных мутаций) в гормон-зависимых тканях предопределено самим фактом существования по следних. В разделе «Два типа эстроген-индуцированного канцерогенеза» мы подробно обсуждали промоторную роль эстрогенов в процессах опухолеобразования. Еще раз напомним, что в тканях женской репродуктивной си стемы ежемесячно происходят колебания митотической клеточной активности, регулируемые ритмическими изме нениями уровня половых гормонов. В первой (т.н. пролиферативной) фазе менструального цикла секретируемыи яичниками эстроген индуцирует пролиферацию клеток эндометрия, гибнущих во время менструации. Аналогич но, каждый менструальный цикл эстроген стимулирует

ГЛАВА 3
чаев на 100 000 женщин) и после 65 лет (250 случаев на 100 000 женщин). Кумулятивный риск развития РМЖ у женщины, дожившей до 85 лет, достигает 10% (в данных рассуждениях не учитывается наследственный рак, веро ятность которого составляет от 3 до 5% всех случаев дан ного опухолевого заболевания).
Таким образом, в отличие от большинства других опухолеобразующих органов и тканей гормон-зависимые ткани представляют собой регулируемую биологическую систему, подвергающуюся на протяжении всего репро дуктивного периода женщины периодической стимуляции к клеточному росту. Пока защитные силы каждой отдель ной клетки и организма в целом достаточны для того, что бы противостоять раскачивающим устойчивость данной системы «качелям», ситуация находится под контролем. В случае их ослабления — при неблагоприятных внешних или внутренних условиях или просто по причине старения организма — нарушаются регуляторные механизмы кле точного деления и появляется вероятность возникнове ния опухолевого процесса. Риск возникновения гормонзависимых опухолей многократно возрастает при нали чии одного или нескольких факторов риска.
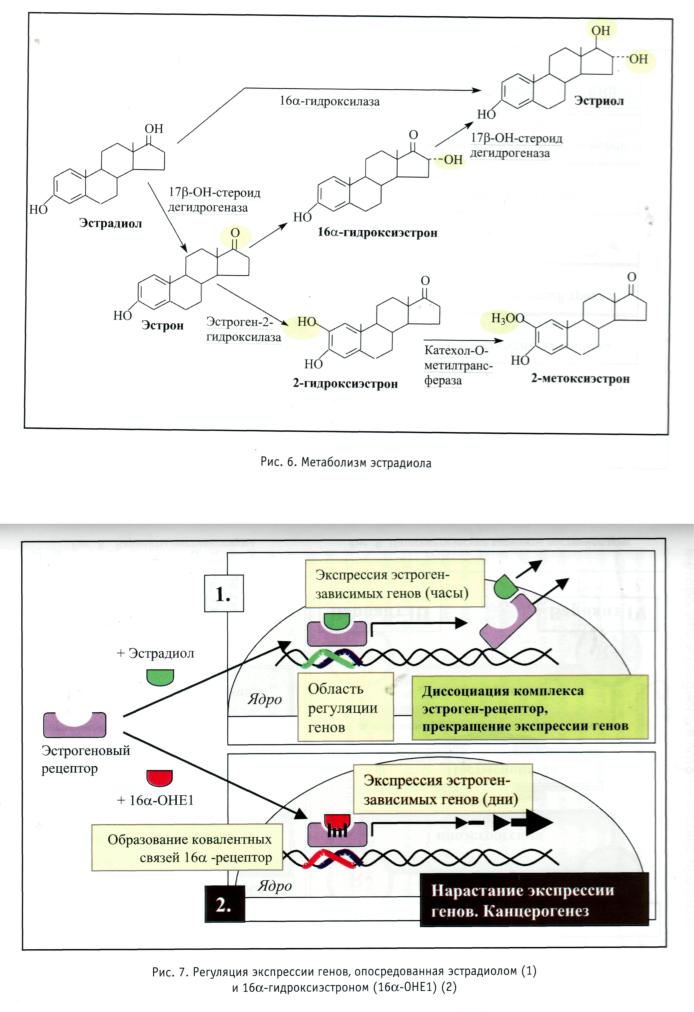
И в заключение еще об одном обстоятельстве, непо средственно касающемся метаболических сдвигов в орга низме, предшествующих канцерогенезу. Как мы отмечали выше, в главе «Роль метаболитов эстрогенов в канцероге незе репродуктивных органов», в последние годы появля ется все больше данных, свидетельствующих о том, что на рушение баланса метаболитов эстрогенов — 2-гидрокси- эстрона и 16а-гидроксиэстрона — играет ведущую роль в процессах опухолеобразования в гормон-зависимых тка нях (органах репродуктивной системы) у женщин, находя-



Метаболиты эстродиоло и патологические процессы...
щихся в менопаузе (постменопаузе). Причины данного фе номена пока до конца не ясны. Одно из возможных объяс нений может выглядеть следующим образом.
Известно, что цитохромы Р-450, относящиеся к фер ментам 1-й фазы трансформации и катализирующие клю чевые фазы метаболизма эстрогенов, а именно образова ние их 2- и 16а-гидроксипроизводных, метаболизируют еще и ксенобиотики, в том числе ряд канцерогенов, нахо дящихся в окружающей среде, например полицикличе ские ароматические углеводороды (ПАУ). Показано, что последние способны изменять активность цитохромов Р-450 для эстрогенов таким образом, что происходит сдвиг метаболизма в сторону накопления более «агрес сивных» форм эстрогенов (2).
Возможно также, что дисфункция изоферментов цитохрома Р-450, контролирующих нормальный метаболизм эстрогенов, наступает вследствие нарушения внутренних регуляторных систем организма.
Нельзя исключить и тот факт, что на преимуществен ное образование «агрессивных» форм эстрогенов у постменопаузальных женщин оказывает влияние смещение места синтеза половых гормонов из яичников в жировую ткань, где основным эстрогеновым продуктом является образующийся из андростендиона эстрон.
Фармакологическая коррекция гормонального баланса и профилактики образования гормон-зависимых опухолей
Довольно давно было замечено, что важнейшим фак тором, влияющим на процессы канцерогенеза, является диета, и что некоторые пищевые компоненты (преимуще-
ГЛАВА 3
ственно растительного происхождения) способны тормо зить образование опухолей в организме. Одними из пер вых в этом списке традиционно назывались растения се мейства крестоцветных: различные виды капусты (бело-,'' краснокачанная, брюссельская, цветная, брокколи), ка бачки, брюква, турнепс, горчица. Позднее выяснилось, что антиканцерогенная активность перечисленных овощ ных культур обусловлена наличием в их составе пищево го индола — индол-3-карбинола (I3C), высвобождающе гося в результате гидролиза его предшественника индолилметилглюкозинолата — глюкобрассицина (11). Было установлено, что I3C обладает уникальной особенностью значительно снижать риск возникновения опухолей в гор мон-зависимых органах и тканях посредством нормали зации гормонального баланса (соотношения метаболитов эстрогенов) в организме.
Впервые противоопухолевое действие I3C было проде монстрировано на модели рака молочной железы в 70- 80-х гг. В экспериментах in vitro и in vivo на животных бы ло установлено, что I3C обладает выраженной способно стью снижать частоту возникновения опухолей молочной железы, индуцированных экзогенными канцерогенами (диметилбензантраценом) (38, 49).
Спустя приблизительно 10 лет был впервые постули рован молекулярный механизм, посредством которого I3C обезвреживает канцерогенные ксенобиотики (б). Оказалось, что пищевые индолы являются активаторами входящих в состав монооксигеназной системы печени индуцибельных изоформ цитохрома Р-450. Напомним, что изоферменты цитохрома Р-450 (функции и механизм действия которых были подробно рассмотрены нами в предыдущих разделах) относятся к ферментам 1-й фазы
