- •С.С. Виноградов
- •Экологически безопасное гальваническое производство
- •Под редакцией проф. В.Н.Кудрявцева
- •Раздел 1. Экологическая опасность технологических растворов 7 гальванического производства и направления ее снижения
- •Раздел 4. Базовые принципиальные схемы очистки промывных и 162 сточных вод
- •Раздел 6. Регенерация (восстановление работоспособности) 241 отработанных электролитов
- •Раздел 8. Утилизация гальванических шламов 289
- •Раздел 9. Создание экологически безопасного гальванического 297 производства
- •Раздел 1. Экологическая опасность технологических растворов гальванического производства и направления ее снижения
- •1.3. Базовые составы растворов и электролитов
- •Анодное окисление алюминия и его сплавов
- •Химическое оксидирование алюминия и его сплавов
- •Покрытий
- •Раздел 2. Рациональное водопотребление на промывочных операциях
- •Удельные нормы расхода воды в зависимости от количества ступеней
- •Раздел 3. Состав и объём сточных вод гальванического производства
- •Процессов
- •Iimpomaiii
- •3.2. Состав и объём общих сточных вод от цеха (участка) гальванопокрытий
- •Раздел 4. Базовые принципиальные схемы очистки промывных и сточных вод
- •Содержание активной части и условия поставки
- •4.2. Электрокоагуляционный метод
- •Ионообменная очистка
- •Метод электрофлотации
- •4.6. Метод электродиализа
- •Поверхностный спои адсорбированных молекул воды
- •1 Вода 1 на доочистку
- •4.10. Метод жидкостной экстракции
- •Метод дозированного выпаривания
- •Раздел 5. Принципы адаптации гальванического цеха и систем очистки сточных вод
- •Раздел 6. Регенерация (восстановление работоспособности) отработанных электролитов
- •6.1. Классификация методов обработки отработанных растворов и
- •6.2. Регенерация отработанных растворов и электролитов
- •Регенерация растворов обезжиривания
- •Ihuh Очищенный раствор Рис. 6.1. Схема мембранной очистки обезжиривающих растворов
- •6.2.2. Регенерация травильных растворов
- •6.2.4. Регенерация электролитов кадмирования
- •6.2.7. Регенерация хромсодержащих растворов и электролитов
- •Раздел 7. Рекуперация (утилизация в гальваническом производстве) отработанных технологических растворов
- •Рекуперация (утилизация в гальваническом производстве)
- •Отработанных технологических растворов, содержащих шестивалентный хром
- •Раздел 8. Утилизация гальванических шламов
- •Раздел 9. Создание экологически безопасного гальванического производства
- •Химикаты вода
В
процессах хромирования электролиты
загрязняются примесями металлов
вследствие растворения материала
деталей, а также ионами Сг3+
из-за нарушения соотношения анодной и
катодной поверхностей. Повышение
содержания примесных металлов существенно
снижает удельную электропроводимость
раствора электролита, приводит к
уменьшению выхода по току, рассеивающей
и кроющей способностей электролитов
хромирования. Загрязнение электролитов
ионами меди, железа, никеля, цинка и
других металлов снижает антикоррозионные
свойства хромовых покрытий. В случае
использования саморегулирующихся
электролитов, содержащих фториды или
кремнийфториды, растворимость и
накопление ионов посторонних металлов
возрастает.
Очистку
электролитов хромирования от примесных
металлов ионообменным
методом
проводят с помощью сильнокислотных
катионообменных смол в Н-форме для
связывания металлов и выделения в
раствор эквивалентного количества
ионов водорода. Однако, этот метод
применим только для регенерации
разбавленных электролитов с концентрацией
СгОз до 100 г/л. При более высокой
концентрации происходит деструкция
смол с одновременным восстановлением
Cr(VI)
до Сг(Ш).
Поэтому
рекомендуется проводить регенерацию
раствора хромирования совместно с
регенерацией хрома (VI) из промывных вод
от ванн улавливания или каскадных ванн
промывки. В этом случае хромсодержащие
растворы пропускают поочередно через
катионообменные и анионообменную
колонки. В катионитовой колонке из
растворов удаляются катионы Сг3+,
Zn2+,
Fe3+,
Cu2+
и др. В качестве катионита может быть
использована сульфостирольная смола
марки КУ-2-8 в Н-форме. Десорбция
производится 10 %-ным раствором серной
кислоты. В анионитоврй колонке
адсорбируются анионы хромовой кислоты.
В качестве анионита используются иониты
марки АВ-17-8, АВ-29, АВ-17-16. Десорбция
анионитовых смол осуществляется
раствором едкого натра. Образующийся
элюат в виде хромата натрия направляется
в катионообменную колонку для удаления
ионов натрия.
При
этом происходят следующие реакции:
2736.2.7. Регенерация хромсодержащих растворов и электролитов
Первая
катионитовая колонка: сорбция 3[R-S03H]
+ Cr3+
—» [R-S03']3Cr
+ ЗН+
десорбция [R-S03']3Cr
+ЗН+
—» 3[R-SCbH]
+ Сг3+
Анионитовая
колонка: сорбция 2R
-OH
+ СгОз —» [R'
]гСг04 + НгО
десорбция [R'
]гСгО* + 2NaOH
—> 2R-OH
+ NагСг04
Вторая
катионитовая колонка: сорбция Na2Cr04
+ 2[R-S03H]
—> 2[R-S03Na]
+ СгОз + НгО
десорбция [R-SOsNa]
+ Н+
—> [R-SO3H]
+
Na+
Регенерированная
хромовая кислота с концентрацией СгОз
в пределах 50-60 г/л после частичного
выпаривания направляется в ванны
хромирования для корректировки
электролита.
Для
регенерации электролитов хромирования
с концентрацией СгОз 150-300 г/л целесообразно
применять электрохимические
методы
регенерации. В большинстве случаев
анодными материалами служат свинец,
сплавы его с сурьмой, серебром и оловом,
графит, титан, сталь, покрытая окисью
свинца или марганца. Катоды изготавливаются
из меди или нержавеющей стали. Так как
реакции окисления и восстановления
протекают почти с одинаковой скоростью,
то для исключения попадания в катодную
зону ионов Сг4*
необходимо с помощью диафрагмы отделить
катодное пространство от анодного,
куда заливается раствор. Наиболее
устойчивыми для этих целей являются
специально изготавливаемые керамические
и фторопластовые диафрагмы, а также из
винипора, винипласта, пористого стекла.
Диафрагмы должны обладать рядом
технических свойств: химической
стойкостью в агрессивных средах, низким
электросопротивлением, достаточно
высокой скоростью движения ионов,
обеспечивающих протекание тока, и
низкой скоростью перемещения других
компонентов раствора, механической
стойкостью, длительностью срока службы.
Процесс
протекает при температуре 40-60 °С,
плотности анодного тока 3-4 А/ду2,
катодного тока 17-20 А/дм2.
Католитом служит раствор серной кислоты
или смеси солей сульфатов и бисульфатов.
274
Использование
ионитовых мембран для разделения
катодного и анодного пространств
проблематично, так как большинство из
них в хромсодержащих растворах теряет
селективность. Наиболее стойкими в
этих условиях являются ионитовые
мембраны марок MAJ1-2
и МП-2. При использовании анионитовых
мембран отработанные электролиты
хромирования помещают в катодную
камеру, а в анодную - 3-4 %-ный раствор
серной кислоты. Электролиз в этом случае
позволяет вернуть в производство 40-50
% хромовой кислоты, остальное количество
идет на осаждение гидроокиси хрома.
Раствор хромовой кислоты после окончания
электролиза в анодной камере практически
не содержит примесей Сг3+,
Си2+
и других металлов, которые осаждаются
в катодной камере преимущественно в
виде гидроокисей.
При
использовании катионитовых
мембран отработанные электролиты
хромирования помещают в анодную камеру
диафрагменного электролизера, а в
катодную заливают 5 %-ный раствор серной
кислоты или сульфата натрия, подкисленного
серной кислотой. Это позволяет обеспечить
практически полное удаление примесей
Сг3+
и большей части (70-90 %) примесей железа,
цинка, меди без снижения концентрации
хромовой кислоты. Примеси металлов
осаждаются в катодном пространстве в
виде осадков гидроокисей или в виде
рыхлого, порошкообразного, легко
отделяемого осадка, частично осыпающегося
с поверхности катодов. Схема процесса
электродиализа показана на рис.6.2.
Процесс ведут при катодной плотности
тока 2,7-10 А/дм2
и объемной плотности тока 2,2-8 А/л. Расход
электроэнергии на обработку 1 л
электролита хромирования составляет
0,4-1,7 кВт-ч.
Мембраны
перед монтажом предварительно
вымачиваются в
%-ном
растворе серной кислоты под прессом
и после набухания подлежат сборке. Для
обеспечения механической прочности
мембран их помещают между сепараторными
сетками из винипласта, а температуру
анолита и католита поддерживают в
пределах 40-50 °С путем искусственного
охлаждения.
В
процессах без дополнительного охлаждения
за 20 ч электролиза при 2,7 А/дм2
концентрация Cr3+,
Cu2+,
Fe3+
в анолите снижается соответственно с
5,8; 11,3 и 3,8 до 0; 2,5 и 1,2 г/л, а за 16 ч при
плотности тока 3,3 А/дм2
- до 0; 1,9 и 0,6 г/л. Расход электроэнергии
составляет соответственно 600 и 640
кВт-ч/м3.
В условиях охлаждения электролитов
эффективность удаления
275
примесей
Сг3+
составляет 20-45%, Cu2+
электроэнергии
- 612-1400 кВт ч.
32-94%,
а расход
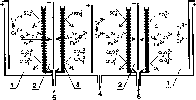
Рис.
6.2. Схема процесса электродиализа:
1-анодное пространство, 2-катодное
пространство, 3-катионитовые мембраны
с сепараторными сетками, 4-выпуск
очищенного раствора хромирования,
5-выпуск раствора сульфатов примесных
металлов и металлического порошка.
Отработанные
растворы хроматирования и травления
меди весьма часто подлежат сливу из-за
быстрого выхода из строя, хотя такие
растворы еще содержат достаточно
большое количество хромовой кислоты
и других компонентов, необходимых для
обработки поверхности.
Регенерацию
отработанных растворов хроматирования
и травления меди можно проводить путем
фильтрации их через слой сильнокислотного
катионита типа КУ-23 или амфотерного
ионита АНКБ, где протекают следующие
ионообменные реакции:
2R-H
+ Zn2+
о R2-Zn
+ 2Н+
,
2R-H
+ Си2+
о R2-C11
+ 2Н+
,
3R-H
+ Сг3+
о R3-Cr
+ ЗН+
.
Преимущественное
высвобождение ионов водорода в процессе
регенерации позволяет поддерживать
кислотность раствора на оптимальном
уровне, составляющем 1,2-1,4. Лишь после
7-8 регенерационных циклов возникает
необходимость корректировки раствора
по кислотности.
Использование
электрохимических методов регенерации
в данном случае аналогично электрохимической
регенерации электролитов хромирования.
276