
- •Сборник контрольных работ по курсу общей химии
- •Рецензенты:
- •Содержание
- •1. Основные классы неорганических соединений
- •1.1. Назовите вещество и укажите класс химических соединений:
- •1.2. Напишите формулы следующих соединений:
- •1.3. Составьте уравнение реакции получения следующего соединения и рассчитайте массы реагентов, необходимых для получения 1 г вещества:
- •1.4. Напишите уравнения соответствующих реакций, учитывая, что другие вещества можно использовать только в качестве катализаторов:
- •1.5. Изобразите структурные формулы следующих соединений:
- •2. Основные законы химии
- •2.1. Рассчитайте давление в сосуде:
- •2.2. Вычислите эквивалентную массу:
- •2.3. Определите простейшую формулу вещества, если оно содержит (по массе):
- •2.4. Расставьте стехиометрические коэффициенты в реакциях и рассчитайте, какую массу второго реагента необходимо взять на 1 г первого, чтобы реакция прошла до конца:
- •2.5. Определите, какие продукты и в каком количестве (по массе) получатся при взаимодействии (обратите внимание на избыток одного из реагентов):
- •3. Строение атома и химическая связь
- •3.2. Определите, относится ли данная электронно-ячеечная формула к основному, возбужденному или невозможному состоянию атома, назовите химический элемент и укажите его порядковый номер:
- •3.3. Напишите уравнения ядерных реакций:
- •3.4. Определите тип гибридизации и пространственное строение следующих молекул и ионов:
- •3.5. Объясните с помощью метода молекулярных орбиталей возможность образования следующих молекул и ионов, определите порядок связи, установите, являются ли они диамагнитными или парамагнитными:
- •4. Химическая термодинамика
- •4.1. Используя справочные данные вычислить тепловой эффект реакции:
- •4.2. Не производя вычислений, определите знак изменения энтропии:
- •4.3. Вычислите изменение свободной энергии Гиббса и определите возможность протекания реакции при стандартных условиях:
- •5. Химическая кинетика и равновесие
- •5.1. Определите порядок реакции и рассчитайте, как изменится начальная скорость гомогенных химических реакций согласно закону действующих масс:
- •5.2. Рассчитать изменение скорости реакции при изменении температуры:
- •5.3. Определите, в каком направлении сместится равновесие гомогенных химических реакций (для оценки влияния температуры на положение химического равновесия рассчитайте δн реакции):
- •5.4. Найдите константы равновесия гомогенных химических реакций и исходные концентрации реагентов, если в закрытом сосуде установились следующие равновесные концентрации:
- •6. Растворы
- •6.1. Определите массовую долю (в %) и молярную концентрацию раствора, содержащего:
- •6.2. Определите массовую долю (в %) и моляльную концентрацию растворов, полученных смешением:
- •6.3. Определите относительное понижение давления пара над раствором, содержащим:
- •6.4. Найдите температуру кипения раствора, содержащего:
- •6.5. Найдите температуру замерзания раствора, содержащего:
- •7. Теория электролитической диссоциации
- •7.1. Запишите уравнения электролитической диссоциации следующих растворов электролитов и определите значение изотонического коэффициента при бесконечном разбавлении раствора:
- •7.2. Определите pH следующих растворов электролитов (изменением объема при смешении растворов пренебречь):
- •7.3. Запишите полные ионные, сокращенные ионные и молекулярные уравнения гидролиза следующих солей и определите реакцию среды:
- •7.4. Рассчитайте степень диссоциации в следующих растворах слабых электролитов, пользуясь справочными данными о Ка (для многоосновных кислот учитывайте только первую ступень диссоциации):
- •8. Окислительно-восстановительные реакции
- •8.1. Определите степени окисления элементов в веществах:
- •8.2. Укажите, какие атомы окисляются, а какие восстанавливаются в указанных схемах, и определите, как изменяется их степень окисления:
- •8.3. Расставьте коэффициенты в уравнениях окислительно-восстановительных реакций ионно-электронным способом:
- •8.4. Определите, в каком направлении протекает реакция в системе, используя справочные данные о стандартных восстановительных потенциалах полуреакций:
- •9. Электрохимические процессы и системы
- •9.1. Вычислите электродные потенциалы металлов, находящихся в контакте с растворами их солей заданной концентрации, при 25с:
- •9.2. Напишите уравнения электродных реакций на катоде и аноде и вычислите эдс гальванических элементов при 25с, для которых указаны концентрации ионов металла в растворах:
- •9.3. Каковы катодные и анодные процессы (угольный анод) при электролизе водного раствора, содержащего смесь солей:
- •9.5. Напишите уравнения, отражающие анодный и катодный процессы при электрохимической коррозии в указанных ниже системах:
- •10. Примеры решения типовых задач
- •Литература
- •Издательство «Экоцентр»
10. Примеры решения типовых задач
1.3
|
x г |
|
y г |
|
1 г |
|
|
2NaOH |
+ |
H3PO4 |
= |
Na2HPO4 |
+ 2H2O |
|
80 г/моль |
|
98 г/моль |
|
142 г/моль |
|
Для получения 142 г Na2HPO4 нужно взять 80 г NaOH;
для получения 1 г Na2HPO4 нужно взять x г NaOH:
![]() ,x
= 80:142 = 0,56 (г).
,x
= 80:142 = 0,56 (г).
Для получения 142 г Na2HPO4 нужно взять 98 г H3PO4;
для получения 1 г Na2HPO4 нужно взять y г H3PO4:
![]() ,
y
= 98:142 = 0,69(г).
,
y
= 98:142 = 0,69(г).
Ответ. Для получения 1 г гидрофосфата натрия нужно взять 0,56 г гидроксида натрия и 0,69 г фосфорной кислоты.
2.3
|
Элемент |
K |
Mn |
O |
|
wm, % |
39,67 |
27,87 |
32,46 |
|
Ar |
39,10 |
54,94 |
16,00 |
|
wm : Ar |
1,015 |
0,507 |
2,023 |
|
Целые кратные |
2 |
1 |
4 |
Ответ. K2MnO4.
3.3
При составлении уравнений ядерных реакций соблюдается равенство суммы зарядов и массовых чисел в левой и правой частях уравнения. При этом заряд электрона учитывается со знаком минус, протона и позитрона – со знаком плюс. Нейтрон и гамма-квант заряда не имеют. Кроме того, массы электронов, позитронов и гамма-квантов не учитываются.
Сумма зарядов частиц в левой части уравнения: 92 + 0 = 92 (нейтрон заряда не имеет), значит, ядро нового элемента имеет заряд 92 – 56 = 36 (криптон). Сумма массовых чисел частиц в левой части уравнения: 235 + 1 = = 236, значит, массовое число ядра криптона 236 – 139 – 3 = 94.
Ответ.
![]() .
.
4.4
Найдем при помощи справочных данных изменения энтальпии и энтропии реакции при стандартныхусловиях:
|
|
2H2(г.) |
+ |
O2(г.) |
|
2H2O(г.) |
|
H298, кДж/моль |
0 |
|
0 |
|
–241,8 |
|
S298, Дж/(мольК) |
130,5 |
|
205,0 |
|
188,7 |
H(реакции) = 2(–241,8) = –483,6 (кДж);
S(реакции) = 2188,7 – 2130,5 – 205 = –88,6 (Дж/К);
T = H/S = 483600 / 88,6 = 5460 (K).
Ответ. 5460 К.
5.2
Используем
правило Вант-Гоффа:
![]() .
.![]() .
.
Ответ. Скорость реакции увеличится в 243 раза.
5.4
2NO2
![]() 2NO
+ O2
2NO
+ O2
Равновесная концентрация [NO] = 0,024 M, значит, равновесная концентрация кислорода в два раза меньше: [O2] = 0,012 М.
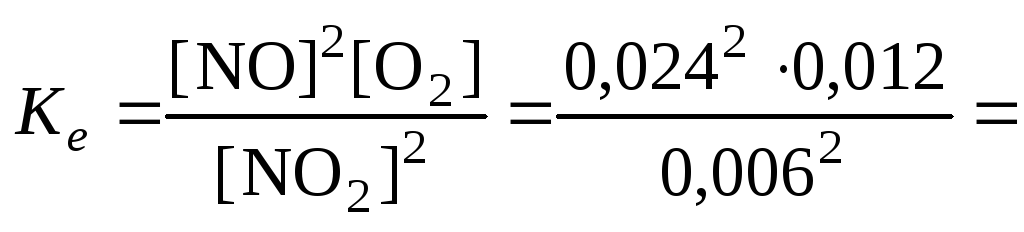 0,192
(моль/л).
0,192
(моль/л).
Учитывая, что стехиометрические коэффициенты перед NO2 и NO одинаковы, [NO2]0 = 0,006 + 0,024 = 0,030 (моль/л).
Ответ. Ke = 0,192 моль/л, [NO2]0 = 0,030 М.
6.2
Масса полученного раствора m = 70 + 50 = 120 (г).
Масса растворенного вещества m2 = 0,4070 + 0,1550 = 35,5 (г).
Массовая
доля растворенного вещества wm
=
![]() = 29,6%.
= 29,6%.
Масса растворителя m1 = 120 – 35,5 = 84,5 (г).
Моляльная
концентрация
![]() (моль/кг).
(моль/кг).
Ответ. wm = 29,6%; cm = 12,4 моль/кг.
6.3
1 = 50/18 = 2,778 (моль); 2 = 4,5/176 = 0,026 (моль);
![]() .
.
Ответ. P/P0 = 0,0093
7.4
Так как для сероводородной кислоты Ka1 = 10–7, то используем приближенную запись закона разбавления Освальда:
![]() или
0,18%.
или
0,18%.
Ответ. = 0,18%.
7.5
3Pb(NO3)2 + 2Na3PO4 = Pb3(PO4)2 +6NaNO3
3Pb2+ + 6NO3– + 6Na+ + 2PO43– = Pb3(PO4)2 + 6Na+ + 6NO3–
3Pb2+ + 2PO43– = Pb3(PO4)2
ПР = [Pb2+]3[PO43–]2
При смешении равных объемов растворов концентрация каждого из них уменьшается в два раза.
K’ = 0,0000530,000052 310–22
K’ > ПР, значит, выпадает осадок.
Ответ. Выпадает осадок Pb3(PO4)2.
8.4
Запишем стандартные восстановительные потенциалы электрохимических систем, участвующих в реакции:
Fe3+
+ 2I–
![]() Fe2++I2
Fe2++I2
Ок-ль:
Fe3+
+
![]() = Fe2+ 1
= 0,77 В;
= Fe2+ 1
= 0,77 В;
Вост-ль:
I2+
2![]() =2I– 2
= 0,54 В.
=2I– 2
= 0,54 В.
Поскольку ок > вос, то окислителем является ион Fe3+, а восстановителем – ион I–, т.е. реакция протекает слева направо.
Ответ. В стандартных условиях указанная реакция протекает слева направо.
9.2
Найдем значения электродные потенциалов:
![]() (В);
(В);
![]() (В).
(В).
Т.к. Fe > Cd, то на аноде окисляется кадмий, на катоде восстанавливаются ионы железа.
Е = –0,47 – (–0,52) = 0,05 (В).
Ответ. Е = 0,05 В.
9.4
K(–): Mg2+
+2![]() = Mg;
= Mg;
A(+): 2Cl–
= Cl2
+ 2![]() .
.
Масса магния, выделившаяся на катоде:
![]() (г).
(г).
Ответ. m = 2,27 г.
