
- •Понятие об эквиваленте. Эквивалент сложных веществ. Изменение эквивалента веществ, при вступлении их в химические реакции. Закон эквивалентов.
- •Теоретические основы объемного анализа. Классификация методов объемного анализа по реакции, лежащей в их основе и по способу титрования. Расчеты, применяемые в объемном анализе.
- •Перманганатометрия. Определение активности каталазы крови.
- •Йодометрия. Определение содержания чистой аскорбиновой кислоты в витамине c.
- •Окислительно-восстановительные реакции. Зависимость эквивалента окислителя и восстановителя от реакции среды.
- •Типы окислительно-восстановительных реакций.
- •Аргенометрия. Методы Мора и Фольгарда.
- •Термохимические уравнения и расчеты. Закон Гесса и следствия из него. Стандартные теплоты сгорания и образования и их применение для термохимических расчетов.
- •Обратимые и необратимые по направлению реакции. Понятия о химическом равновесии. Принцип Ле-Шателье.
- •Химическая кинетика, как основа для изучения скоростей и механизма биохимических процессов. Средняя скорость реакции.
- •Закон действующих масс. Константа скорости реакции. Зависимость скорости реакции от концентрации.
- •Молекулярность и порядок реакции. Лимитирующая стадия процесса.
- •Типы сложных химических реакций.
- •Уравнение кинетики реакции 1 порядка. Период полупревращения.
- •Уравнения кинетики реакции 2 порядка.
- •Зависимость скорости реакции от температуры. Температурный коэффициент скорости реакции (правило Вант-Гоффа).
- •Энергия активации. Уравнение Аррениуса.
- •Катализ и катализаторы. Гомогенный, гетерогенный и микрогетерогенный катализ.
- •Ферменты как биологические катализаторы и их классификация.
- •Ферментативный катализ. Уравнение Михаэлиса-Ментен и его анализ.
- •Способы выражения концентрации растворов.
- •Коллигативные свойства растворов. Закон Рауля и следствия из него.
- •Осмос и осмотическое давление. Закон Вант-Гоффа. Изотонический коэффициент.
- •Понижение температуры замерзания растворов. Криоскопическая постоянная.
- •Повышение температуры кипения растворов. Эбуллиоскопическая постоянная.
- •Роль осмоса и осмотического давления в биологических системах. Плазмолиз. Гемолиз.
- •Теория кислот и оснований. Сильные и слабые электролиты. Степень диссоциации.
- •Константа диссоциации. Закон разбавления Освальда.
- •Электролиты в организме человека.
- •Протолитическая теория кислот и оснований.
- •Диссоциация воды. Ионное произведение воды. Водородный показатель.
- •Гидролиз солей. Степень гидролиза.
- •Константа гидролиза соли, образованной сильным основанием и слабой кислотой (вывод уравнения).
- •Константа гидролиза соли, образованной слабым основанием и сильной кислотой (вывод реакции).
- •Константа гидролиза соли, образованной слабым основанием и слабой кислотой.
- •Ступенчатый гидролиз солей. Связь константы гидролиза со степенью гидролиза.
- •Буферные системы и механизм их действия. Буферная емкость и факторы ее определяющие.
- •Уравнение Гендерсона-Гассельбаха для расчета pH буферных систем (вывод).
- •Буферные системы крови.
- •Методы получения коллоидных растворов.
- •Методы очистки коллоидных растворов. Искусственная почка.
- •Строение коллоидных частиц. Строение мицеллы.
- •Электрокинетические явления. Электрофорез. Электроосмос. Потенциалы протекания и седиментации.
-
Аргенометрия. Методы Мора и Фольгарда.
Аргенометрия-метод объемного анализа, основанный на применении стандартного раствора нитрата серебра. Различают несколько методов аргенометрии: метод просветления, метод Мора, метод Фольгарда, метод Фаянса.
Метод Мора применяется для определения бромидов и хлоридов. Он основан на реакции, протекающей между Ag+ и Cl-,выполняется в присутствии индикатора – раствора хромата калия. Лишняя капля титрованного раствора AgNO3, прибавленная после достижения точки эквивалентности, вызывает выпадение кирпично-красного осадка Ag2CrO4, образующегося в результате взаимодействия Ag+ с ионами индикатора: 2Ag++CrO4-2=Ag2CrO4. Этот метод выполняется только в нейтральной или слабощелочной среде. В сильнощелочной среде образуется AgOH, который сразу же распадается на Ag2O и H2O: 2Ag+OH-=Ag2O+H2O.
Метод Фольгарда, основанный на реакции, протекающей между Ag+ и SCN-, выполняется в присутствии индикатора- насыщенного раствора железлоаммонийных квасцов, содержащих ионы железа. Ag++SCN-=AgSCN.
Лишняя капля раствора NH4SCN, прибавленная после достижения точки эквивалентности, вызывает появление кроваво-красного окрашивания раствора вследствие взаимодействия SCN- с ионами Fe+3 индикатора: Fe+3+3SCN-=Fe(SCN)3. Этот метод применяется в нейтральной и кислой среде. В щелочной среде Fe+3 образует осадок Fe(OH)3, а Ag+ может образовать осаок Ag2O.
-
Термохимические уравнения и расчеты. Закон Гесса и следствия из него. Стандартные теплоты сгорания и образования и их применение для термохимических расчетов.
Уравнения химических реакций, в которых записывается величина теплового эффекта, называются термохимическими. Для определения теплового эффекта используется калориметр, снабженный точным термометром. Количество теплоты, выделяющейся в калориметре, определяют по общей теплоемкости всех частей калориметра и изменению температуры: Q=C∆t, С=m1c1+m2c2.
Закон Гесса гласит: тепловой эффект реакции зависит только от природы и состояния исходных веществ и конечных продуктов и не зависит от пути, по которому реакция протекает.
C+1/2O2=CO+ Q1
CO+1/2 O2=CO2+Q2
C+O2=CO2+Q
Q= Q1+Q2
1 следствие из закона Гесса: тепловой эффект реакции равен сумме теплот образования продуктов реакции минус сумма теплот образования исходных веществ.
Q=∑nQобр.пр.- ∑nQобр.исх.
2 следствие из закона Гесса: тепловой эффект реакции равен сумме теплот сгорания исходных веществ минус сумма теплот сгорания продуктов реакции.
Q=∑nQсгор.пр.- ∑nQсгор.исх.
Стандартной теплотой образования называется тепловой эффект образования 1 моль сложного вещества из простых веществ при стандартных условиях.
Стандартной теплотой сгорания называется тепловой эффект сгорания 1 моль органического вещества до Co2 и H2O при стандартных условиях, а если речь идет о неорганических веществах, то указываются степени окисления продуктов сгорания.
-
Обратимые и необратимые по направлению реакции. Понятия о химическом равновесии. Принцип Ле-Шателье.
Состояние реагирующих веществ, при котором скорость прямой реакции равна скорости обратной реакции называется состоянием химического равновесия. Состояние химичесчкого равновесия характеризуется константой равновесия K. Так, для реакции H2+I2=2HI
K=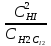
Для обратимой реакции
V1=K1[A]a[B]b
V2=K2[C]c[D]d
В 1884г. Французский ученый Ле-Шателье сформулировал принцип подвижного равновесия: при изменении каких-либо параметров системы, находящейся в химическом равновесии, происходит смещение его в направлении, при котором уменьшается влияние этого изменения.
