
химия биополимеров
.pdf
При проведении анионной полимеризации ε−капролактама при высокой температуре вначале образуются полимеры с высокой ММ, которая при дальнейшем нагревании реакционной смеси уменьшается и достигает равновесного значения. В результате изменяется ММР полимера, обусловленное реакцией переамидирования между растущими и “мертвыми“ цепями полиамида.
П о л и м е р и з а ц и я ε−к а п р о л а к т а м а в п р и – с у т с т в и и в о д ы. Полимеризация ε−капролактама в присутствии инициатора (вода, 2-аминокапроновая кислота или бензойная кислота) является типичной ступенчатой реакцией полиамидирования. В этом случае концевые группы образующейся макромолекулы являются остатками молекул инициатора.
Инициирование:
Рост цепи:
61

В результате реакции образуется поли-ε−капролактам (капрон). Значение ММ образующегося полимера возрастает с увеличением конверсии и уменьшается в результате гидролиза амидной связи.
− СО −NH − + H2O −NH2 + − СОOH
Повышение температуры увеличивает скорость гидролиза и уменьшает ММ полимера. При этом скорость полимеризации возрастает. Величину ММ полимера можно регулировать путём добавления небольших количеств соединений, способных к реакции переамидирования с цепями полиамидов.
Характерной особенностью полимеризации циклических соединений, отличающей её от цепной полимеризации и поликонденсации, является то, что превращение мономеров в линейные полимеры происходит без возникновения новых типов химических связей. Например, связь −СО−NH−, разрывающаяся при расщеплении кольца у ε−капролактама, заменяется точно такой же связью между мономерными звеньями в макромолекуле.
Реакция Метатезиса Заслуживает внимания следующая реакция полимеризации
циклических соединений, которая называется реакцией Метатезиса:
Здесь W − вольфрамовый катализатор.
62
Под действием вольфрамового катализатора из двух молекул циклоолефина образуется через переходное состояние одна молекула циклоолефина. Последняя может полимеризоваться за счёт разрыва σ−связи с образованием полимера, в каждом мономерном звене которого содержатся две двойные связи.
2.2. Поликонденсация
Поликонденсация является эффективным методом получения ряда промышленных полимеров и, в частности, волокнообразующих – полиамидов, полиэфирных смол, лавсана.
Поликонденсация – это процесс образования полимеров из двухили полифункциональных соединений, который сопровождается выделением побочного низкомолекулярного вещества (вода, спирты, галогенводороды и др.)
Пример, синтез сложного полиэфира из гликоля и дикарбоновой кислоты
nHO-R-OH + nHOOC-R/-COOH → [-O-R-O-OC- R/-CO-]n + 2n H2O
При поликонденсации образование полимера идет за счет взаимодействия функциональных групп. Реакция протекает по ступенчатому механизму (т.е. последовательными актами) и рост цепи протекает очень медленно (в отличие от быстрого роста при цепной полимеризации). При выделении низкомолекулярных побочных продуктов элементный состав полимера не соответствует составу исходных мономеров.
63
Классификация и терминология
• В зависимости от числа участвующих в реакции мономеров различают гомополиконденсацию и гетерополиконденсацию. Гомополиконденсация – реакция с участием одного мономера:
n HO-R-COOH → [-O-R-CO-]n + nH2O
Гетерополиконденсация – это реакция с участием двух мономеров, у которых функциональные группы одного мономера реагируют с функциональными группами другого мономера
nHO-R-OH + nHOOC-R/-COOH → [-O-R-O-OC- R/-CO-]n + 2n H2O
Сополиконденсацией называется реакция, в которой помимо мономеров, необходимых для реакции, участвует ещё один мономер:
n H2N-R-NH2 + 2n HOOC-R/-COOH + n H2N-R//-NH2 → → [-HN-R-NH-OC- R/-CO-HN-R//-NH-OC- R/-CO-]n + 4nH2O
• В зависимости от участия одинаковых или различных функциональных групп различают гомофункциональную и гетерофункциональную поликонденсацию.
Гомофункциональная - реакция с участием одинаковых функциональных групп:
n HO-R-OH + n HO-R-OH → [-O-R-]n + n H2O
Гетерофункциональная – реакция с участием различных функциональных групп:
n HO-R-OH + n HOOC-R/-COOH → [-O-R-O-OC- R/-CO-]n + 2n H2O
64
•В зависимости о числа функциональных групп у мономеров получаются различные продукты: линейные (если участвуют
вреакции две группы) и трехмерные (при участии трёх или полифункциональных мономеров).
•Если поликонденсация сопровождается циклизацией, то процесс называется полициклоконденсация.
Взависимости от обратимости реакции различают равновесную (обратимая) и неравновесную (необратимая) поликонденсацию. При обратимой поликонденсации полимер взаимодействует с низкомолекулярным веществом.
Обратимость реакции характеризуется значениями константы равновесия
К= |
[X ][Z ] |
, |
(33) |
|
[A][B] |
||||
|
|
|
где [A] и [B] – соответственно концентрации функциональных групп, [X] и [Z] – соответственно концентрации образовавшихся при поликонденсации связей и побочного продукта.
Для обратимых реакций значения К находятся в пределах до100, а для необратимых значения К≥1000.
Мономеры при поликонденсации делят на три группы:
1) мономеры с одинаковыми функциональными группами, способными реагировать между собой:
n HO-R-OH + n HO-R-OH → [-O-R-]n + n H2O
2) мономеры с одинаковыми функциональными группами, неспособными реагировать между собой, но способными реагировать с функциональными группами другого мономера:
n H2N-R-NH2 + m HOOC-R/-COOH → [-HN-R-NH-OC-R/-CO-]n + 2n H2O
65

3) мономеры с различными функциональными группами, способными реагировать между собой:
n H2N-R-COOH → [-HN-R-CO-]n + nH2O
При поликонденсации следует учитывать влияние различных сопутствующих реакций.
Процессы сопутствующие поликонденсации
Сопутствующие основному процессу реакции могут подавлять основную реакцию, ухудшать качество полимера и увеличивать расход сырья, т.е. их роль отрицательная. По природе сопутствующие процессы разделяют на физические и химические.
Кфизическим сопутствующим процессам относят:
•исключение функциональных групп из реакции вследствие самопроизвольного выпадения полимера в осадок,
•блокирование функциональных групп молекулами растворителя,
•повышение вязкости реакционной системы и др.
Кхимическим сопутствующими процессам относят:
•нежелательные реакции функциональных групп с примесями, растворителями, монофункциональными добавками. Например
•химические превращения функциональных групп вследствие побочных реакций с участием примесей. Например:
1)разложение функциональных групп
HOOC-R/-COOH → 2CO2 + НRH
66

2) видоизменение функциональных групп
ClOC-R-COCl + H2O → ClOC-R-COOH + HCl
Реакции осложняющие поликонденсацию
Осложняющими поликонденсацию являются реакции циклизации и деструкции макромолекул.
Циклизация. В зависимости от механизма процессы циклизации разделяют на внутри- и межмолекулярные. Внутримолекулярная циклизация происходит при взаимодействии функциональных групп, принадлежащих одной молекуле мономера.
Например, побочная реакция циклизации при синтезе полиамида из аминокислоты:
Межмолекулярная циклизация происходит при взаимодействии функциональных групп различных молекул.
Например: |
|
|
|
HO-СH2-СН2-OH |
O-СH2-СН2-O |
|
|
+ |
→ \ |
⁄ |
+ 2 С2H5ОН |
H5С2ОOС-R/-СОOС2H5 |
O=С―R/―С=О |
|
|
Легко циклизующимися являются соединения, которые образуют 5-7 членные циклы, но возможно образование 20-40 членных циклов из промежуточных продуктов поликонденсации.
Осложняющая реакция циклизации протекает в случае обратимой поликонденсации - при взаимодействии полимеров с низкомолекулярными побочными продуктами.
Деструкция макромолекул является также осложняющей реакциeй при поликонденсации. Деструкция может протекать при взаимодействии продуктов поликонденсации с низкомолекуляр-
67
ными соединениями (см. Тема 3. Химические превращения полимеров. Раздел. Химическая деструкция).
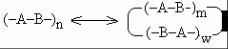
В случае поликонденсации необходимо учитывать не только возможность протекания побочных конкурирующих реакций, но и циклизацию. Так, гетероциклические полимеры в разбавленных растворах могут деструктироваться с образовыванием макроциклических соединений за счёт обменных реакций между звеньями полимерных цепей:
где n = m +w.
Соотношение скоростей основной и побочной реакций определяет молекулярные характеристики полимера (структуру макромолекул, ММ, ММР), содержание примесей и др. Это соотношение зависит от строения мономеров, степени их очистки, условий синтеза.
Внутримолекулярную циклизацию можно предотвратить увеличением концентрации мономеров и снижением температуры реакции. Деструкцию предотвращают удалением низкомолекулярного продукта из зоны реакции.
Кинетика поликонденсации
При поликонденсации удобно выражать скорость процесса через концентрации реагирующих функциональных групп. В случае мономеров взятых в эквимолярных количествах [A]=[B] уравнение поликонденсации имеет вид
– |
d[A] |
= – |
d[B] |
= k[A][B] = k[A]2 |
(34) |
||
dt |
|
dt |
|
||||
Здесь [A] и [B] – концентрации функциональных групп, k – константа скорости реакции.
После подстановки в уравнение (34) начальной концентрации функциональных групп [A]0, конверсии (X) и интегрирования получается
68

k t [A]0 = |
X |
|
(35) |
1− X |
|||
Уравнение (35) соблюдается для |
необратимых процессов и |
||
для начальных стадий обратимых процессов. Уравнение (35) можно преобразовать к виду:
|
|
|
P = k t [A]0 |
(36) |
|
Здесь P - среднечисловая степень поликонденсации.
Согласно уравнению (36), для получения полимеров с высокой ММ необходимо увеличивать исходную концентрацию мономера и проводить поликонденсацию до глубоких конверсий.
Кинетические параметры необратимой и обратимой поликонденсации различаются:
•для необратимых процессов характерны высокие скорости и малые энергии активации, эти процессы экзотермичны,
•для обратимых процессов характерны малые скорости и большие энергии активации.
Для обратимой поликонденсации соблюдается уравнение
|
= |
K |
, |
(37) |
P |
||||
|
|
[Z ] |
|
|
Здесь K – константа равновесия, [Z] – концентрация низкомолекулярного продукта.
Из уравнения (37) следует, что для получения высокомолекулярного продукта необходимо уменьшать концентрацию низкомолекулярного продукта Z (путём применения вакуума, проведения реакции при высоких температурах и в тонком слое реагирующих мономеров).
ММ продукта поликонденсации зависит от конкуренции основной реакции с параллельно протекающими процессами, приводящими к дезактивации реагирующих групп).
69

Рис. 11. Зависимость степени полимеризации ( ) при линейной ступенчатой поликонденсации
) при линейной ступенчатой поликонденсации
от глубины превращения функциональных групп (X).
Факторы влияющие на молекулярную массу продуктов поликонденсации
Такими факторами являются: глубина превращения мономеров в полимер, соотношение исходных мономеров, концентрация регуляторов ММ, условия синтеза.
1) Глубина превращения мономеров в полимер.
Средняя степень полимеризации образующегося полимера
при поликонденсации определяется выражением: |
|
|||||||
|
|
= |
|
|
1 |
|
, |
(38) |
|
P |
|
|
|
||||
|
1 |
− |
X |
|||||
|
|
|
|
|
||||
где Х – конверсия. Согласно приведенному уравнению, чем глубже прошла реакция поликонденсации (Х→1, т.е. 100%), тем больше размер макромолекул и их ММ.
Зависимость степени полимеризации от глубины поликонденсации представлена на рис. 11. Видно, длина макромолекул в течение реакции непрерывно нарастает со временем. Эта закономерность поликонденсации отлична от закономерности цепной полимеризации, когда со временем нарастает степень превращения мономера, а ММ не изменяется. Характерной особен-
70
