
- •Тема 4.
- •Раздел1.
- •1.1 Характеристика углеводов организма.
- •1. 2 Значение и биологическая роль углеводов организма
- •1. 3 Углеводы пищи, нормы и принципы нормирования их суточной пищевой
- •1.4 Всасывание углеводов
- •1.5 Нарушение переваривания и всасывания углеводов
- •1). Наследственные и приобретенные дефекты ферментов, участвующих в переваривании.
- •1. 6 Углеводы пищи и полость рта
- •1. 6 Усвоение моносахаридов тканями
- •1.7 Взаимные превращения моносахаридов в клетке.
- •Наследственное заболевание галактоземия
- •Раздел 2 Энергетический путь обмена глюкозы
- •2.1 Гликолитический путь окисления глюкозы
- •2.2. Регуляция гликолитического пути
- •2.3 Взаимосвязь гликолиза и цикла Кребса.
- •2.3.1 Превращение пвк – АцКоА
- •2.3.2 Эффект Пастера.
- •III. Пластические пути обмена гл-6-ф
- •3.1 Пентозофосфатный цикл( шунт) ( пфц)
- •IV Регуляция углеводного обмена
- •4.1 Гипогликемия.
- •4.2 Гипергликемия
- •Инсулин
- •4.4 Синтез и распад гликогена( гликогенолиз)
- •4.5. Инсулин
- •4.5.1 Строение инсулина
- •Биосинтез инсулина
- •Регуляция синтеза и секреции инсулина
- •Биологические функции инсулина
- •4.5.5 Действие инсулина на метаболизм.
- •4.5.6.Механизм действия инсулина на клеточном уровне.
- •4.6. Контринсулярные гормоны : глюкагон, катехоламины, кортизол
- •4.6.1. Глюкагон
- •4.6.2. Адреналин
- •4.6.3 Глюкокортикоиды ( кортизол)
- •V. Патология углеводного обмена
- •5.1 Диабет
- •Лабораторная диагностика показателей углеводного обмена.
- •Вопросы по теме: ”Углеводы”
- •Тестовые задания для самопроверки усвоения темы
- •1. Лабораторное исследование выявило высокую амилазную активность крови и мочи . Этот энзимодиагностический тест указывает на:
- •3. О функции фермента фосфатаза можно сказать, что он осуществляет:
- •4. Фермент гл-6-фосфатаза содержится в тканях:
- •5. Транспорт глюкозы в клетку осуществляется одновременно с ионом
- •8. Качественная реакция обнаружения фруктозы названа по имени автора:
- •10. Тип рецептора глют-4 характерен для клеток ткани:
- •12. Транспортер глюкозы, наиболее чувствительный к инсулину, можно обозначить как:
- •Раздел 2. Пути обмена глюкозы в клетке
- •14. Место локализации ферментов гликолиза в клетке
- •16. Выберите главный регуляторный фактор гликолиза
- •17. Для синтеза атф в анаэробных условиях в организме человека используются субстраты:
- •Раздел 3 Регуляция уровня глюкозы в крови
- •39. Взаимные связи гормонов инсулина и глюкагона можно выразить отношением( 2 ответа) :
- •40. В процессе превращения проинсулина в инсулин выделяется пептид, который носит название:
- •43. Гипергликемия сопровождается :
- •44. Гипогликемия сопровождается :
- •46. После проведения теста на толерантность к глюкозе в моче пациента была обнаружена глюкоза. Сделайте вывод:
- •48. Укажите ион, снижение концентрации в крови которого препятствует нормальной секреции инсулина:
- •Приложение
2.3.2 Эффект Пастера.
Включение ПВК в аэробный путь окисления происходит только в том случае, если клетка
потребляет кислород, « дышит». Впервые снижение образования молочной кислоты в присутствии
кислорода заметил Л. Пастер.
Эффект Пастера –это снижение в клетке скорости потребления глюкозы и накопления лактата в присутствии кислорода |
Эффект Пастера объясняется наличием конкуренции за кофермент НАДН между ферментами аэробного тканевого дыхания в митохондриях и анаэробной ЛДГ.
Без кислорода митохондрии не потребляют ПВК и НАДН. ПВК и НАДН остаются в цитоплазме и используются для образования лактата с участием ЛДГ.
В присутствии кислорода митохондрии «выкачивают» ПВК и НАДН из цитоплазмы, прерывая реакцию образования лактата.
2.3.7 Механизмы взаимосвязи аэробного гликолиза и окислительного фосфорилирования
Кроме соотношения АДФ/ АТФ, регуляторным действием на скорость реакций гликолиза и цикла Кребса оказывает соотношение НАД +/ НАДН , цитрат и жирные кислоты.
Угнетение окисления глюкозы на уровне пируваткиназы при повышении концентрации жирных кислот направлено на сбережение глюкозы в клетке в условиях, когда клетка обеспечена другим субстратом, способным образовать также АцКоА. ( смысл цикла Рендла, или другое название цикла глюкоза-жирные кислоты).
Надо помнить, что Гл-6-Ф- более универсальный энергетический субстрат по сравнению с жирными кислотами: из углеводов образуются АцКоА и ЩУК, а из природной жирной кислоты - только АцКоА. При аэробном окислении из 1 глюкозы образуется 38 АТФ, а в анаэробном гликолизе 2 АТФ, соответственно, для образования достаточного количества АТФ в аэробных условиях необходимо глюкозы в 19 раз меньше, чем в анаэробных условиях |
Схема: связь реакций гликолиза с циклом Кребса
.
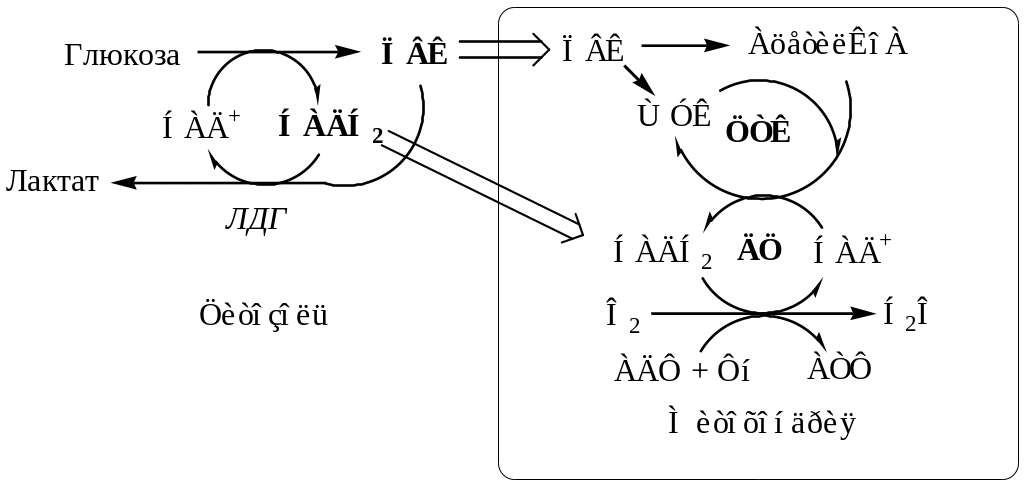
Сокращения: ЦТК- цикл Кребса
ДЦ- дыхательная цепь
III. Пластические пути обмена гл-6-ф
3.1 Пентозофосфатный цикл( шунт) ( пфц)
Пентозофосфатный путь обмена глюкозы относят к анаэробным процессам. Это филогенетически древний путь, подобный набор реакций в растениях встречается при фотосинтезе углеводов. В организме человека ПФЦ является главным поставщиком пентоз и восстановленного пиридиннуклеотида НАДФН, у которого множество функций.
Ферменты ПФЦ локализованы в эритроцитах, лейкоцитах, в цитозоле клеток слюнных железах, коры надпочечников, жировой ткани, печени, молочной железы, семенников, кожи.
Процесс протекает в цитозоле клетки без участия О2 и включает в себя две стадии: окислительную и неокислительную.
Реакции окислительной стадии
Глюкозо-6 -фосфат окисляется глюкозо-6-фосфат ДГ, образуется 6-ф-глюконолактон, который гидролизуется с участием фермента лактоназы.
При окислении полученной 6-фосфоглюконовой кислоты происходит декарбоксилирование, образуются пентоза - рибулозо-5-ф и НАДФН.
Гл-6-ф-ДГ
1. Гл-6-ф + НАДФ+ ————> НАДФН + Н ++ 6-ф-глюконолактон
лактоназа
2. 6-ф-глюконолактон-6-ф + Н2О————> 6-ф-глюконовая кислота
6-ф—глюконат ДГ
3. 6-ф-глюконовая кислота + НАДФ————>НАДФН + Н ++СО2 + рибулозо-5-ф
Рибулозо-5-ф изомеризуется, по мере необходимости, в рибозо-5-ф или ксилулозо-5ф для обеспечения второго неокислительного этапа.
Неокислительная стадия
На неокислительной стадии действуют ферменты класса лиаз- транскетолаы и трансальдолазы , в их составе кофермент- тиаминпирофосфат ( витаминВ-1).
Этот этап активируется в том случае, когда ПФЦ «нарабатывает» НАДФН для различных пластических и других целей, и необходимо утилизовать полученные одновременно пентозы, поскольку накопление пентоз по принципу обратной связи ингибирует активность Гл-6-Ф-ДГ и начальную реакцию окисления.
Общее уравнение ПФЦ:
6 Гл-6-ф + 12 НАДФ++7 Н2О ——> 6 СО2 + 12 НАДФН+ Н+ + 5 гл-6-ф + Ф
( 36 атомов углерода) ( 6 атомов углерода + 30 атомов углерода= 36 атомов))
Значение ПФЦ
1. Главный источник образования НАДФН. Потребителями НАДФН являются :
- система микросомального окисления( МСО)
- антиоксидантная защита в процессах образования активных форм кислорода и перекисного окисления липидов
-защита гемоглобина от превращения в метгемоглобин, неспособный транспортировать
кислород ( метгемоглобинредуктазная система )
- активация витамина Д в процессе реакций гидроксилирования
- пластический обмен- синтез жирных кислот, холестерина,
- метаболизм пуриновых соединений.
2.Синтез пентоз, необходимых для образования нуклеотидов, динуклеотидов( АТФ, ГТФ, НАД, ФАД и др.)и нуклеиновых кислот.
3 Синтез 3-ФГА. Связь с гликолизом осуществляется через 3-ф-ГА- эта связь объясняет термин «шунт». Очень важна в обеспечении метаболизма в эритроците. Из 3-ФГА образуется
3- фосфоглицерол- субстрат для синтеза триглицеридов и фосфолипидов.
Причины нарушения ПФЦ:
1.Недостаток тиамина в продуктах питания или нарушение его тканевого обмена.
2. Генетические дефекты Гл-6-ф-ДГ ( описано более 250 патологических изоформ). Особенно опасно нарушение в эритроцитах :
- снижается концентрация восстановленного антиоксиданта глутатиона
- увеличивается количество активных форм кислорода
-возникает нарушение пластичности мембран эритоцитов - появляется риск гемолиза эритроцитов
Клинические проявления дефекта Гл-6-ф-ДГ
Характерны приступы гемолитической анемии. Возникают под влиянием провоцирующих агентов: некоторые лекарственные соединения(сульфаниламиды, анальгетики, противомалярийные и др.), из пищевых продуктов бобовые(фасоль, горох),
