
- •Аденин Гуанин (стр.421)
- •Трипептид серин-аспарагиновая кислота – фенилаланин
- •Наиболее важные моносахариды карбонильная группа альдегидная кетонная
- •Лизин (2,6-диаминогексановая кислота) — алифатическая, незаменимая аминокислота. Содержит дополнительную аминогруппу, из-за чего у нее выраженные основные свойства.
- •In vivo ак используются для синтеза пептидов, полипептидов и белков.
Билет №1
-
Химические свойства, стереоизометрия аминокислот на примере лизина (образование биполярного иона, амфотерность, декарбоксилирование, область изоэлектрической точки)
-
Полисахариды соединительной ткани – гликозаминогликаны: особенности структуры, свойств, типы гликозидных связей, биологическое значение на примере гиалуроновой кислоты и хондроитин сульфатов.
-
Строение, номенклатура, типы связей, условия гидролиза, биологическое значение нуклеозидов пуринового и пиримидинового рядов.
-
Лизин (2,6-диаминогексановая кислота) — алифатическая, незаменимая аминокислота. Содержит дополнительную аминогруппу, из-за чего у нее выраженные основные свойства.
Химическая формула:
Химические свойства:
-
Аминокислоты – амфотерные вещества, в твердом состоянии – всегда в виде биполярного, двухзарядного иона – «цвиттер-иона». В растворе возникает катион аминокислоты с зардом +1. Изоэлектрическая точка в щелочной среде: лизин (pI=9,74)
-
Величина и знак заряда иона зависит от ph-среды.
-
Лизин обладает всеми химическими свойствами, присущим карбоновым кислотам и аминам
-
in vivo АК используются для синтеза пептидов, полипептидов и белков.
-
АК проявляют амфотерные свойства, поскольку в их составе присутствует карбоксильная группа, проявляющая кислотные свойства, и амино-группа – основные свойства.
-
Декарбоксилирование:
-
Гликозаминогликаны – высокомолекулярные соединения, образованные двумя видами моносахаридов: уроновыми кислотами (глюкуроновой и идуроновой) и N-ацетилированными аминосахарами – 2-N-ацетилглюкозамином и 2-N-ацетилгалактозамином.
Гетерополисахариды – компоненты межклеточного вещества, матрикса соединительной ткани. Наибольшее значение имеют гиалуроновая кислота, хондроитинсерная кислота, гепарин.
Гиалуроновая кислота состоит из D-глюкуроновой кислоты (бета 1-3) и N-ацетил-D-глюкозамина (бета 1-4). Широко распространена в живой природе: присутствует у микроорганизмов, в тканях и жидкостях животных и человека (стекловидное тело глаза, суставная жидкость, кожа, пуповина). Служит смазочным материалом в суставах, придает тканям эластичность и устойчивость к сжатию. Выполняет барьерную функцию.
ХС – различают два типа: ХС-4 и ХС-6 (в зависимости от положения сульфогруппы).
ХС-6 состоит из D-глюкуроновой кислоты (бета 1-3) и N-ацетил-D-галактозамина-6 сульфата (бета 1-4). Содержатся в хрящах, сухожилиях, костях, роговице глаза.
Значение: Применяются как лекарственные препараты при патологии соединительной ткани.
-
Нуклеозиды — это N-
 -гликозид,
у которого неуглеводная часть является
азотистым основанием, производным
пиримидина или пурина.
-гликозид,
у которого неуглеводная часть является
азотистым основанием, производным
пиримидина или пурина.
В зависимости от того, какой моносахарид входит в состав нуклеозида, их подразделяют на два вида – рибозиды и дезоксирибозиды.
В кислой среде in vitro нуклеозиды распадаются на компоненты (пуриновые легче, чем пиримидиновые). Пурины прикреплены к альдопентозе атомом N-9, пиримидин – атомом N-1. Пуриновые гидролизуются легко, пиримидиновые – труднее.
Значение: При лечении некоторых опухолевых заболевай в качестве лекарственных средств используются систематические производные пиримидинового и пуринового рядов.
Билет №3
-
Природные аминокислоты: классификация по биологической ценности, значение. Использование аминокислот в медицине.
-
Строение, физические свойства, биологическое значение альдогексоз: глюкозы и галактозы. Энантиомерия и цикло-оксотаутомерия на примере глюкозы. Запишите структурные формулы глюкозо-1-фосфата и глюкозо-6-фосфата.
-
Строение, номенклатура, типы связей, условия гидролиза, биологическое значение нуклеотидов пиримидинового ряда.
-
По биологическому признаку природные аминокислоты классифицируют на:
-
заменимые (синтезируются в клетках человека): аланин, аргинин, аспарагиновая кислота, глицин, глутаминовая, кистидин, пролин. серин, тирозин, цистеин.
-
незаменимые: валин, изолейцин, лейцин, лизин, метионин, треонин, триптофан, фенилаланин.
Медико-биологическое значение АК:
-
участвуют в биосинтезе нейромедиаторов и гормонов
-
из серина – нейромедиатор ацетилхолин
-
из фенилаланина или тирозина – медиатор норадреналин и гормоны адреналин, тироксин
-
глицин, глутаминовая – нейромедиаторные функции
-
аспарагиновая кислота – необходима в синтезе азотистых оснований
-
глутаминовая и аспарагиновая – в обезвреживании аммиака
-
в условиях углеводного голодания из АК синтезируется глюкоза
-
АК используются в качестве лекарственных средств: глутаминовая, метионин, глицин, цистеин, триптофан.
-
Состав гексозы C6(H2O)6. Альдогексозы содержат 4 хиральных атома, образуют 16 стереоизомеров (8 принадлежат Д-ряду, 8 – Л-ряду)
Физические свойства: твердые кристаллические вещества, хорошо растворимые в воде, плохо в органических растворителях. Сладкие на вкус.
Глюкоза Галактоза
Биологическое значение:
-
Глюкоза — основной продукт фотосинтеза.
-
В организме человека и животных глюкоза является основным и наиболее универсальным источником энергии для обеспечения метаболических процессов.
-
Глюкоза участвует в образовании гликогена, питании тканей мозга, работающих мышц.
-
При гипоксии – единственное вещество, обеспечивающее мышечную деятельность.
-
Запасается в составе олигосахарида сахарозы или полисахарида крахмала.
-
Подвергается «брожению»
-
Применяется в медицине.
Галактоза при окислении образует галактоновую, галактуроновую и слизевую кислоты.
Альдогексозы in vivo шестичленные пиранозные циклы.
Энантиомерия и цикло-оксотаутомерия на примере глюкозы:
Глюкозо-1-фосфат Глюкозо-6-фосфат
-
Нуклеиновые основания пиримидинового ряда:
урацил тимин цитозин
Нуклеотиды – фосфаты нуклеозидов.
Химический состав: азотистое основание + пентоза + фосфорная кислота
Для связывания трех компонентов в молекуле нуклеотида используются сложноэфирная и N-гликозидная связи.
Нуклеотиды можно рассматривать с двух сторон: как эфиры нуклеозидов (фосфаты) и как кислоты (в связи с наличием остатка фосфорной кислоты).
За счет фосфатного остатка нуклеотиды проявляют свойства двухосновной кислоты и в физиологических условиях при ph=7 находятся в полностью ионизированном состоянии.
Для нуклеотидов используют два вида названия. Одно – включает наименование нуклеозида с указанием положения в нем фосфатного остатка, другое строится с добавлением суффикса –иловая кислота к названию остатка пиримидинового основания.
Нуклеотиды играют чрезвычайно важную роль в жизнедеятельности клетки:
-
нуклеозиддифосфаты и нуклеозидтрифосфаты относятся к высокоэнергетическим (макроэргическим) соединениям.
-
нуклеозидтрифосфаты участвуют в синтезе нуклеиновых кислот
Билет №4
-
Природные аминокислоты, классификация по сторению. Их амфотерные свойства, примеры.
-
Написать формулу трипептида цис+ что то там (вроде арг) + глу. Виды связи в третичной структуре белка.
-
Формулы д-рибозы, л-рибозы, д-рибулозы, 2-дезокси-д-рибозы. Их биологическое значение. Цикло-оксо-таутомерия на примере д-рибозы.
-
Важнейшие а-АК - H2N-CH(R))-COOH
Алифатические
Глицин
Аланин
Валин*
Содержащие ОН-группу
Серин
Треонин*
Содержащие СООН-группу
Аспарагиновая
Глутаминовая
Содержащие CONH2-группу
Аспарагин
Глутамин
Содержащие NH2-группу
Лизин*
Аргинин
Серосодержащие
Цистеин
Метионин*
Ароматические
Фенилаланин*
Тирозин
Гетероциклические
Триптофан*
Гистидин
АК проявляют амфотерные свойства, поскольку в их составе присутствует карбоксильная группа, проявляющая кислотные свойства, и амино-группа – основные свойства.
стр.327
-
В стабилизации третичной структуры белка принимают участие:
-
ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
-
ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
-
водородные связи;
-
гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
Трипептид цис-арг-глу
-
д-рибоза л-рибоза д-рибулоза 2-дезоксирибоза
Биологическое значение:
-
Рибоза входит в состав рибонуклеиновой кислоты, аденозина, нуклеотидов и других биологических важных веществ.
-
Является компонентом РНК и используется при генетической транскрипции.
-
Производная рибозы — дезоксирибоза является компонентом ДНК.
-
Рибоза является компонентом АТФ и некоторых других веществ, участвующих в метаболизме.
-
Эфиры рибулозы и фосфорной кислоты — рибулозо-5-фосфат и рибулозо-1,5-дифосфат участвуют в важных процессах обмена веществ; распаде углеводов (пентозофосфатный цикл), а также их образовании в зелёных растениях при фотосинтезе.
-
Дезоксирибоза входит в состав ДНК, вместе с азотистым основанием и остатком фосфорной кислоты образуя мономерную единицу дезоксирибонуклеиновой кислоты — нуклеотид.
Цикло-оксо-таутомерия на примере д-рибозы:
Билет №5
-
Денатурация белков, виды, причины, денатурирующие факторы, биологическое значение.
-
Целлюлоза; химический состав, строение, тип химсвязей, условия гидролиза, биологическое значение.
-
Строение , номенклатура, типы связей, условия гидролиза, биологическое значение нуклеотидов пуринового ряда.
-
Денатурация – разрушение макроструктуры белка.
Виды:
Денатурация может быть обратимой и необратимой. Часто видимым следствием денатурации белка является осаждение белка из раствора.
Причины:
Практически любое заметное изменение внешних условий, например, нагревание или обработка белка щелочью приводит к последовательному нарушению четвертичной, третичной и вторичной структур белка.
Денатурирующие факторы:
-
повышение температуры
-
действие сильных кислот и щелочей, солей тяжелых металлов, некоторых растворителей (спирт).
-
изменение ph-среды
-
присутствие ПАВ
-
физические факторы (УФ-излучение, рентгеновское излучение, радиация)
-
Целлюлоза (клетчатка)— (C6H10O5)n, белое твердое вещество, нерастворимое в воде.
Строение:
Целлюлоза построена из остатков
Д-глюкопиранозы, звенья которой в
полисахаридной цепи связаны
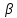 (1-4)
гликозидными связями. Биозный фрагмент
целлюлозы составляет собой целлобиозу.
(1-4)
гликозидными связями. Биозный фрагмент
целлюлозы составляет собой целлобиозу.
Целлюлоза представляет собой длинные нити, содержащие 2500-12000 остатков глюкозы, без боковых ответвлений. Эти нити соединены между собой множеством водородных связей, что придает целлюлозе большую механическую прочность, при сохранении эластичности.
Целлюлоза труднее, чем крахмал подвергается гидролизу, лишь при высокой температуре и в присутствии конц.H2SO4. Гидролиз протекает ступенчато. Конечный продукт Бета-D-глюкоза.
Целлюлоза не расщепляется обычными ферментами желудочно-кишечного тракта, но она является необходимым веществом для нормального пищеварения.
Значение: Полисахарид, главная составная часть клеточных оболочек всех высших растений. Обладает высокой механическое прочностью и выполняет роль опорного материала растений. Является важным сырьем для ряда отраслей промышленности.
-
Аденин Гуанин (стр.421)
Аденин — азотистое основание, аминопроизводное пурина (6-аминопурин). Образует две водородных связи с урацилом и тимином (комплементарность).
Хорошо растворим в воде, особенно горячей, с понижением температуры воды, растворимость аденина в ней падает. Плохо растворим в спирте, в хлороформе, эфире, а также в кислотах и щелочах — не растворим.
Значение: Аденин входит в состав многих жизненно важных для живых организмов соединений, таких как: аденозин, аденозинфосфотазы, аденозинфосфорные кислоты, нуклеиновые кислоты, адениновые нуклеотиды и др. В виде этих соединений аденин широко распространен в живой природе.
Гуанин, Г, G — азотистое основание, аминопроизводное пурина (6-окси-2-аминопурин), является составной частью нуклеиновых кислот. В ДНК, при репликации и транскрипции образует три водородных связи с цитозином (C) (комплементарность).
Химическая формула — C5H5N5O. Проявляет основные свойства. Реагирует с кислотами и щелочами с образованием солей. При действии на гуанин HNO2 (азотистой кислоты) образуется ксантин. Хорошо растворим в кислотах и щелочах, плохо растворим в эфире, спирте, аммиачных и нейтральных растворах, нерастворим в воде.
Значение: Входит в состав нуклеиновых кислот. Впервые был выделен из гуано, из-за чего и получил своё название.
Билет №6
-
Реакции декарбоксилирования природных аминокислот на примере тирозина, триптофана, гистидина и глутаминовой кислоты. Биологическое значение этих реакций.
-
Составьте структурную формулу трипептида из аминокислот серин - аспарагиновая кислота – фенилаланин. Какие виды связей в третичной структуре белка могут образовываться с участием радикалов этих аминокислот?
-
Гепарин: особенности структуры, типы гликозидных связей, свойства, биологическое значение, использование в медицине.
-
Процесс отщепления карбоксильной группы аминокислот в виде CO2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилированию в животных тканях, образующиеся продукты реакции – биогенные амины (т.н. "Трупные яды") - оказывают сильное фармакологическое действие на множество физиологических функций человека и животных.
Декарбоксилирование тирозина:
Декарбоксилирование триптофана:
Декарбоксилирование гистидина:
Декарбоксилирование глутаминовой кислоты:
-
Трипептид серин-аспарагиновая кислота – фенилаланин
В стабилизации третичной структуры белка принимают участие:
-
ковалентные связи (между двумя остатками цистеина — дисульфидные мостики);
-
ионные связи между противоположно заряженными боковыми группами аминокислотных остатков;
-
водородные связи;
-
гидрофильно-гидрофобные взаимодействия. При взаимодействии с окружающими молекулами воды белковая молекула «стремится» свернуться так, чтобы неполярные боковые группы аминокислот оказались изолированы от водного раствора; на поверхности молекулы оказываются полярные гидрофильные боковые группы.
-
Гепарин — кислый серосодержащий гликозаминогликан,состоящий из глюкуроновой кислоты (
 и N-ацетилглюкозамина;
и N-ацетилглюкозамина;
В клинической практике известен, как вещество, препятствующее свёртыванию крови.
Применяется:
-
для профилактики и терапии тромбоэмболических заболеваний
-
при операциях на сердце и кровеносных сосудах
-
для поддержания жидкого состояния крови в аппаратах искусственного кровообращения и гемодиализа
-
для предотвращения свертывания крови при лабораторных исследованиях.
Синтезируется в тучных клетках, скопления которых находятся в органах животных, особенно в печени, лёгких, стенках сосудов.
Билет №7
-
Химические свойства, стереоизометрия аминокислот на примере глутаминовой кислоты (образование биполярного иона, амфотерность, декарбоксилирование, дезаминирование, область изоэлектрической точки)
-
Строение, физико-химические свойства, классификации, биологическое значение важнейших моносахаридов организма человека. Особая биологическая роль глюкозы.
-
Строение и свойства пиримидина, нумерация атомов в цикле. Строение, свойства и биологическое значение пиримидиновых азотистых оснований нуклеиновых кислот тимина, цитозина, урацила.
-
Глутаминовая кислота (2-аминопентандиовая кислота) — алифатическая аминокислота. Моноаминодикарбоновая, кислая аминоксилота. Содержит дополнительные карбоксильные группы в составе радикала:
Химические свойства:
-
Амфотерные вещество, в твердом состоянии – всегда в виде биполярного, двухзарядного иона – «цвиттер-иона». При растворении происходит диссоциация второй карбоксильной группы, среда раствора становится кислой, а кислота превращается в анион с зарядом -1. Изоэлектрическая точка моноаминодикарбоновых кислот находится в кислой среде.
-
Биполярный ион:
-
Глутаминовая кислота обладает всеми химическими свойствами, присущим карбоновым кислотам и аминам
-
Декарбоксилирование:
-
Дезаминирование:
-
Моносахариды классифицируют относительно количества атомов С (пентозы, гексозы) и наличия карбонильной группы (альдегидной, кетонной)
