
- •Министерство образования российской федерации
- •Череповецкий государственный университет
- •Инженерно -технический институт
- •Кафедра химии
- •Лабораторный практикум
- •По дисциплине
- •Часть 2
- •Титриметрический (объёмный) анализ
- •Определение массовой доли h2so4 в технической серной кислоте
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм выполняемой работы
- •Классификация титриметрических методов
- •5. Обработка результатов
- •Массовая доля серной кислоты, %:
- •Экспериментальные и расчетные данные
- •Плотность водных растворов серной кислоты h2so4
- •6. Контрольные вопросы и задания
- •Окисляемость воды
- •Определение окисляемости воды перманганатометрическим методом
- •2. Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра раствора kMnO4
- •4.2. Анализ природной воды
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •6. Контрольные вопросы и задания
- •Йодометрия
- •Определение содержания аскорбиновой кислоты в фруктовых соках
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •6. Контрольные вопросы
- •Дихроматометрия
- •Определение массовой доли органического углерода в жидких комплексных удобрениях
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра соли Мора
- •Установка титра
- •4.2. Определение углерода органического
- •5. Обработка результатов
- •Экспериментальные и расчетные данные
- •5. Контрольные вопросы и задания
- •Определение хлоридов в водопроводной воде
- •Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Установка титра азотнокислой ртути (II)
- •Установка титра
- •4.2. Определение хлоридов
- •5. Обработка экспериментальных данных Содержание хлоридов в исследуемой воде вычисляют по формуле, мг/дм3:
- •6. Контрольные вопросы и задания
- •Определение кальция и магния в водной вытяжке из почвы
- •2. Сущность метода
- •3. Приборы и реактивы
- •4. Алгоритм определения
- •4.1. Определение суммарного содержания ионов кальция и магния
- •Экспериментальные и расчетные данные
- •Определение содержания кальция
- •2. Сущность метода
- •Приборы и реактивы
- •4. Алгоритм определения
- •5. Обработка результатов
- •6. Контрольные вопросы
- •Литература
- •Содержание Ведение 3
- •162600, Г. Череповец, Советский пр. 8.
5. Обработка результатов
Определяют титр рабочего раствора, в г/см3:
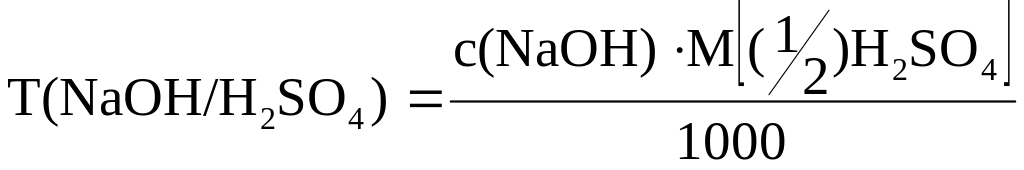
где М[(1/2)Н2SО4] - молярная концентрация эквивалентов серной кислоты, [моль/дм3];
с[(1/2)H2SO4]=
![]()
где V(NaOH)-объём израсходованный на титровоние, см3;
V(H2SO4)- объём взятый на титрование (аликвота), см3.
Массовая доля серной кислоты, %:
![]()
![]() ,
,
где Vк - объём мерной колбы с приготовленным раствором, см3; m - масса навески серной кислоты, г.
Таблица 6
Экспериментальные и расчетные данные
с(NaOH), моль/дм3 |
m, г |
V(NaOH), см3 |
Т(NaOH/H2SO4), г/см3 |
С[(1/2)H2SO4] моль/дм3 |
% |
|
|
|
Vi |
Vср |
|
|
|
|
|
|||||
|
||||||
|
||||||
Таблица 7
Плотность водных растворов серной кислоты h2so4
|
Концентрация |
|
Концентрация |
||||
% |
Моль/л |
г/л |
% |
моль/л |
Г/л |
||
1,800 |
87,69 |
16,09 |
1578 |
1,826 |
92,51 |
17,22 |
1689 |
1,805 |
88,43 |
16,27 |
1596 |
1,827 |
92,77 |
17,28 |
1695 |
1,810 |
89,23 |
16,47 |
1615 |
1,828 |
93,03 |
17,34 |
1701 |
1,815 |
90,12 |
16,68 |
1636 |
1,829 |
93,33 |
17,40 |
1707 |
1,820 |
91,11 |
16,91 |
1659 |
1,830 |
93,64 |
17,47 |
1713 |
1,821 |
91,33 |
16,96 |
1663 |
1,831 |
93,94 |
17,54 |
1720 |
1,822 |
91,56 |
17,01 |
1668 |
1,832 |
94,32 |
17,62 |
1728 |
1,823 |
91,78 |
17,06 |
1673 |
1,833 |
94,72 |
17,70 |
1736 |
1,824 |
92,00 |
17,11 |
1678 |
1,834 |
95,12 |
17,79 |
1745 |
1,825 |
92,25 |
17,17 |
1684 |
1,835 |
95,72 |
17,91 |
1757 |
