
- •Содержание
- •Введение
- •Диссоциация электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Ионное произведение воды
- •Расчет рН сильных кислот и оснований
- •Расчет рН слабых бинарных кислот и оснований
- •Влияние сильных электролитов и одноименных ионов на ионные равновесия в слабых электролитах
- •Буферные растворы
- •Гидролиз солей
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в гомогенных системах»
- •Равновесия в гетерогенных системах
- •Произведение растворимости
- •Задачи на применение условия выпадения осадка
- •Расчет растворимости осадков в присутствии одноименных ионов
- •Расчет растворимости осадка в присутствии разноименных ионов (солевой эффект)
- •Дробное осаждение
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное равновесие
- •Расчет констант равновесия окислительно-восстановительных реакций
- •Расчет окислительно-восстановительного потенциала
- •Вопросы и задачи для самостоятельного решения
- •Равновесия в растворах комплексных соединений
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в реакциях осаждения, комплексообразования и окисления-восстановления»
- •Качественный анализ
- •Вопросы и задачи для самостоятельной работы
- •Гравиметрический анализ
- •Расчет количества осадителя
- •Рассчитаем массу 4 %-ного раствора Na2hpo4:
- •Расчет потерь осадка при промывании
- •Выбор оптимального интервала значений рН
- •Расчёт результатов гравиметрического определения
- •0,0623 Г Ag содержится в 125 мл раствора;
- •Вопросы и задачи для самостоятельного решения
- •Титриметрические методы анализа
- •Способы выражения концентраций растворов
- •Определение фактора эквивалентности
- •Пример 2. Какой объем 0,1 н. Раствора серной кислоты необходимо отмерить для приготовления 100 мл 0,02 н. Раствора?
- •Способы титрования
- •Кислотно-основное титрование
- •Выбор индикатора
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Оксидиметрические индикаторы
- •Вопросы и задачи для самостоятельного решения
- •Комплексонометрическое титрование
- •Выбор индикатора и условий проведения анализа
- •Вопросы и задачи для самостоятельного решения
- •Примеры построения кривых титрования
- •Титрование сильных кислот и оснований
- •Титрование слабой кислоты сильным основанием
- •0,40 Моль/л раствором koh.
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Вопросы и задачи для самостоятельного решения
- •Физико-химические методы анализа
- •Потенциометрия и потенциометрическое титрование.
- •Вольтамперометрия
- •Кулонометрия.
- •Вопросы и задачи для самостоятельного решения
- •Спектроскопические методы анализа
- •Фотометрические методы анализа.
- •Вопросы и задачи для самостоятельного решения
- •Атомно-абсорбционная спектроскопия
- •Вопросы и задачи для самостоятельного решения
- •Эмиссионный спектральный анализ
- •Вопросы и задачи для самостоятельного решения
- •Люминесцентный анализ
- •Вопросы и задачи для самостоятельного решения
- •Хроматографические методы анализа
- •Ионообменная хроматография.
- •100,0 ∙ 0,09567 Ммоль NaOh.
- •17,80 ∙ 0,09051 Ммоль щелочи,
- •Газовая хроматография.
- •Вопросы и задачи для самостоятельного решения
- •Метрологические характеристики методов анализа
- •Вопросы и задачи для самостоятельного решения
- •Справочные материалы
- •Коэффициенты активности ионов
- •Коэффициенты активности при высоких значениях ионной силы
- •Относительные атомные массы элементов
- •Растворимость неорганических и некоторых органических соединений в воде
- •Плотности водных растворов некоторых веществ при 20оС
- •Произведения растворимости важнейших малорастворимых веществ
- •Значения рН осаждения гидроксидов металлов
- •Гравиметрические факторы
- •Константы ионизации кислот
- •Константы ионизации оснований
- •Интервал рН перехода важнейших индикаторов
- •Некоторые смешанные индикаторы
- •Стандартные электродные потенциалы (е°) при 25°с
- •Окислительно-восстановительные индикаторы
- •Логарифмы суммарных констант устойчивости комплексных соединений
- •Логарифмы констант устойчивости комплексонатов металлов
- •Литература
Сильные электролиты
Сильные электролиты в растворах и расплавах полностью диссоциируют на ионы. Однако экспериментальные исследования электропроводности растворов сильных электролитов показывают, что ее величина несколько занижена по сравнению с той, которая должна была бы быть при 100 %-ной диссоциации. Такое несоответствие объясняется теорией сильных электролитов, предложенной Дебаем и Гюккелем.
В основе теории лежат следующие положения:
1.Электролит полностью диссоциирует, но в сравнительно разбавленных растворах (C = 0,01 моль/л).
2.Каждый ион окружен «ионной атмосферой», состоящей из ионов противоположного знака, препятствующей его свободному передвижению. Эта «ионная атмосфера» тормозит движение ионов в растворе при пропускании постоянного электрического тока, что создает эффект неполной диссоциации молекул, т.е. кажущейся степени диссоциации.
В таких системах понятие концентрации становится неоднозначиным и для более точных вычислений заменяется активностью. Активность и концентрация связаны между собой выражением:
![]() ,
,
где f – коэффициент активности, который характеризует взаимодействие ионов.
Мерой электростатического взаимодействия всех ионов, присутствующих в растворе, является ионная сила раствора μ:
![]() ,
,
Сi - молярные концентрации, zi - заряды всех ионов в растворе.
Связь коэффициента активности с ионной силой раствора выражается формулами:
![]() ,
при
,
при
![]() ;
;
![]() ,
при
,
при
![]()
![]() ,
если
,
если
![]()
Для нахождения коэффициентов активности можно использовать справочные данные табл.1 (Справочные материалы), рассчитанные на основе закона ионной силы Льюиса и Рендалла:
«В достаточно разбавленных растворах с одинаковой ионной силой коэффициенты активности большинства одинаково заряженных ионов приблизительно одинаковы.
Для выражения:
aA + bB ⇄ dD + eE
термодинамическая константа равновесия имеет вид:
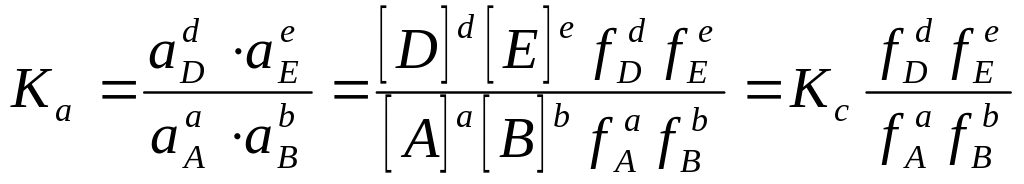
В таком виде закон действующих масс применим как к сильным электролитам, так и к смеси сильных и слабых электролитов.
Пример 3. Рассчитать активность ионов алюминия в растворе, содержащем смесь Al2(SO4)3 с концентрацией 0,005 моль/л и Na2SO4 с концентрацией
0,006 моль/л.
Решение: Ионная сила раствора складывается из всех ионов, образующихся при диссоциации сильных электролитов:
Al2(SO4)3 → 2Al3+ + 3SO42-
Na2SO4 → 2Na+ + SO42-
![]() при
,
используем формулу:
при
,
используем формулу:
![]() ,
,
![]()
![]()
С ростом ионной силы и заряда иона коэффициент активности и активность иона уменьшается.
Ионное произведение воды
Вода, являясь слабым электролитом, в незначительной степени подвергается диссоциации с образованием ионов водорода и гидроксила:
H2O ⇄ H+ + OH-.
По закону действия масс константу равновесия процесса диссоциации воды можно записать в виде:
![]()
Измерение электропроводности чистой воды показало, что концентрации [OH-]=[H+]=1.10-7 моль/л, а концентрация чистой воды равна [H2O]=1000/18=55,56 моль/л. Тогда:
![]()
Диссоциация воды очень незначительна, поэтому ее концентрацию можно считать практически неизменной и ввести в константу, тогда
![]() ,
,
т.е. произведение концентрации ионов водорода и гидроксила есть величина постоянная при данной температуре. Ее называют ионным произведением воды и обозначают Kw.
Диссоциация воды возрастает с повышением температуры.
Соотношение концентраций ионов водорода и гидроксила определяет кислотность среды:
если [H+] > [OH–] – среда кислая;
если [H+] < [OH–] – среда щелочная;
если [H+] = [OH–] – среда нейтральная.
Целесообразно кислотность раствора характеризовать не концентрацией, а водородным или гидроксильным показателем:
pН = – lg[H+] или pOH = – lg[OH–] .
В соответствии с этим, характер среды водных растворов можно определить следующими значениями рН:
pН < 7 – среда кислая;
pH = 7 – среда нейтральная;
pH > 7 – среда щелочная.
Выражение, связывающее рН и рOH раствора:
14 = рН+ + рОН–
Пример 4. Определите рН 0,01 М раствора гидроксида аммония, если
Кb = 1,7710–5.
Решение. Гидроксид аммония слабое основание и в водном растворе диссоциирует по схеме: NH4OH NH4+ + OH. Используя закон разбавления Оствальда, можно вычислить концентрацию ионов OH:
OH = С = (KbС)1/2 = (1,7710–5 0,01)1/2 = 4,210–4.
Тогда рОН = –lg[OH–] = –lg(4,210–4) = 3,38.
Следовательно, при 298 K, рН = 14 – рОН = 10,62.
Пример 5. Как изменится концентрация ионов водорода и рН, если к 1 л 0,1 М раствора цианистоводородной кислоты добавить 0,1 моль NaCN, кажущаяся степень диссоциации которого NaCN=85%? Константа диссоциации HCN равна 4,910–10.
Решение. Цианистоводородная кислота диссоциирует согласно уравнению: HCN H+ + CN. Учитывая, что Kа очень мала, вычисляем степень диссоциации кислоты в растворе без добавления соли по:
HCN = (Kа /С)1/2 = (4,910–10 / 0,1)1/2 = 710–5.
Отсюда [H+] = HCNС = 710–5 0,1 = 710–6 моль/л
рН = – lg[H+] = – lg(710–6) = 5,15.
При добавлении в раствор соли NaCN равновесие диссоциации кислоты, согласно принципу Ле-Шателье, сместится влево в результате появления в растворе большого количества ионов CN за счет диссоциации сильного электролита:
NaCN Na+ + CN
При этом уменьшится концентрация ионов водорода в растворе, то есть диссоциация слабой кислоты будет подавлена.
Обозначим новую концентрацию ионов водорода через х моль/л. Зная степень диссоциации соли (85%), можно определить концентрацию ионов CN, вносимых солью. Считаем, что объем раствора не изменился, поэтому концентрация соли составит 0,1 моль/л, а концентрация ее ионов CN
0,10,85 = 0,085 моль/л. Общая концентрация цианид-ионов составляет в образовавшемся растворе (х + 0,085) моль/л.
Подставим концентрации в выражение для Ка(HCN), помня, что из-за очень незначительной диссоциации цианистоводородной кислоты концентрация недиссоциированной кислоты практически совпадает с исходной концентрацией:
Ka = [H+][CN–]/[HCN]недисс = х(х + 0,085) / 0,1 = 4,910–10.
Решая квадратное уравнение, находим концентрацию ионов водорода в растворе с добавленной солью: х = 5,7610–10 моль/л.
Отсюда, новое значение рН = –lg(5,7610–10) = 9,24.
Таким образом, после добавления соли с одноименным анионом к раствору HCN концентрация ионов водорода понизилась в 12153 раз
(710–6 / (5,7610–10) 12153), а реакция среды изменилась с кислотной на щелочную.
Пример 6. Определите рН 0,15 М раствора азотистой кислоты HNO2, константа диссоциации которой составляет 5,110–4.
Решение. Кислота диссоциирует по уравнению:
HNO2 H+ + NO2
Для определения концентрации ионов водорода нужно использовать выражение для константы диссоциации:
Kа = [H+][NO2] / [HNO2]недисс.
Принимая [H+] = [NO2] = x, а [HNO2]недисс = (0,15 – х),
получим: Kа = х2 / (0,15 – х) = 5,110–4.
Решая квадратное уравнение, находим [H+] = x 8,510–3 моль/л.
По определению, рН = –lg[H+] = –lg(8,510–3) 2,07.
