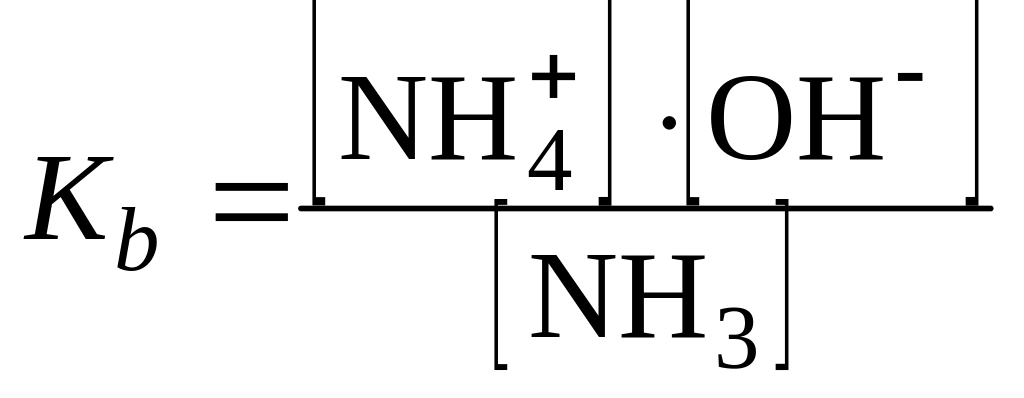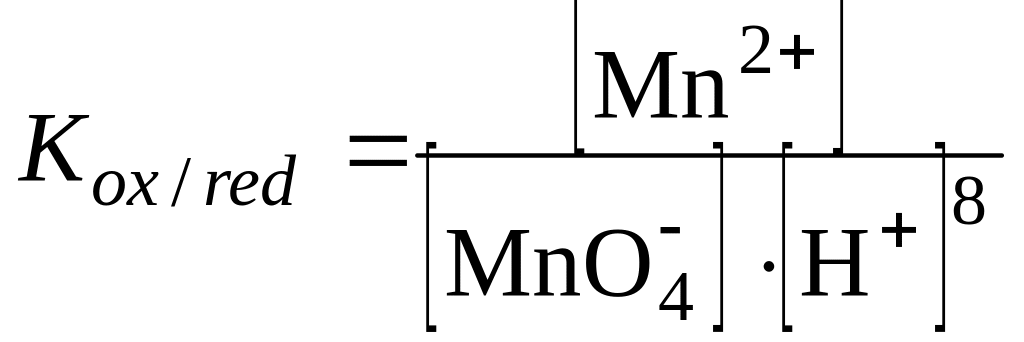- •Содержание
- •Введение
- •Диссоциация электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Ионное произведение воды
- •Расчет рН сильных кислот и оснований
- •Расчет рН слабых бинарных кислот и оснований
- •Влияние сильных электролитов и одноименных ионов на ионные равновесия в слабых электролитах
- •Буферные растворы
- •Гидролиз солей
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в гомогенных системах»
- •Равновесия в гетерогенных системах
- •Произведение растворимости
- •Задачи на применение условия выпадения осадка
- •Расчет растворимости осадков в присутствии одноименных ионов
- •Расчет растворимости осадка в присутствии разноименных ионов (солевой эффект)
- •Дробное осаждение
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное равновесие
- •Расчет констант равновесия окислительно-восстановительных реакций
- •Расчет окислительно-восстановительного потенциала
- •Вопросы и задачи для самостоятельного решения
- •Равновесия в растворах комплексных соединений
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в реакциях осаждения, комплексообразования и окисления-восстановления»
- •Качественный анализ
- •Вопросы и задачи для самостоятельной работы
- •Гравиметрический анализ
- •Расчет количества осадителя
- •Рассчитаем массу 4 %-ного раствора Na2hpo4:
- •Расчет потерь осадка при промывании
- •Выбор оптимального интервала значений рН
- •Расчёт результатов гравиметрического определения
- •0,0623 Г Ag содержится в 125 мл раствора;
- •Вопросы и задачи для самостоятельного решения
- •Титриметрические методы анализа
- •Способы выражения концентраций растворов
- •Определение фактора эквивалентности
- •Пример 2. Какой объем 0,1 н. Раствора серной кислоты необходимо отмерить для приготовления 100 мл 0,02 н. Раствора?
- •Способы титрования
- •Кислотно-основное титрование
- •Выбор индикатора
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Оксидиметрические индикаторы
- •Вопросы и задачи для самостоятельного решения
- •Комплексонометрическое титрование
- •Выбор индикатора и условий проведения анализа
- •Вопросы и задачи для самостоятельного решения
- •Примеры построения кривых титрования
- •Титрование сильных кислот и оснований
- •Титрование слабой кислоты сильным основанием
- •0,40 Моль/л раствором koh.
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Вопросы и задачи для самостоятельного решения
- •Физико-химические методы анализа
- •Потенциометрия и потенциометрическое титрование.
- •Вольтамперометрия
- •Кулонометрия.
- •Вопросы и задачи для самостоятельного решения
- •Спектроскопические методы анализа
- •Фотометрические методы анализа.
- •Вопросы и задачи для самостоятельного решения
- •Атомно-абсорбционная спектроскопия
- •Вопросы и задачи для самостоятельного решения
- •Эмиссионный спектральный анализ
- •Вопросы и задачи для самостоятельного решения
- •Люминесцентный анализ
- •Вопросы и задачи для самостоятельного решения
- •Хроматографические методы анализа
- •Ионообменная хроматография.
- •100,0 ∙ 0,09567 Ммоль NaOh.
- •17,80 ∙ 0,09051 Ммоль щелочи,
- •Газовая хроматография.
- •Вопросы и задачи для самостоятельного решения
- •Метрологические характеристики методов анализа
- •Вопросы и задачи для самостоятельного решения
- •Справочные материалы
- •Коэффициенты активности ионов
- •Коэффициенты активности при высоких значениях ионной силы
- •Относительные атомные массы элементов
- •Растворимость неорганических и некоторых органических соединений в воде
- •Плотности водных растворов некоторых веществ при 20оС
- •Произведения растворимости важнейших малорастворимых веществ
- •Значения рН осаждения гидроксидов металлов
- •Гравиметрические факторы
- •Константы ионизации кислот
- •Константы ионизации оснований
- •Интервал рН перехода важнейших индикаторов
- •Некоторые смешанные индикаторы
- •Стандартные электродные потенциалы (е°) при 25°с
- •Окислительно-восстановительные индикаторы
- •Логарифмы суммарных констант устойчивости комплексных соединений
- •Логарифмы констант устойчивости комплексонатов металлов
- •Литература
Введение
Аналитическая химия – наука разрабатывающая теоретические основы и методы химического анализа. Ее практической задачей является установление химического состава веществ и их смесей.
Обнаружение отдельных элементов или ионов, входящих в состав вещества является задачей качественного анализа.
Определение количественного содержания отдельных составных частей исследуемого вещества является задачей количественного анализа.
Перед аналитической химией полупроводниковых материалов поставлены следующие задачи:
- анализ химического состава полупроводниковых и диэлектрических элементов на различных подложках;
- анализ профиля распределения легирующих добавок в полупроводнико
вых материалах;
- исследование совместимости материалов и технологических процессов при изготовлении многослойных микросхем;
- исследование процессов растворения проводниковых, полупроводниковых и диэлектрических элементов микросхем при создании физико -химических основ фотолитографии или определении влагоустойчивости микросхем;
- контроль исходного сырья и реактивов, применяемых в технологии изго
товления полупроводников и диэлектриков и т.д.
В настоящее время в промышленной электронике и радиотехнике, кроме широко используемых кремния и германия, находят применение полупроводниковые соединения сложного химического состава: антимонид индия, арсенид галлия, фосфиды индия и галлия, халькогениды цинка, кадмия, ртути, свинца, висмута, сурьмы, а также оксидные ванадийсодержащие полупроводниковые стекла и др.
Особое значение уделяется чистоте материалов, которая определяет вос-
производимость и физические параметры схем и приборов в микроэлектронике.
Получение и очистка веществ до особочистого состояния неразрывно связаны с методами анализа на микропримеси. Качественное и количественное определение микропримесей составляет главную задачу аналитической химии полупроводников и диэлектриков. При анализе материалов на микропримеси необходима особая чистота химических реагентов и воды, коррозионно-стойкая аппаратура, предварительная подготовка проб.
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ ОСНОВЫ
КАЧЕСТВЕННОГО И КОЛИЧЕСТВЕННОГО АНАЛИЗА
ПРИМЕРЫ РЕШЕНИЯ ТИПОВЫХ ЗАДАЧ
Ионные равновесия в гомогенных системах
Закон действия масс
В аналитической химии закон действующих масс является теоретической основой многих методов анализа, так как устанавливает количественные соотношения между веществами, участвующими в обратимых химических реакциях в момент достижения равновесия.
Для обратимой химической реакции:
aA + bB ⇄ dD + eE
скорость прямой реакции равна:
![]() ,
,
т.к. при постоянной температуре скорость реакции прямо пропорциональна произведению концентраций реагирующих веществ в степенях их стехиометрических коэффициентов. Тогда скорость обратной реакции:
![]() .
.
В некоторый момент времени наступает состояние равновесия:
![]() ,
,
следовательно,
![]()
Преобразовав данное выражение, получим:
![]() .
.
Полученное выражение представляет собой закон действующих масс: для обратимой химической реакции в состоянии равновесия произведение равновесных концентраций (активностей) в степенях их стехиометрических коэффициентов, отнесенное к такому же произведению для исходных веществ, есть величина постоянная при данной температуре. Константа химического равновесия не зависит от концентрации реагирующих веществ.
Основные типы химических равновесий, для описания которых применим закон действующих масс, и выражения для константы равновесия приведены в таблице 1:
Таблица 1
Основные типы химических равновесий |
Выражение для константы равновесия |
кислотно - основные равновесия
NH3 + H2O NH4+ + OH-,
HCOOH HCOO– + H+ |
константа диссоциации
|
гетерогенные равновесия BaSO4 Ba2++SO42- |
произведение
растворимости
|
равновесия комплексообразования
Fe3+ + CN- FeCN2+ |
константа устойчивости комплексного иона
|
окислительно- восстановительные равновесия MnO4+8H++5e Mn2++4H2O |
Окислительно – восстановительная константа
|
Пример1. Во сколько раз изменится скорость прямой и обратной реакции в системе: 2SO2(г) + O2(г) 2SO3(г), если объем газовой смеси уменьшить в три раза? В какую сторону сместится равновесие системы?
Решение: Обозначим концентрации реагирующих веществ:
[SO2] = А, [O2] = В, [SO3] = С.
Согласно закону действия масс скорости и прямой и обратной реакций до изменения объема:
![]() ;
;
![]()
После уменьшения объема гомогенной системы в три раза концентрация каждого из реагирующих веществ увеличится в три раза: [SO2] = 3А,
[O2] = 3В, [SO3] = 3С. При новых концентрациях скорости прямой и обратной реакций:
![]() ;
;
![]()
Отсюда :
![]() ;
;
![]()
Следовательно, скорость прямой реакции увеличилась в 27 раз, а обратной – только в девять раз. Равновесие системы сместилось в сторону образования SO3.