
- •Содержание
- •Введение
- •Диссоциация электролитов
- •Слабые электролиты
- •Сильные электролиты
- •Ионное произведение воды
- •Расчет рН сильных кислот и оснований
- •Расчет рН слабых бинарных кислот и оснований
- •Влияние сильных электролитов и одноименных ионов на ионные равновесия в слабых электролитах
- •Буферные растворы
- •Гидролиз солей
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в гомогенных системах»
- •Равновесия в гетерогенных системах
- •Произведение растворимости
- •Задачи на применение условия выпадения осадка
- •Расчет растворимости осадков в присутствии одноименных ионов
- •Расчет растворимости осадка в присутствии разноименных ионов (солевой эффект)
- •Дробное осаждение
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное равновесие
- •Расчет констант равновесия окислительно-восстановительных реакций
- •Расчет окислительно-восстановительного потенциала
- •Вопросы и задачи для самостоятельного решения
- •Равновесия в растворах комплексных соединений
- •Вопросы и задачи для самостоятельного решения
- •Тест для самоконтроля «Ионные равновесия в реакциях осаждения, комплексообразования и окисления-восстановления»
- •Качественный анализ
- •Вопросы и задачи для самостоятельной работы
- •Гравиметрический анализ
- •Расчет количества осадителя
- •Рассчитаем массу 4 %-ного раствора Na2hpo4:
- •Расчет потерь осадка при промывании
- •Выбор оптимального интервала значений рН
- •Расчёт результатов гравиметрического определения
- •0,0623 Г Ag содержится в 125 мл раствора;
- •Вопросы и задачи для самостоятельного решения
- •Титриметрические методы анализа
- •Способы выражения концентраций растворов
- •Определение фактора эквивалентности
- •Пример 2. Какой объем 0,1 н. Раствора серной кислоты необходимо отмерить для приготовления 100 мл 0,02 н. Раствора?
- •Способы титрования
- •Кислотно-основное титрование
- •Выбор индикатора
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Оксидиметрические индикаторы
- •Вопросы и задачи для самостоятельного решения
- •Комплексонометрическое титрование
- •Выбор индикатора и условий проведения анализа
- •Вопросы и задачи для самостоятельного решения
- •Примеры построения кривых титрования
- •Титрование сильных кислот и оснований
- •Титрование слабой кислоты сильным основанием
- •0,40 Моль/л раствором koh.
- •Вопросы и задачи для самостоятельного решения
- •Окислительно-восстановительное титрование
- •Вопросы и задачи для самостоятельного решения
- •Физико-химические методы анализа
- •Потенциометрия и потенциометрическое титрование.
- •Вольтамперометрия
- •Кулонометрия.
- •Вопросы и задачи для самостоятельного решения
- •Спектроскопические методы анализа
- •Фотометрические методы анализа.
- •Вопросы и задачи для самостоятельного решения
- •Атомно-абсорбционная спектроскопия
- •Вопросы и задачи для самостоятельного решения
- •Эмиссионный спектральный анализ
- •Вопросы и задачи для самостоятельного решения
- •Люминесцентный анализ
- •Вопросы и задачи для самостоятельного решения
- •Хроматографические методы анализа
- •Ионообменная хроматография.
- •100,0 ∙ 0,09567 Ммоль NaOh.
- •17,80 ∙ 0,09051 Ммоль щелочи,
- •Газовая хроматография.
- •Вопросы и задачи для самостоятельного решения
- •Метрологические характеристики методов анализа
- •Вопросы и задачи для самостоятельного решения
- •Справочные материалы
- •Коэффициенты активности ионов
- •Коэффициенты активности при высоких значениях ионной силы
- •Относительные атомные массы элементов
- •Растворимость неорганических и некоторых органических соединений в воде
- •Плотности водных растворов некоторых веществ при 20оС
- •Произведения растворимости важнейших малорастворимых веществ
- •Значения рН осаждения гидроксидов металлов
- •Гравиметрические факторы
- •Константы ионизации кислот
- •Константы ионизации оснований
- •Интервал рН перехода важнейших индикаторов
- •Некоторые смешанные индикаторы
- •Стандартные электродные потенциалы (е°) при 25°с
- •Окислительно-восстановительные индикаторы
- •Логарифмы суммарных констант устойчивости комплексных соединений
- •Логарифмы констант устойчивости комплексонатов металлов
- •Литература
Вопросы и задачи для самостоятельного решения
Какие реакции называют окислительно-восстановительными?
Что характеризует стандартный окислительно-восстановительный потенциал?
Как можно оценить направление окислительно-восстановительной реакции?
Какие факторы влияют на величину формального окислительно-восстановительного потенциала?
5. На кислый раствор, содержащий ионы MnO4–, Cr2O72–, IO3–, NO3–, действуют H2S. Какой из указанных ионов вступит в реакцию: а) первым, б) последним?
Ответ: а) MnO4– , б) NO3–
6. На кислый раствор, содержащий Sn2+, HNO2, Fe2+, I–, действуют
КМnО4. Какой восстановитель будет окисляться, а) первым: б) последним?
Ответы: а) HNO2, б) Sn2+
7. Закончите уравнения реакций
а) KМnО4 + KNO2 + H2SO4 →
б) KI + KNO2 + H2SO4 →
Объясните, почему нитрит калия в одном случае ведет себя как восстановитель, а в другом - как окислитель.
8. Чему равны окислительные потенциалы (в вольтах):
а) пары Sn4+/Sn2+ при [Sn4+] = 0,001 моль/л и [Sn2+] = 0,1 моль/л;
б) пары MnO4–/Mn2+ при равных концентрациях окисленной и восста-
новленной форм и рН = 5?
Ответы: а) 0,092 В, б) 1,046 В
9. Чему равен окислительный потенциал (в вольтах) пары Cr2O72–/Cr3+
при единичной концентрации окисленной и восстановленной форм и рН = 1?
Ответ: 1,22 В
10. Выведите формулы для вычисления констант равновесия реакций:
а) Sn2+ + I2 = Sn4+ + 2I–,
б) МnО4– + 5Fe2+ + 8H+ = Mn2+ + 5Fe2+ + 4Н2О
и найдите их численные значения. В какой из этих реакций степень превращения исходных веществ будет больше?
Ответы: а) K = 2,8 1013; б) K = 6,3 1063.
11. Чему равна эквивалентная масса KMnO4 в реакциях с Na2SO3 в различных средах: а) кислой, б) нейтральной; в) щелочной?
Ответы: а) 31,6; 6)52,7; в) 158 г/моль.
12 Как изменится электродный потенциал серебряного электрода, помещенного в 0,1 М раствор AgNO3, при введении в раствор 0,5 М KI
(Ео(Ag+/Ag) = 0,8В, ПР(AgI)|=1∙10–16)?
Ответы: Ео(Ag+/Ag) = 0,74 В, Ео(AgI/Ag) = –0,12 В.
13. Будет ли реагировать металлическое серебро с 0,1 М раствором H2S
(Ео(Ag+/Ag) = 0,8В, ПР(Ag2S = 6,3∙10–50)? Ответ подтвердить расчетом.
Ответ: будет.
Рассчитайте величину окислительно-восстановительного потенциала
пары MnO4-/Mn2+, если в растворе активности ионов равны a(Mn2+) = 0,01 моль/л, a(MnO4-) = 0,1 моль/л, рН = 7.
. Ответ: E = 0,86 В.
Расставьте стехиометрические коэффициенты и рассчитайте константу
равновесия реакции
Fe2+ + O2 + H+ ↔ Fe3+ + H2O
Ответ: К = 1.1031.
Определите направление протекания реакции при рН = 0 и при рН = 8
I2 + HAsO2 + 2H2O H3AsO4 + 2H+ + 2I-
Вычислите растворимость металлического кобальта в 1 М растворе
хлороводородной кислоты.
Ответ: S(Co) = 0,5 моль/л.
Вычислите растворимость металлического золота в 1,2 М азотной ки-
слоте.
Ответ: S(Au) = 4.10-12 моль/л.
Равновесия в растворах комплексных соединений
Комплексные соединения – это частицы, образованные двумя или большим числом более простых частиц (ионов, молекул), способных к самостоятельному существованию в растворе. Молекулы комплексных соединений состоят, как правило, из внешней сферы и внутренней сферы. Диссоциация по внешней сфере протекает практически полностью, например
Ag(NH3)2Cl Ag(NH3)2+ + Cl-.
Внутренняя сфера комплексного иона или молекулы состоит из одного или нескольких центральных атомов или ионов, называемых комплексообразователями, вокруг которых координируются ионы или молекулы, называемые лигандами. Координационное число показывает, сколько лигандов непосредственно связано с комплексообразователем. Диссоциация комплексных соединений по внешней сфере идет ступенчато, каждая стадия характеризуется своей ступенчатой константой, процесс диссоциации внутренней сферы комплексной частицы обратим. Константа диссоциации комплексных частиц называется константой нестойкости Кн , а обратная ей величина – константой устойчивости комплексного иона.
В аналитической химии наиболее часто встречаются следующие комплексные соединения:
- ацидокомплексы – соединения, в которых роль лигандов выполняют кислотные остатки, например: K4[Fe(CN)6], Na3[Co(NO2)6], Na3[FeF6];
- гидроксокомплексы – соединения, в которых роль лигандов принадлежит ионам гидроксила, например; Na3[Al(OH)6], Na2[Zn(OH)4];
- аммиакаты – комплексные соединения, в состав которых входят молекулы аммиака, например: [Ag(NH3)2]Cl, [Cu(NH3)4](OH)2;
- аквакомплексы – соединения, содержащие во внутренней сфере молекулы воды, например: [Al(H2O)6]Cl3, [Co(H2O)6]Cl3;
- внутрикомплексные соединения.
 O…..H–O
O…..H–O
H3C–C=N N=C–CH3
Ni
H3C–C=N N = C–CH3
O–H…...O
Реакции комплексообразования широко применяются в качественном и в количественном анализе. Основные направления использования комплексов в качественном анализе.
1. Огромное число характерных реакций на те или иные ионы основано на комплексообразовании. Например, по образованию характерно окрашенного комплекса ионов никеля и диметилглиоксимом (реакция Чугаева) можно сделать вывод о наличии ионов никеля в растворе.
2. Комплексообразование имеет значение не только при обнаружении отдельных ионов, но и для их разделения. Например, для разделения ионов Al3+ и Zn2+ используется раствор аммиака. Ионы алюминия переходят в осадок Al(OH)3, а ионы цинка образуют аммиачный комплекс [Zn(NH3)6]2+.
3. Комплексообразование используют для маскировки отдельных ионов. Например, присутствие в растворе ионов Fe3+ мешает обнаружению ионов Co2+. Чтобы значительно снизить концентрацию ионов Fe3+ и обнаружить ионы кобальта, можно внести в раствор фторид аммония. Образуется прочный комплекс [FeF6]3–, и концентрация ионов Fe3+ снижается настолько, что оказывается возможным обнаружить ион Co2+.
4. Комплексообразование используется для перевода в раствор некоторых малорастворимых веществ. Например, хлорид серебра растворяется при добавлении раствора аммиака, так как образуется комплексное соединение:
AgCl + 2NH3•H2O = [Ag(NH3)2]Cl + 2H2O.
Равновесия в растворах комплексных соединений характеризуется константой устойчивости комплекса:
![]() .
.
Отношение общей концентрации соли металла к равновесной концентрации его ионов – есть функция закомплексованности Ф:
![]() ;
;
![]() .
.
Доля образующегося комплекса вычисляется следующим образом:
![]() или
или
![]() .
.
Если лиганд является анионом слабой кислоты или основания, то функция закомплексованности зависит от рН растворителя, а равновесная концентрация лиганда: [L–m] = C(HmL) ∙ αm,
где C(HmL) – общая концентрация кислоты,
αm – доля аниона кислоты.
![]() ,
,
где K1, K2 Km – константы диссоциации кислоты.
В этом случае уместно пользоваться значением условной константы устойчивости βn:
![]() ;
;
![]() .
.
Пример 1. Рассчитайте равновесную концентрацию ионов серебра в
0,01 М растворе AgNO3 в присутствии 2 М раствора аммиака.
Решение. В растворе устанавливается равновесие
![]() ;
;
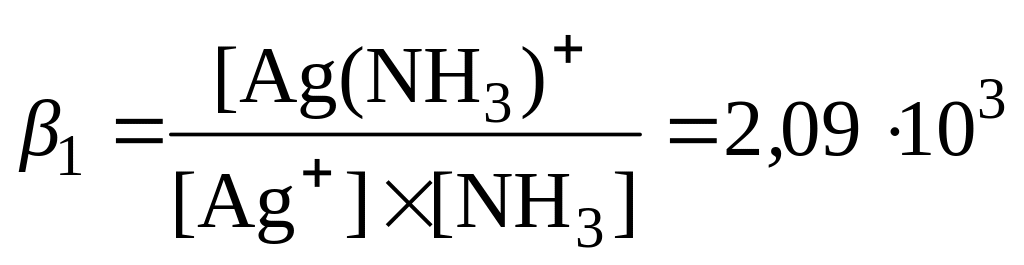 ;
;
![]() ;
;
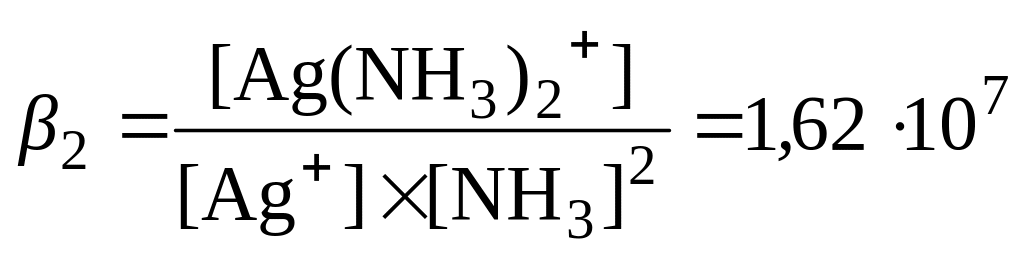 ;
;
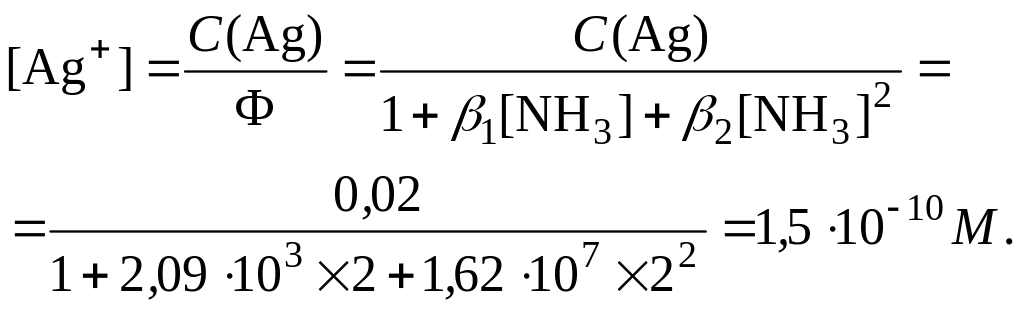
Пример 2. Рассчитайте равновесную концентрацию ионов Zn2+ в 1 М растворе [Zn(NH3)4]Cl2, (lg =8,7).
Решение:
[Zn(NH3)4]Cl2 → [Zn(NH3)4]2+ + 2Cl–
[Zn(NH3)4]2+ ↔ Zn2+ + 4NH3
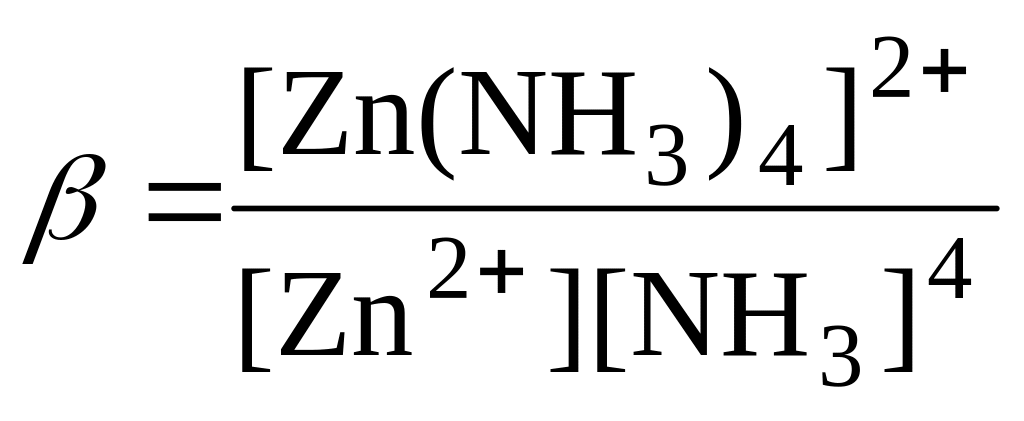
![]()
Обозначим [Zn2+] = x моль/л, тогда [NH3] = 4x моль/л.
Величина х<<1, ею можно пренебречь,
Равновесная концентрация [Zn(NH3)4]2+ = 1 моль/л.
Подставим равновесные концентрации ионов в выражение константы устойчивости:
![]()
![]()
Пример 3 Выпадет ли осадок оксалата цинка при добавлении к 0,001 М раствору [Zn(NH3)4]2+ 0,1 моль/л оксалата натрия, если равновесная концентрация аммиака в растворе составляет 0,1 моль/л, ПР(ZnC2O4) = 2,75∙10–8,
([Zn(NH3)4]2+) = 2,0∙109
Решение: Осадок будет образовываться, если выполняется условие:
[Zn2+]∙[C2O42–] > ПР
[C2O42–] = [Na2C2O4] = 0,1 моль/л
Равновесную концентрацию ионов цинка рассчитаем из константы устойчивости аммиакатного комплекса цинка:
[Zn(NH3)4]2+ ↔ Zn2+ + 4NH3
В растворе присутствует избыток аммиака, следовательно, равновесие сдвинуто в сторону образования комплекса, диссоциация комплекса подавлена. [NH3]=0,1 моль/л.
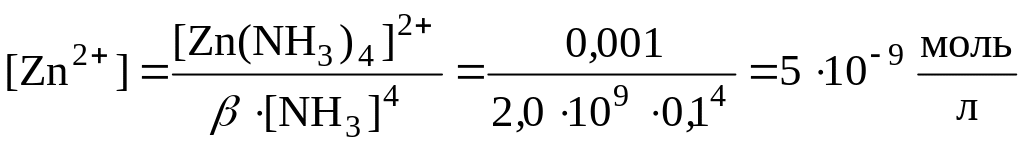 ;
;
[Zn2+]∙[C2O42–] = 0,1∙5∙10–9 < ПР, следовательно осадок в данных условиях не образуется.
Пример 4. Найти растворимость (S) фторида магния в растворе HCl с молярной концентрацией эквивалента 0,01, если KHF = 6 ∙ 10–4 ,
а ПР (MgF2) = 6,4 ∙ 10–9.
Решение. Находим значение α:
![]()
тогда
![]()
![]() моль/л.
моль/л.
