
- •Тема 1. Введение. Предмет и задачи микробиологии. Классификация микроорганизмов
- •Основы бактериологии
- •Тема 2. Основы морфологии бактерий.
- •Размер бактерий
- •Основы бактериологии
- •Тема 3. Физиология и биохимия бактерий. Строение и классификация грибов.
- •Тема 4. Знакомство с микробиологической лабораторией. Микроскопические методы исследования морфологии бактерий и грибов.
- •Ема 5. Бактериологические методы исследования.
- •Тема 9. Паразитологические методы исследования. Лабораторная диагностика инвазий.
- •Тема 10
- •Тема 11. Вирусологические методы исследования.
- •Тема 12. Генетика микроорганизмов и генная инженерия в медицинской микробиологии
- •Влияние факторов окружающей среды на микроорганизмы
- •Тема 13. Основы экологической микробиологии. Микрофлора тела здорового человека.
- •Значение микрофлоры тела для человека
- •Влияние факторов окружающей среды на микроорганизмы
- •Тема 14. Действие физических, химических и биологических факторов внешней среды на микроорганизмы.
- •Влияние факторов окружающей среды на микроорганизмы
- •Тема 15. Микробиологические основы химиотерапии и химиопрофилактики инфекционных болезней.
- •Асептика
- •Тема 16. Методы стерилизации и дезинфекции. Определение чувствительности микроорганизмов к антибиотикам.
- •Методы стерилизации и дезинфекции в микробиологической лаборатории.
- •Лабораторная диагностика дисбактериоза
- •Тема 17. Учение об инфекции. Патогенность микроорганизмов.
- •Факторы вирулентности вирусов
- •Тема 17. Учение об инфекции. Патогенность микроорганизмов.
- •Основы эпидемиологии
- •Тема 18. Основы эпидемиологии. Основы клинической микробиологии.
- •Тема 19. Микробиологические основы борьбы с внутрибольничными инфекциями.
- •Основы иммунологии
- •Тема 20. Понятие об иммунологии. Неспецифические факторы защиты организма человека.
- •Структура иммунной системы
- •Тема 20. Понятие об иммунологии. Неспецифические факторы защиты организма человека.
- •Структура иммунной системы
- •Тема 21. Антигены.
- •Тема 22. Иммунная система организма человека. Антитела.
- •Тема 23. Формы иммунитета. Виды иммунитета.
- •Регуляция иммунного ответа
- •Основы клинической иммунологии
- •Тема 24. Клиническая иммунология: аллергия, иммунодефицитные состояния.
- •Реакции гиперчувствительности (аллергические)
- •Аутоиммунная патология
- •Иммунодефицитные состояния
- •Оценка иммунного статуса человека
- •Основы иммунодиагностики
- •Тема 25. Применение реакции антиген-антитело в медицинской практике (иммунодиагностика).
- •Иммуномикробиологические исследования
- •Тема 26. Иммуномикробиологические исследования. Реакции агглютинации и преципитации.
- •Иммуномикробиологические исследования Серологические реакции в микробиологических и иммунологических лабораториях используют в двух целях:
- •Иммунологические реакции выявления специфических антигенов
- •Условные обозначения: - торможение гемагглютинации (пуговка) ; - гемагглютинация (зонтик).
- •Определение групп крови аво
- •9. Реакция гемагглютинации (рга)
- •Тема 27. Реакции связывания комплемента. Риф и ифа.
- •Реакция связывания комплемента
- •Метод флюоресцирующих антител (мфа) или реакции иммунофлюоресценции (риф)
- •Иммуноферментный анализ (ифа)
- •Основы иммунопрофилактики
- •Тема 28. Основы иммунотерапии и иммунопрофилактики.
- •Иммунотропные лекарственные средства
- •Специфическая иммунопрофилактика и иммунотерапия вакцины
- •Иммунные сыворотки и иммуноглобулины
- •Основы иммунопрофилактики
- •Тема 29. Изучение препаратов, применяемых для иммунопрофилактики и иммунотерапии.
- •Вакцинопрофилактика
- •Серопрофилактика и серотерапия
- •Определение пригодности иммунобиологических препаратов
- •Тема 30. Основы иммунологии.
Тема 22. Иммунная система организма человека. Антитела.
Содержание:
Факторы специфической защиты
Иммунная система человека
Антитела
ФАКТОРЫ СПЕЦИФИЧЕСКОЙ ЗАЩИТЫ
Наряду с факторами неспецифической защиты среда организма защищена от проникающих в нее чужеродных макромолекул, в том числе от патогенных микробов, механизмами специфического иммунного ответа. Эти механизмы приобретаются организмом после контакта с конкретным чужеродным веществом, носящим название антиген. Действие этих механизмов строго избирательно и распространяется только на конкретный антиген, который индуцировал иммунный ответ. Реализация иммунного ответа является функцией высоко специализированной иммунной системы организма. Основные защитные функции иммунной системы - распознавание и элиминацию чужеродных макромолекул - осуществляют иммунокомпетентные клетки (лимфоциты), а также продуцируемые и секретируемые ими макромолекулы - антитела (иммуноглобулины). Специфический иммунный ответ является одним из компонентов общей системы защиты организма, в которой все вышеперечисленные клетки и макромолекулы взаимосвязаны. Местом функциональной кооперации всех перечисленных клеток и макромолекул служат органы и ткани иммунной системы организма.
Лимфоциты
Лимфоциты - это единственные клетки организма, способные специфически распознавать и различать разные антигены и отвечать активацией на контакт с определенным антигеном. Лимфоциты находятся в состоянии рециркуляции, т.е. постоянно происходит обмен клетками между кровью, лимфой и лимфоидными органами. Это необходимо для реализации специфического иммунного ответа, так как иммунная система должна быть готова ответить на любой из множества чужеродных антигенов, попадающих в любой участок тела. Поскольку каждый отдельный антиген распознается лишь очень небольшой частью популяции лимфоцитов, только постоянная рециркуляция может создать условия для встречи каждого антигена с единичными лимфоцитами, несущими специфические для него антиген-распознающие рецепторы. Встретив и распознав этот антиген, лимфоциты размножаются (пролиферация) и дифференцируются, благодаря клональной селекции. Большая часть из них принимает непосредственное участие по уничтожению антигена, а меньшая часть остается в виде долгоживущих активированных клеток памяти и в данный момент участие в защите не принимает. При весьма сходной морфологии малые лимфоциты делятся на две популяции, имеющие различные функции и продуцирующие разные белки. В зависимости от места созревания в организме подразделяются на Т-(тимус) и В- (бурса Фабрициуса, костный мозг) лимфоциты.
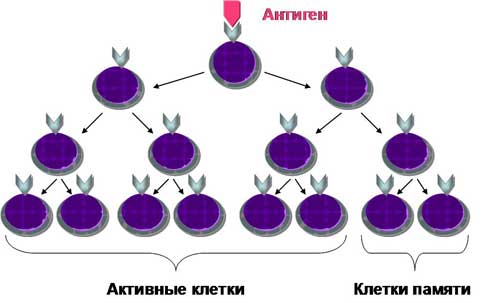
Рис. 1. Клональная селекция лимфоцитов (схема). После антигенной стимуляции лимфоциты размножаются и дифференцируются. Большая часть из них активно участвуют в уничтожении антигена, а меньшая остается в виде долгоживущих клеток памяти.
В-лимфоциты Каждая В-клетка генетически запрограммирована на синтез поверхностного рецептора иммуноглобулиновой природы (иммуноглобулиновые антигенраспознающие рецепторы), специфичного к одному определенному антигену. Встретив и распознав этот антиген, В-клетки размножаются и дифференцируются в плазматические клетки, которые образуют и выделяют в растворимой форме большие количества таких рецепторных молекул, называемых антителами. Антитела представляют собой крупные гликопротеины и содержатся в крови и тканевой жидкости. Благодаря своей идентичности исходным рецепторным молекулам они взаимодействуют с тем антигеном, который первоначально активировал В-клетки.
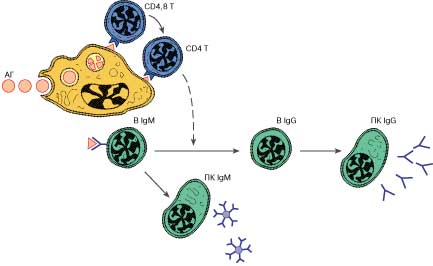
Рис. 2. В-лимфоциты после антигенной стимуляции размножаются и дифференцируются в плазматические клетки (ПК), которые образуют и выделяют антитела.
Т-лимфоциты Другая популяция получила название Т-лимфоциты в связи с их дифференцировкой в тимусе. Имеются несколько субпопуляций Т-клеток с различными функциями. Одни взаимодействуют с мононуклеарными фагоцитами, способствуя разрушению локализованных в них микроорганизмов. Другие взаимодействуют с В-клетками, помогая им размножаться, созревать и образовывать антитела. Обе эти субпопуляции Т-клеток названы хелперными Т-клетками (Тх) и для них характерен поверхностный маркер CD4+. Первые из них обозначаются как Тх1 (Th1)-клетки, они участвуют в реализации реакции гиперчувствительности замедленного типа (ГЗТ) и способны синтезировать ИЛ-2, ИФНg и лимфотоксин, а вторые обозначаются - Тх2 (Th2)-клетки и продуцируют ИЛ-4, ИЛ-5, ИЛ-6 и ИЛ-10. Таким образом Т-хелперы являются индукторами (активаторами) иммунных реакций. Третья субпопуляция Т-клеток осуществляет разрушение клеток организма, зараженных вирусами или иными внутриклеточно размножающимися патогенными микробами. Этот тип активности Т-клеток назван цитотоксичностью, а сами клетки соответственно цитотоксическими Т-лимфоцитами (ТЦТЛ или ТCTL или Тц) или Т-киллерами (Тк), они имеют маркер CD8+. Свои функции воздействия на другие клетки Т-лимфоциты осуществляют путем выделения растворимых белков - цитокинов, которые передают сигналы другим клеткам, или путем прямых межклеточных контактов. В цитотоксической реакции атакующая клетка направляет содержимое своих гранул наружу, к клетке-мишени. Гранулы цитотоксических Т-клеток содержат соединения, называемые перфоринами, которые способны создавать каналы в наружной мембране клеток-мишеней. (Подобно этому, антитела, связавшись с поверхностью клетки-мишени, могут привлечь комплемент для перфорирования ее цитоплазматической мембраны). Кроме того гранулы содержат лимфотоксины, которыми цитотоксические лимфоциты, путем введения через проделанное отверстие в мембране, лизируют клетку-мишень. Некоторые цитотоксические клетки способны также своим сигналом включать программу саморазрушения клетки-мишени - процесс апоптоза. Как правило, распознавание антигена Т-клетками происходит только при том условии, что он презентирован на поверхности других клеток в ассоциации (комплексе) с молекулами МНС. В распознавании участвует специфичный к антигену Т-клеточный рецептор(ТкР или TCR), функционально и структурно сходный с той поверхностью молекулы иммуноглобулина, которая у В-клеток служит антигенсвязывающим рецептором. При этом Т-хелперы распознают антиген в ассоциации с МНС II класса, Т- киллеры - с МНС I класса.
Рис. 3. Т-хелперы распознают антиген Т-клеточным рецептором (ТКР) в ассоциации с МНС II класса, Т- киллеры - с МНС I класса.
После антигенной стимуляции Т-лимфоциты в результате пролиферативного размножения и дифференцировки могут в виде небольшой группы долгоживущих клеток памяти (как Тх, так и Тц) оставаться в организме в качестве резерва и при повторной встрече с данным антигеном быстро и эффективно уничтожать его.
ИММУННАЯ СИСТЕМА ЧЕЛОВЕКА
Иммунная система включает специализированную, анатомически обособленную лимфоидную ткань, «разбросанную» по всему организму в виде различных лимфоидных образований и отдельных клеток. Различают первичные - центральные (костный мозг и тимус) и вторичные - периферические (селезенка, лимфатические узлы, скопления лимфоидной ткани) органы иммунной системы. Все они взаимосвязаны системой кровообращения, лимфотока и единой системой иммунорегуляции. Первичные - центральные органы иммунной системы Центральные органы иммунной системы - костный мозг и тимус выполняют важнейшие функции, обеспечивая самообновление иммунной системы, в этих органах идут процессы пролиферации клеток предшественников, их дифференцировка и созревание, вплоть до выхода в циркуляцию и заселения периферических органов иммунной системы зрелыми иммунокомпетентными клетками.
Рис. 4. Клетки крови формируются в костном мозге (фотография).

Рис. 5. В тимусе происходит созревание Т-хелперов и Т-киллеров, которые изначально поступают из костного мозга незрелыми, в процессе созревания они приобретают ТКР для распознавания антигена и CD4+ или CD8+ рецепторы для согласованной работы с другими иммуноцитами (схема).
Вторичные - периферические органы иммунной системы Периферические органы иммунной системы - лимфатические узлы, селезенка и лимфоидная ткань, ассоциированная со слизистыми - являются местом встречи антигенов с иммунокомпетентными клетками, местом распознавания антигена и развития специфического ответа, местом взаимодействия иммунокомпетентных клеток, их пролиферации (клональной экспансии), антиген-зависимой дифференцировки и местом накопления продуктов иммунного ответа.
АНТИТЕЛА
Антитела (иммуноглобулины) (АТ, Ig) - в большинстве случаев представлены сывороточными гликопротеинами, входящие в состав фракции гамма-глобулинов. АТ образуют один из основных классов белков крови, составляя 20% массы белка плазмы. Молекула АТ состоит из 2 идентичных тяжелых (Н-цепи) и 2 идентичных легких (L-цепи) аминокислотных цепей, соединенных дисульфидными -S-S- связями (рис.3). В цепях различают вариабельную область (V-область) в N-концевой части и постоянную, или константную, область (С-область). V-область у разных АТ варьирует. V-области L- и Н-цепей образуют Аг-связывающий центр (активный центр АТ, паратоп), или Fab-фрагмент. Константная область молекулы имеет Fc-фрагмент. Аг-связывающий центр, образованный вариабельными областями L- и Н-цепей; именно с ним взаимодействует Аг-детерминанта (эпитоп) антигена. Аг-связывающий центр комплементарен эпитопу Аг по приципу «ключ-замок». Молекула Ig как минимум двухвалентна; такие антитела известны как полные АТ, а мономеры с меньшей валентностью - как неполные АТ. Fc-фрагмент определяет специфичность связывания молекулы Ig с клетками-эффекторами (например, макрофагами, полиморфноядерными лейкоцитами, тучными клетками), несущими на своей поверхности рецепторы Fc-фрагмента.

Рис. 6. Структура иммуноглобулина.
Классы иммуноглобулинов и свойства антител В зависимости от структуры Н-цепей выделяют 5 разных классов (изотипов) АТ: IgA, IgD, IgE, IgG и IgM. 1. IgM - пентамер из 5 субъединиц, соединенных дисульфидными связями, имеет 10 Аг-связывающих участков. IgM - наиболее ранний класс АТ, обнаруживаемый при первичном попадании Аг в организм, т.е. наличие IgM к Аг конкретного возбудителя указывает на наличие острого инфекционного процесса. Молекулы IgM опсонизируют, агглютинируют, преципитируют и лизируют содержащие Аг структуры, а также легко активируют систему комплемента. 2. IgG - Основной класс АТ (до 75% всех Ig), защищающих организм от бактерий, вирусов и токсинов. После первичного контакта с Аг синтез IgM обычно сменяется образованием более дифференцированных IgG. Максимальные титры IgG при первичном ответе наблюдаются на 6-8 сутки. Обнаружение высоких титров IgG к Аг конкретного возбудителя указывает на то, что организм находится на стадии реконвалесценции или конкретное заболевание перенесено недавно. IgG непосредственно участвуют в реакциях иммунного цитолиза, реакциях нейтрализации, а также усиливают фагоцитоз. Только IgG беременной форсируют плацентарный барьер, проходят через базальную мембрану трофобласта в соединительную ткань плода и попадает в капилляры плода. Транспорт IgG через плаценту обеспечивает формирование пассивного иммунитета у плода. 3. IgA (в сывороточном пуле Ig составляют 15-20%) секретируются на поверхность эпителиев, присутствуют в слюне, слезах, молоке, выделяются на поверхность слизистых оболочек, где взаимодействуют с Аг, усиливая защитные свойства слизистых оболочек пищеварительного тракта, дыхательных, половых и мочевыделительных путей. В сыворотке IgA циркулируют в виде мономеров, а в секретируемых SIgA преобладают четырехвалентные димеры, содержащие одну J-цепь и дополнительную полипептидную цепь (синтезируемых эпителиальными клетками секреторный компонент). 4. IgE специфически взаимодействуют с тучными клетками и базофильными лейкоцитами; эти клетки содержат многочисленные гранулы с биологически активными аминами. Защитные потенции IgE направлены преимущественно против гельминтов (нематод). 5. IgD. Биологическая роль этого Ig не установлена; IgD обнаруживают на поверхности развивающихся В-лимфоцитов; в сыворотке здоровых лиц он присутствует в крайне низкой концентрации.
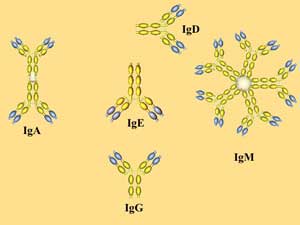
Рис. 7. Антитела разных классов отличаются биологическими свойствами.
Защитные механизмы антител (функции). АТ помогают предотвратить инфицирование и/или элиминировать возбудитель, активируя при этом несколько механизмов.
Опсонизация (иммунный фагоцитоз) - связывание АТ с клеточной стенкой микроорганизма с последующим эффективным поглощением образовавшегося комплекса фагоцитом при взаимодействии Fc-фрагмента АТ с соответствующим Fc-рецептором (FcR) на мембране фагоцита.
Антитоксический эффект. АТ могут связывать и тем самым инактивировать бактериальные токсины.
Активация комплемента. Антитела (IgM и IgG) после связывания с Аг (микроорганизм, опухолевая клетка и др.) могут активировать каскад сывороточных протеаз (систему комплемента), что приводит к уничтожению индуктора в результате перфорации его клеточной стенки, усилению хемотаксиса и иммунного фагоцитоза.
Нейтрализация. Взаимодействуя с рецепторами клетки, связывающими бактерии или вирусы, АТ могут препятствовать адгезии и проникновению микроорганизмов в клетки организма-хозяина.
Антителозависимая цитотоксичность. Распознавание клетки-«мишени» антителами, адсорбированными на Fc-рецепторах NK-клеток, с последующим разрушением их.
Динамика антителообразования Первичный ответ. Появлению АТ предшествует латентный период продолжительностью 3-5 суток. В это время происходит распознавание Аг и образование клонов плазматических клеток. Затем наступает логарифмическая фаза, соответствующая поступлению АТ в кровь; ее продолжительность - 7-15 суток. Постепенно титры АТ достигают пика и наступает стационарная фаза, продолжительнстью 15-30 суток. Ее сменяет фаза снижения титров АТ, длящаяся 1-6 месяцев. Вторичный ответ. После антигенной стимуляции часть В- и Т-лимфоцитов циркулирует в виде клеток памяти. Особенности вторичного иммунного ответа - высокая скорость антителообразования, появление максимальных титров АТ и длительное (иногда многолетнее) их циркулирование. Основные характеристики вторичного ответа:
образование АТ индуцируется значительно меньшими дозами Аг;
индуктивная фаза сокращается до 5-6 ч;
среди АТ доминируют IgG с большой аффинностью, пик их наступает раньше (3-5 сут);
АТ образуются в более высоких титрах и циркулируют в организме длительное время.
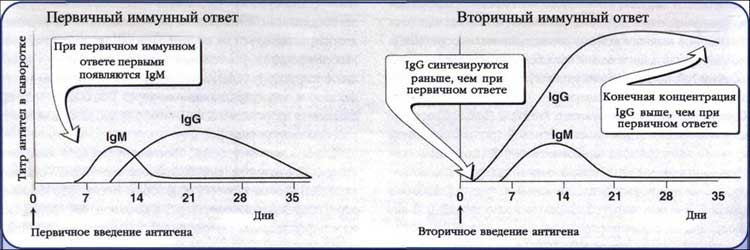
Рис. 8. Антителобразование при первичном и вторичном иммунном ответе.
Структура иммунной системы
