
- •Лекции по физической химии
- •2 Лекция: Законы идеального газа.
- •Энергия. Теплота. Работа.
- •Первый закон термодинамики.
- •Первый принцип термодинамики
- •Теплоёмкость.
- •3 Лекция: Понятие внутренней энергии и энтальпии чистого вещества
- •Термохимия. Энтальпия химических реакций. Закон Гесса
- •Закон Гесса
- •Закон Киркхгоффа
- •Схемы зависимости энтальпий реакций от температуры
- •2Ой Закон термодинамики. Энтропия
- •4 Лекция: 2 закон термодинамики.
- •Постулат Томпсона.
- •Формулировка Оствальда.
- •5 Лекция:
- •Направление процессов открытых многокомпонентных
- •6 Лекция: Фазовое равновесие
- •7 Лекция:
- •8 Лекция:
- •Химическое равновесие
- •Критерий направленности и равновесия в химических реакциях
- •Критерий направленности
- •9 Лекция:
- •10 Лекция: Растворы неэлектролитов. Общие понятия и определения.
- •Межчастичные взаимодействия в растворах.
- •Экспериментальные методы определения парциально – мольных величин.
- •Графический метод.
- •11 Лекция:Основные классы растворов и их термодинамические свойства
- •Совершенные растворы
- •Бесконечно разбавленные растворы
- •Термодинамические свойства бесконечно разбавленного раствора
- •Неидеальные (реальные) растворы
- •Термодинамические условия образования реального раствора
- •1)Равновесие совершенный раствор (пар) Закон Рауля.
- •14 Лекция: Кинетика сложных реакций
Закон Киркхгоффа
Если известно значение энтальпии химической реакции при определенной температуре то с помощью закона Киркхгоффа можно рассчитать ее значение при любой другой температуре
p =const
![]()
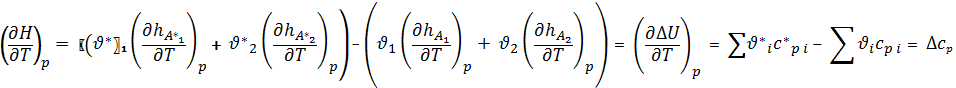
![]()
V = const
![]()
![]() -
разность сумм теплоемкостей продуктов
с учетом стехиометрии
-
разность сумм теплоемкостей продуктов
с учетом стехиометрии
Закон Киркхгоффа
Изменение энтальпии химической реакции равно разности теплоемкостей участников реакции
Таким образом влияние температуры на энтальпию химической реакции обусловлено значением величины . Возможны три случая:
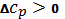 cростом
температуры энтальпия увеличивается
cростом
температуры энтальпия увеличивается
![]()
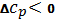 с ростом температуры энтальпия
уменьшается
с ростом температуры энтальпия
уменьшается
![]()
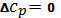 изменение температуры не влияет на
энтальпию реакции
изменение температуры не влияет на
энтальпию реакции
![]()
Схемы зависимости энтальпий реакций от температуры
Теплоемкость исходных веществ растет с температурой быстрее чем продуктов
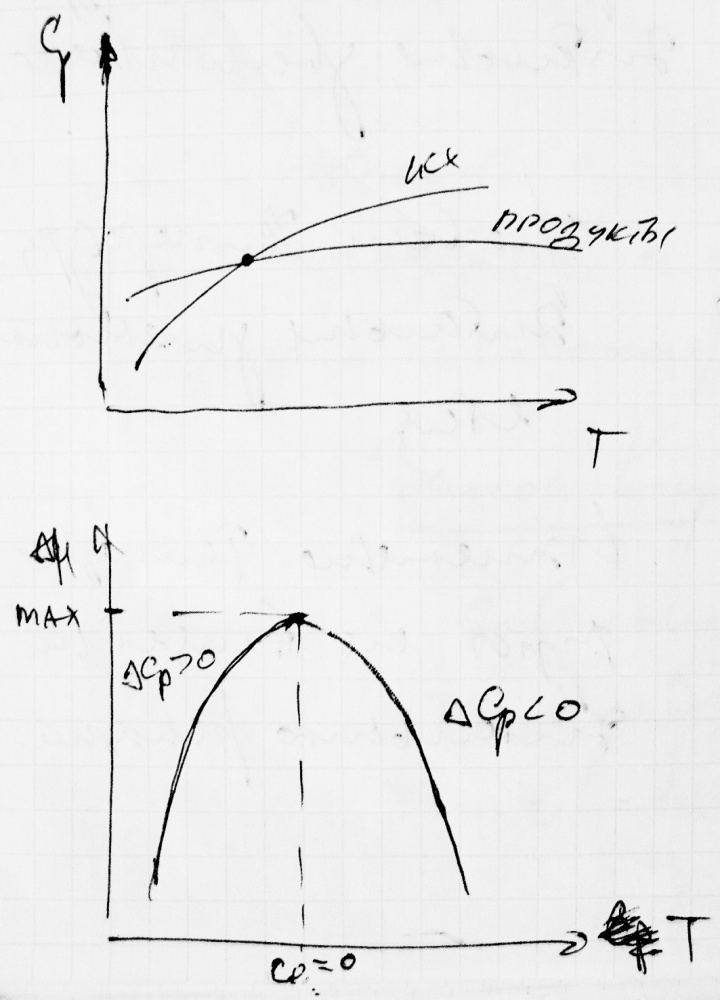
Теплоемкость исходных веществ растет с температурой медленнее чем теплоемкость продуктов
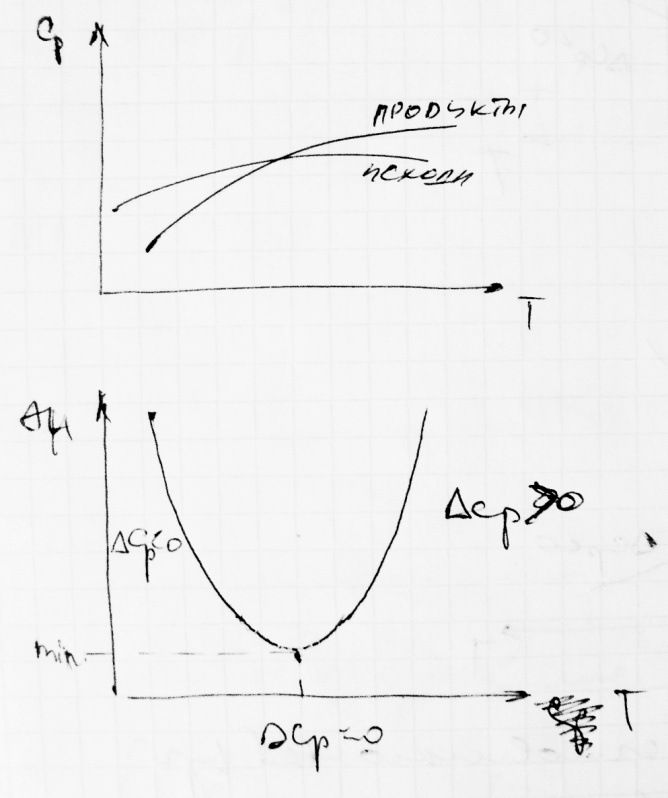
3) Теплоемкость исходного вещества и продуктов возрастает одинаково
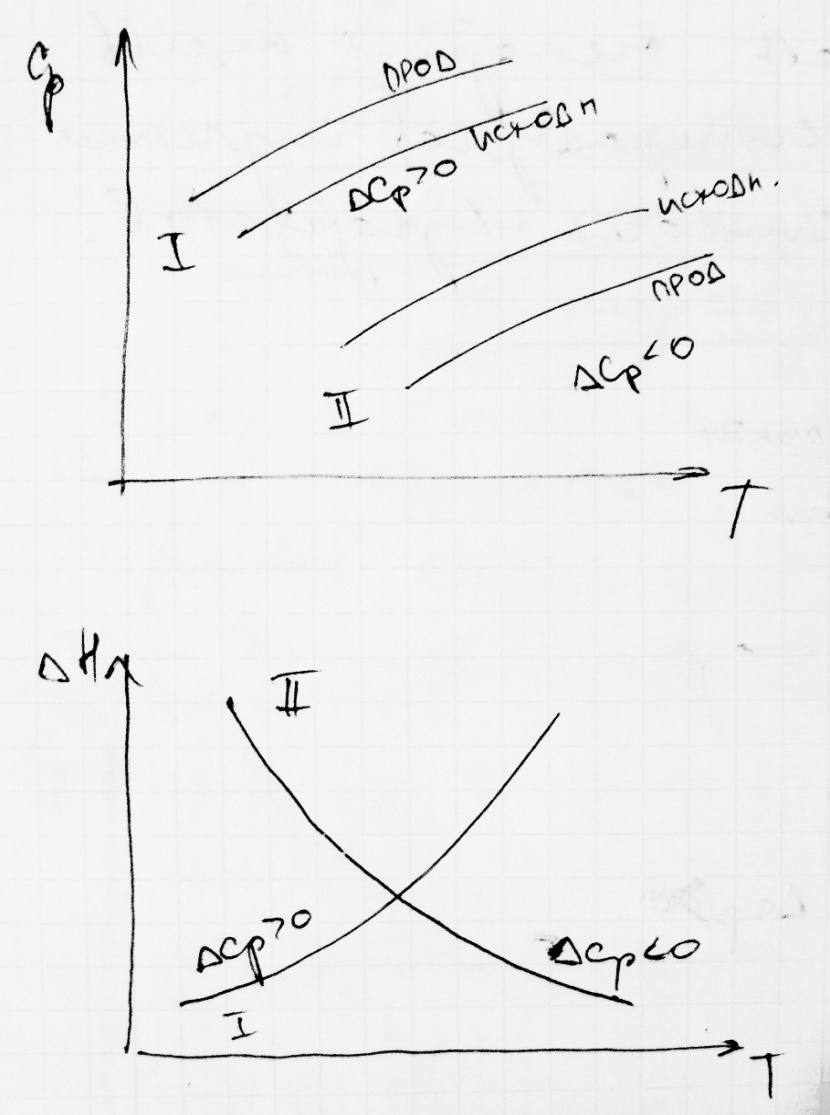
Сумма теплоемкостей продуктов равна сумме теплоемкостей исходных веществ
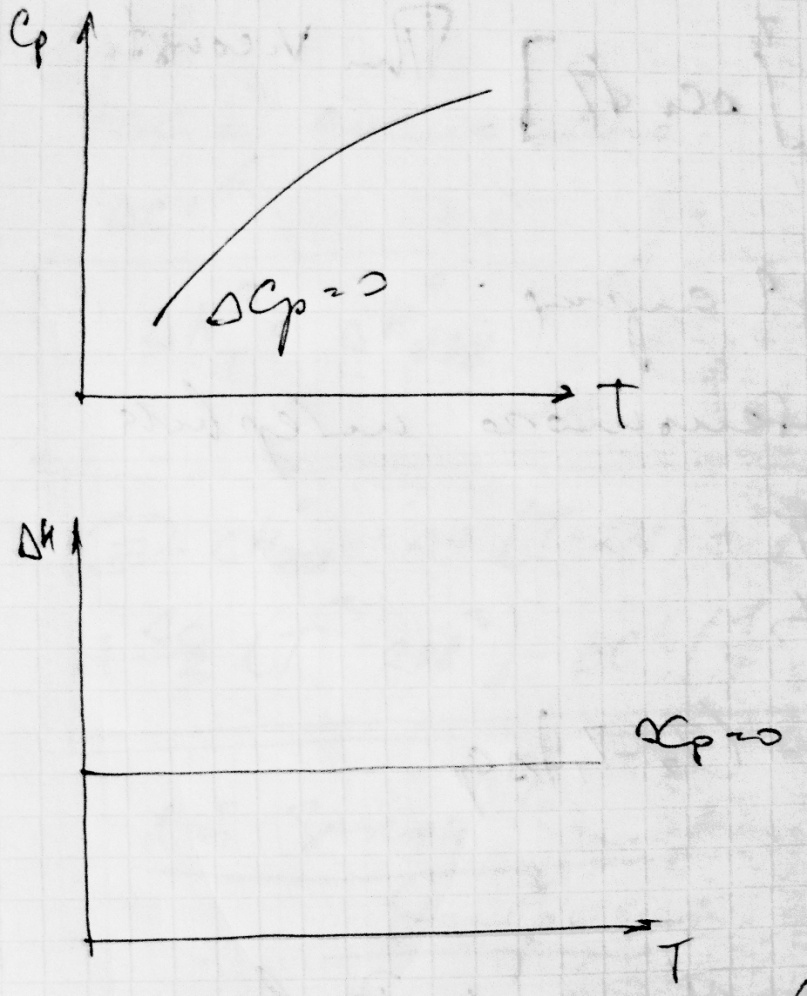
Решение уравнения Киркхгоффа:
а) При T = const
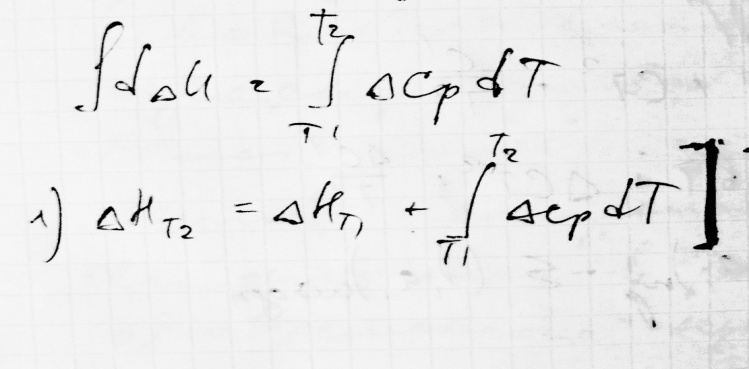
б) При V = const

Возможны 2 случая:
Для небольшого интервала температур

Для большого интервала температур
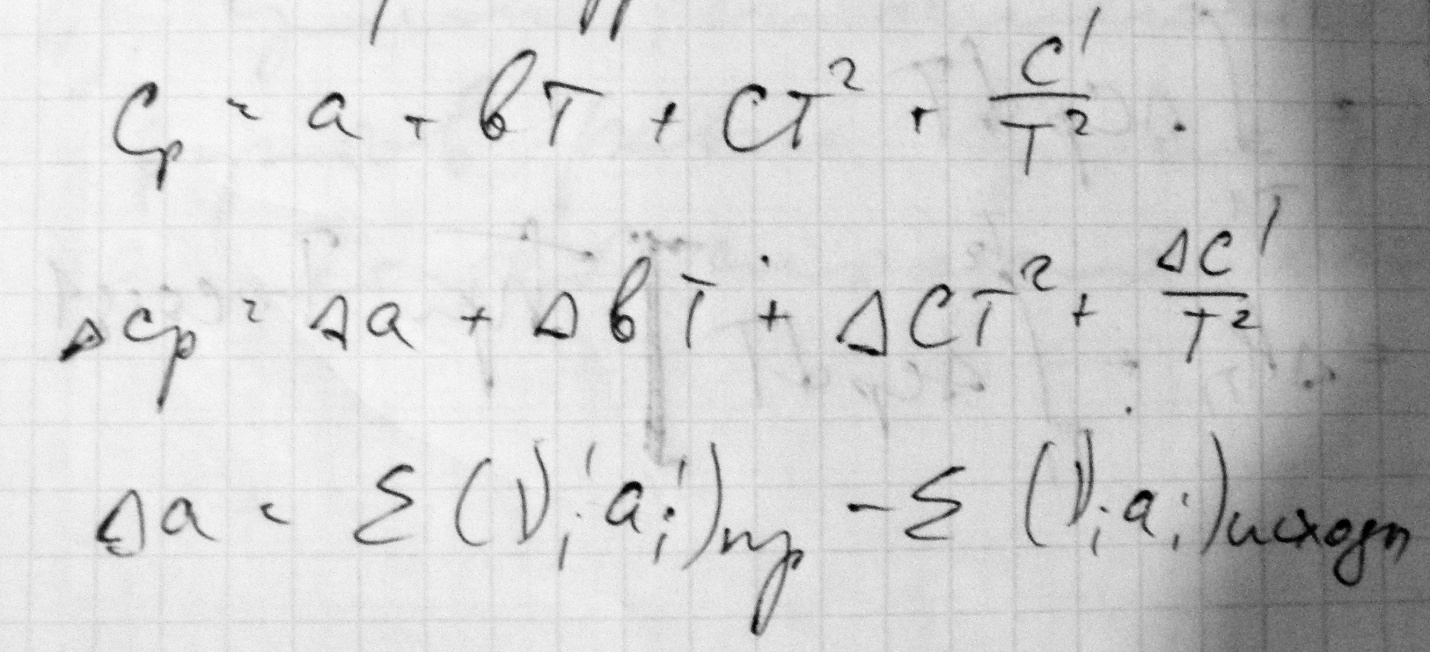
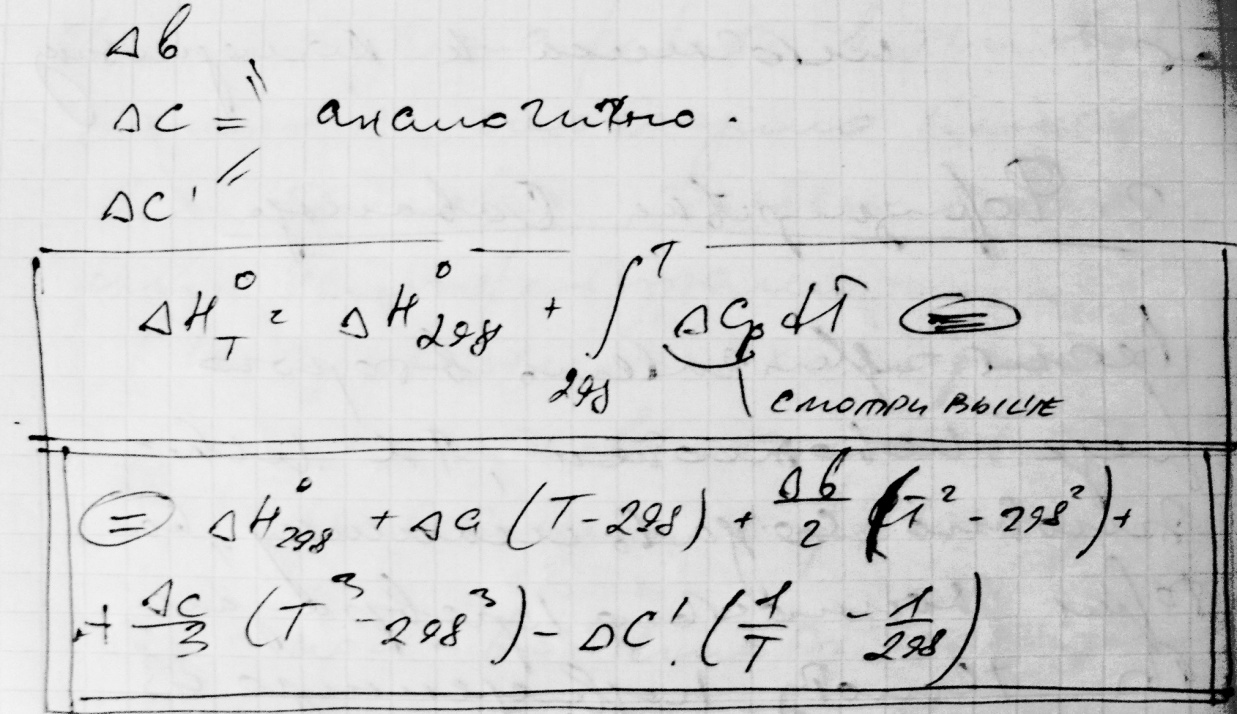
2Ой Закон термодинамики. Энтропия
ПостулатТомпсона
Невозможен циклический процесс результатом которого было бы превращение всей теплоты полученной из теплоисточника в работу без одновременного переноса части от источника к холодильнику
2ая Формулировка Освальда
Вечный двигатель второго рода невозможен т.к. невозможно создать машину которая полностью превратит теплоту подведенную из окружающей среды в работу
Идеальный цикл Карно
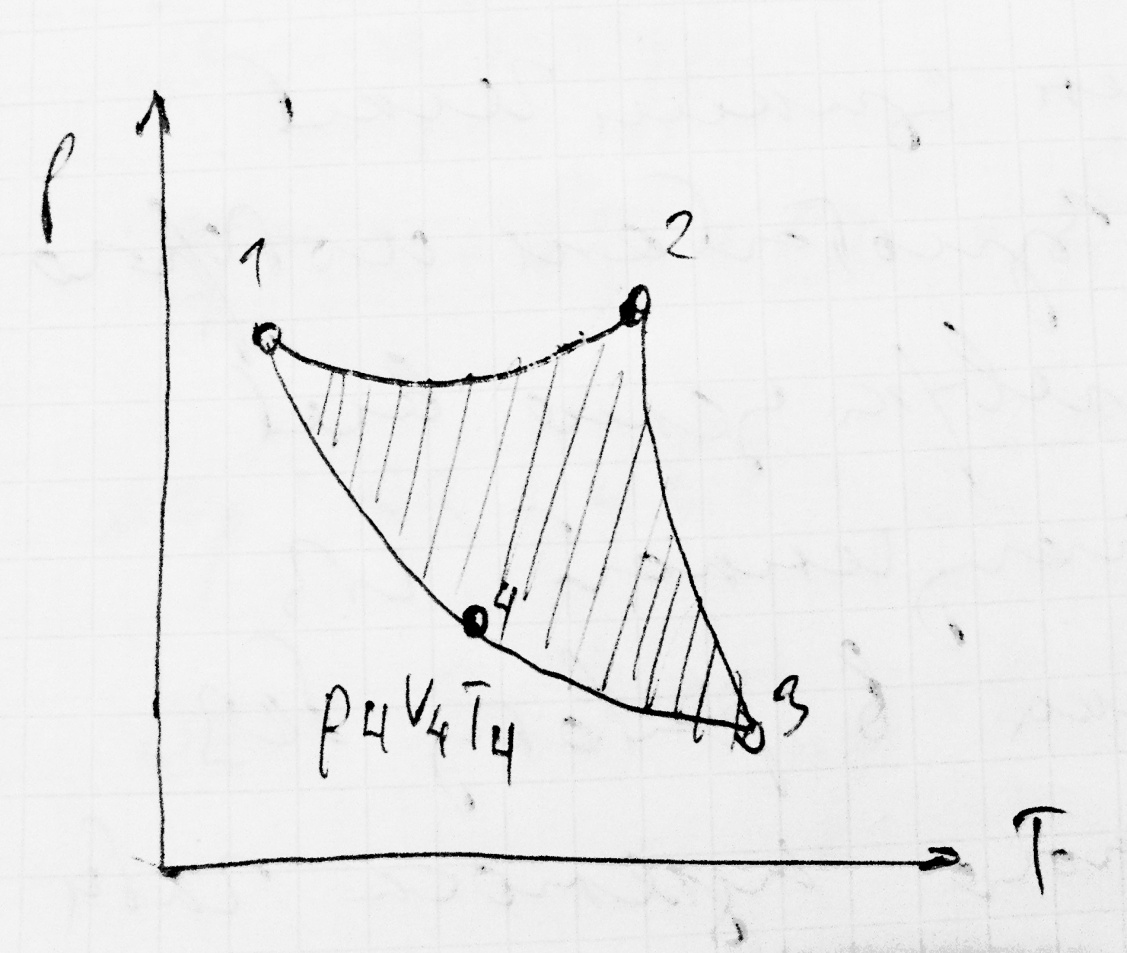
Для получения работы в тепловой машине необходимо наличие 2-х тепловых систем с различными температурами (нагреватель и холодильник)
Q1 – количество теплоты переданное от источника рабочему телу
Q2 – количество теплоты сообщенное рабочим телом холодильнику
1-2 - изотермическое расширение
2-3 - адиабатическое расширение
3-4 - изотермическое сжатие
4-1 - адиабатическое сжатие
Сумарно :
W = Q1- Q2
КПД идеальной тепловой машины не зависит от природы рабочего тела, а зависит только от температуры теплоисточника и холодильника
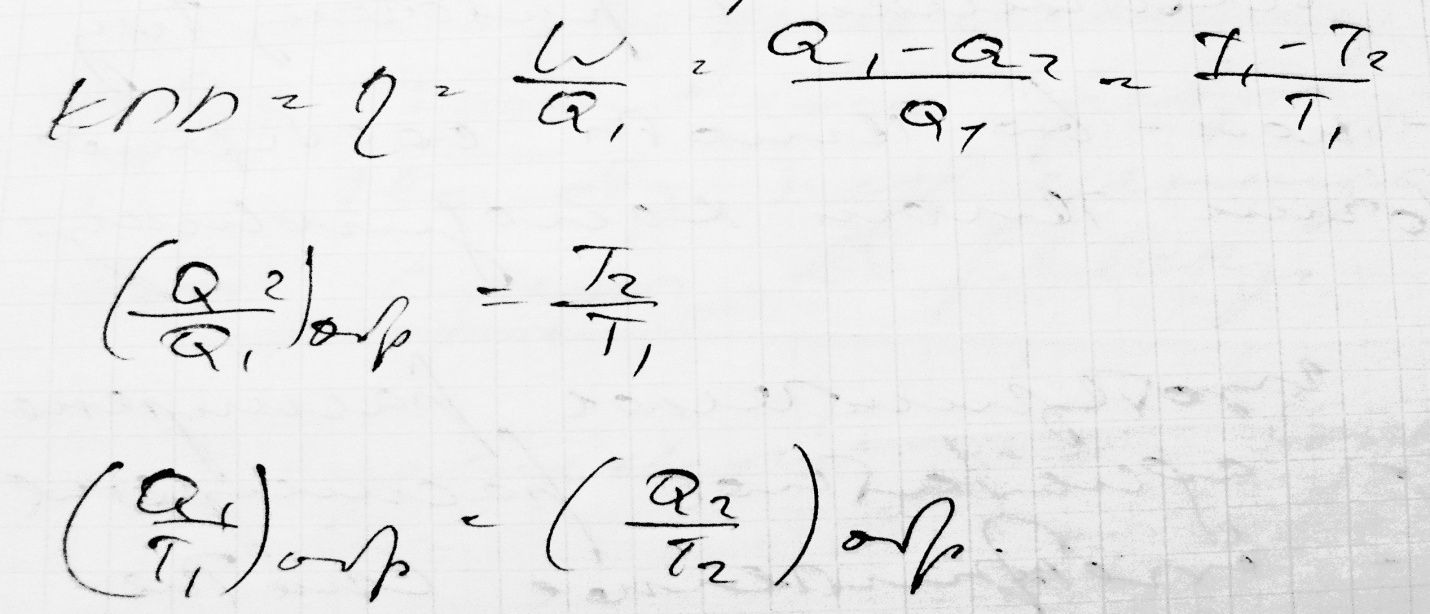

Таким образом получаем, что для цикла алгебраическая сумма подведенных теплот с учетом знаков равна нулю.
Любой произвольный круговой процесс можно разбить на бесконечное множество элементарных циклов Карно
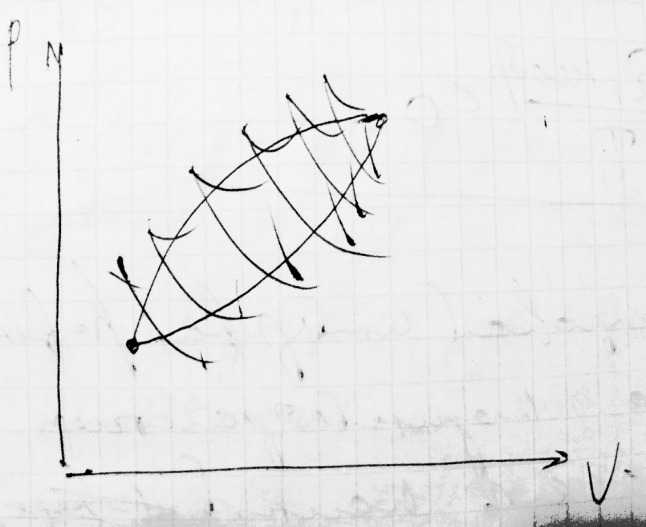
Для каждого малого цикла:
Первое обобщение Клаузиуса для равновесных циклов
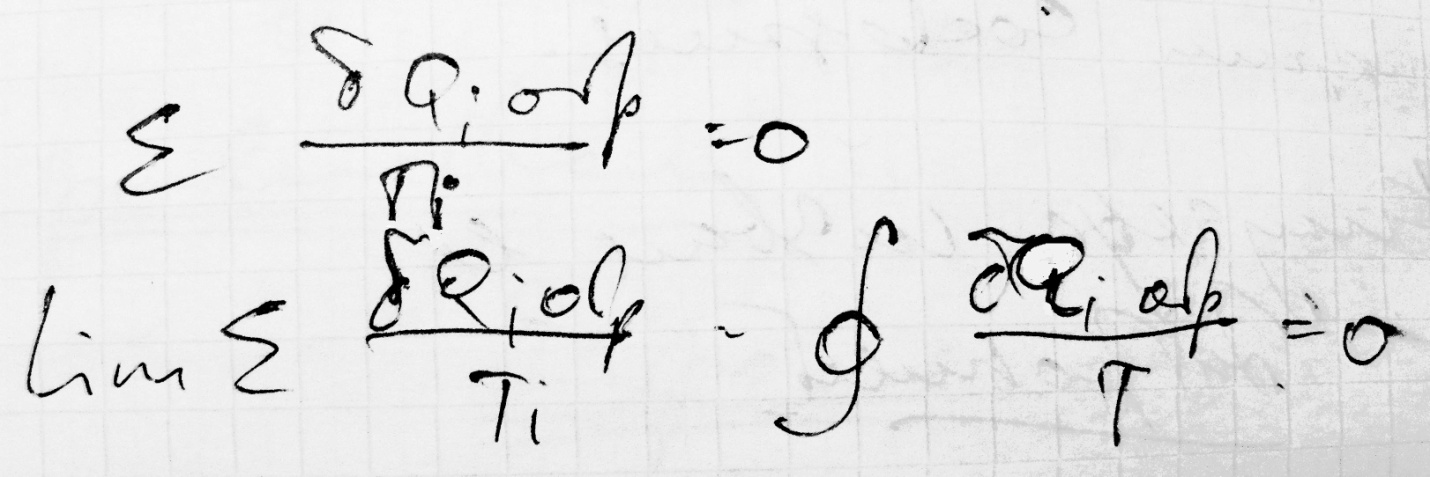
2ое обобщение Клаузиуса для реальных циклов
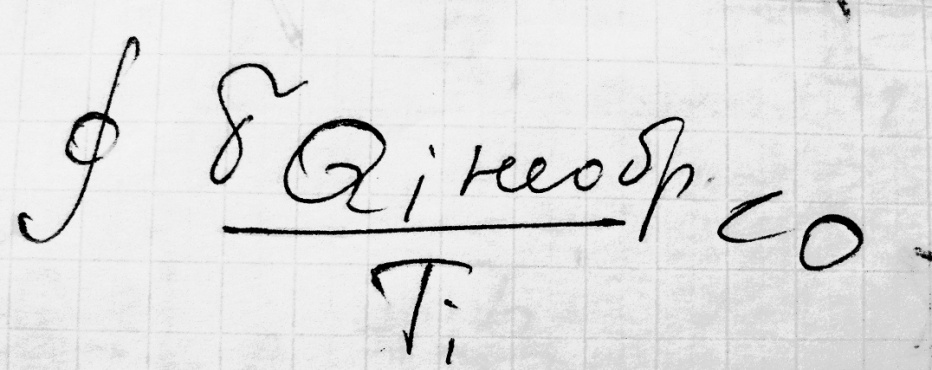
Если круговой интервал равен нулю то подинтегральная величина есть полный дифференциал некоторой функции состояния.Клаузиус назвал ее энтропией
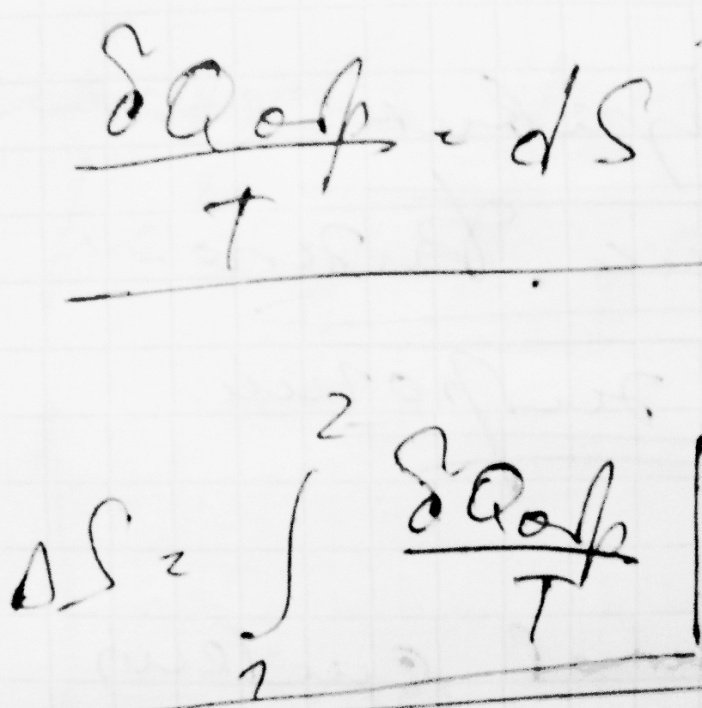
Энтропия – это функция состояния, ее изменение не зависит от пути протекания, но изменение энтропии можно вычислить лишь на обратимом пути.
4 Лекция: 2 закон термодинамики.
Энтропия.
Постулат Томпсона.
Невозможен циклический процесс единственным результатом, которого было бы превращение всей теплоты полученной от теплоисточника в работу без одновременного переноса части теплоты от теплоисточника к холодильнику.
