- •Лекции по физической химии
- •2 Лекция: Законы идеального газа.
- •Энергия. Теплота. Работа.
- •Первый закон термодинамики.
- •Первый принцип термодинамики
- •Теплоёмкость.
- •3 Лекция: Понятие внутренней энергии и энтальпии чистого вещества
- •Термохимия. Энтальпия химических реакций. Закон Гесса
- •Закон Гесса
- •Закон Киркхгоффа
- •Схемы зависимости энтальпий реакций от температуры
- •2Ой Закон термодинамики. Энтропия
- •4 Лекция: 2 закон термодинамики.
- •Постулат Томпсона.
- •Формулировка Оствальда.
- •5 Лекция:
- •Направление процессов открытых многокомпонентных
- •6 Лекция: Фазовое равновесие
- •7 Лекция:
- •8 Лекция:
- •Химическое равновесие
- •Критерий направленности и равновесия в химических реакциях
- •Критерий направленности
- •9 Лекция:
- •10 Лекция: Растворы неэлектролитов. Общие понятия и определения.
- •Межчастичные взаимодействия в растворах.
- •Экспериментальные методы определения парциально – мольных величин.
- •Графический метод.
- •11 Лекция:Основные классы растворов и их термодинамические свойства
- •Совершенные растворы
- •Бесконечно разбавленные растворы
- •Термодинамические свойства бесконечно разбавленного раствора
- •Неидеальные (реальные) растворы
- •Термодинамические условия образования реального раствора
- •1)Равновесие совершенный раствор (пар) Закон Рауля.
- •14 Лекция: Кинетика сложных реакций
Экспериментальные методы определения парциально – мольных величин.
А)Если известна зависимость между функцией и составом, то взяв частную производную этой функции по составу V=f(n) можно найти п.м.в. компонента
![]()
Б) Для бинарного раствора можно воспользоваться уравнением Гиббса-Дюгема:
![]()
![]()
Графический метод.
А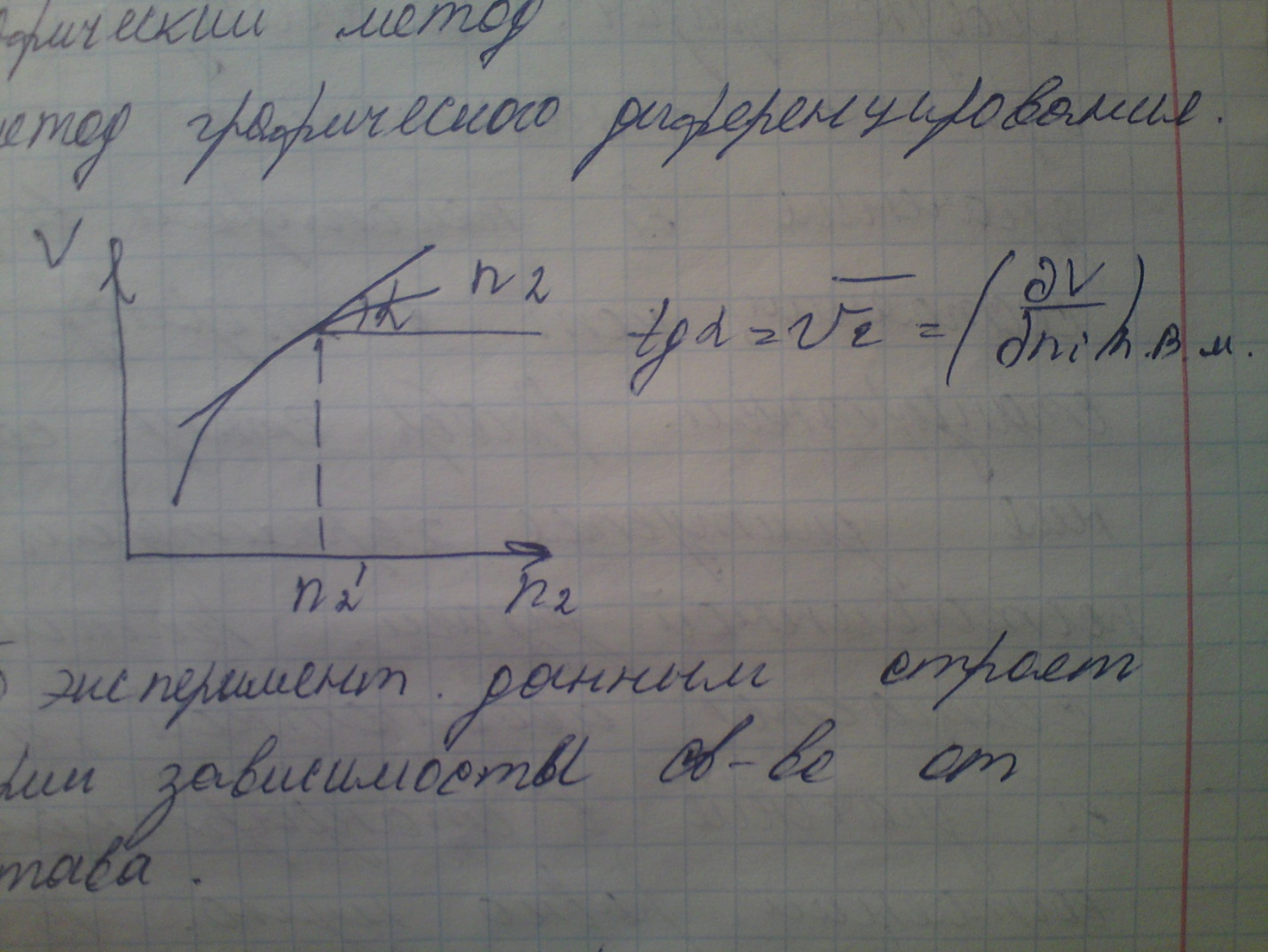 )
Метод графического дифференцирования
)
Метод графического дифференцирования
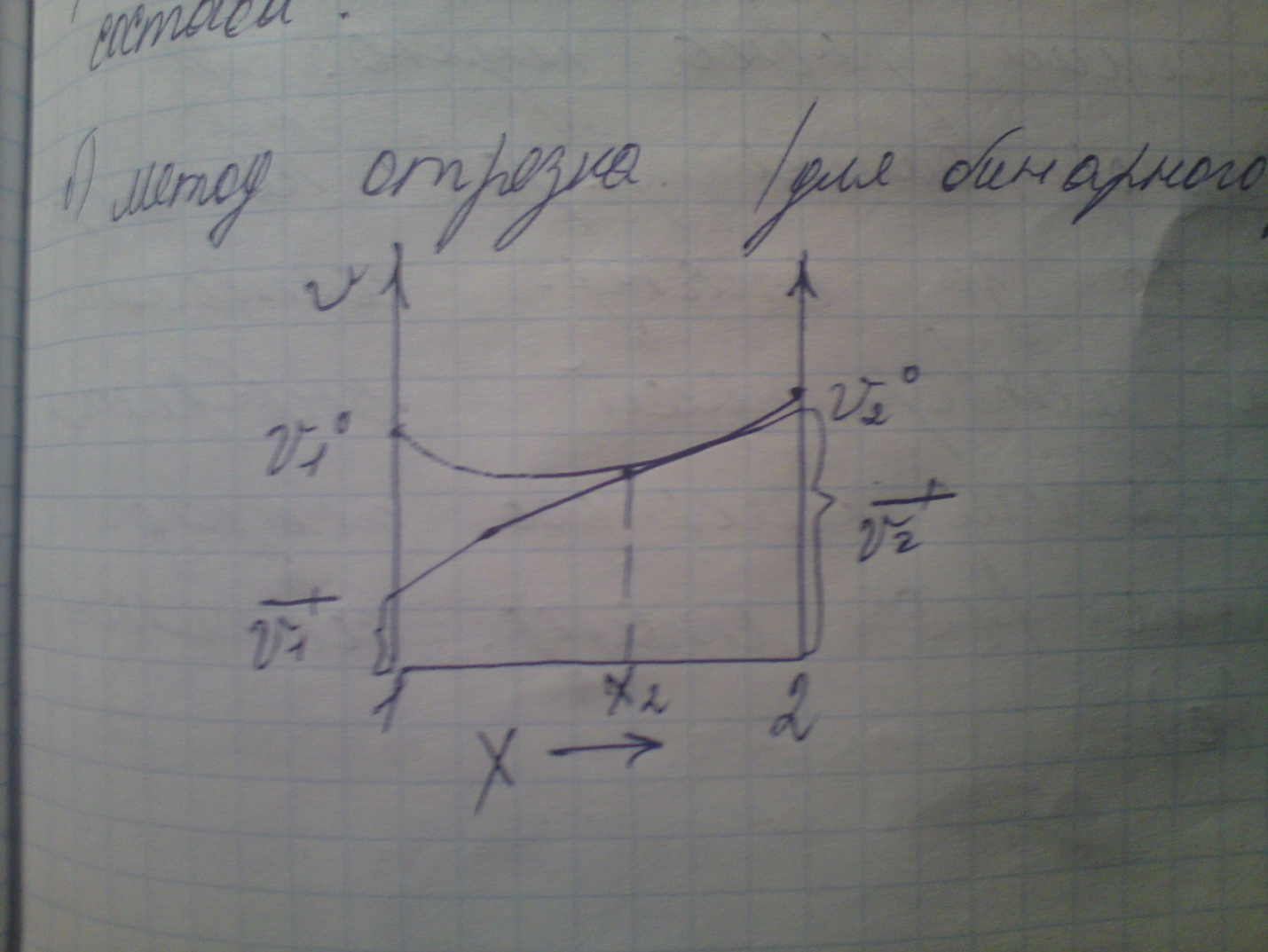
Б) Метод отрезка (для бинарного раствора)
Стандартные состояния в термодинамике жидких растворов.
Любую физическую величину можно определить относительно её значения в некотором выбранном состоянии, которое в термодинамике называют стандартным. Выбор стандартного состояния диктуется характером поставленной задачи. Величина считается абсолютной, если её значение в стандартном состоянии равно нулю. В термодинамике растворов неэлектролитов за стандартные состояния для растворителей выбирается состояние чистого жидкого растворителя (первое стандартное состояние 0)
Д ля
растворённого вещества принимается
или состояние чистого жидкого растворённого
вещества (1 стандартное состояние) или
состояние гипотетического растворённого
аещества (второе стандартное состояние
0)
ля
растворённого вещества принимается
или состояние чистого жидкого растворённого
вещества (1 стандартное состояние) или
состояние гипотетического растворённого
аещества (второе стандартное состояние
0)
Гипотетическое вещество- это вещество такого же химического состава, что и реальное растворённое вещество, но со свойствами частиц, которыми они обладали бы в бесконечно разбавленном растворе, где нет взаимодействия между частицами.
Химический потенциал компонентов жидкого идеального раствора.
Пусть при T,P-const жидкий раствор находится в равновесии со своим паром, который можно считать идеальным газом.
![]()

пар
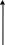
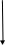
жид.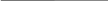
11 Лекция:Основные классы растворов и их термодинамические свойства
Все растворы подразделяются на:
Идеальные
Для них выполняется условие
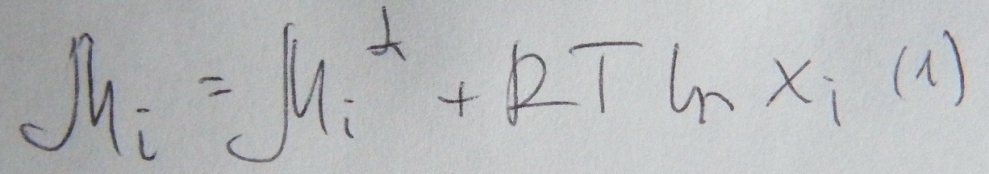
Они делятся на:
а) совершенные растворы
б) бесконечно разбавленные растворы
2) Реальные
Для них зависимость не выполняется
Совершенные растворы
По Гиббсу раствор называется совершенным если для каждого компонента, т.е. и для растворенного вещества, во всей области существования концентрации выполняется условие
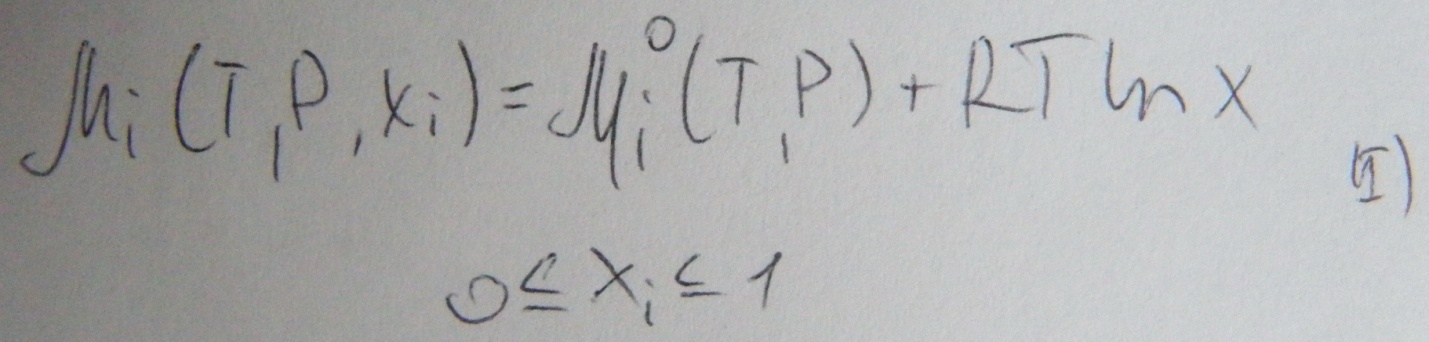
Тогда запишем выражение для химического потенциала растворителя и растворенного вещества в совершенном растворе.
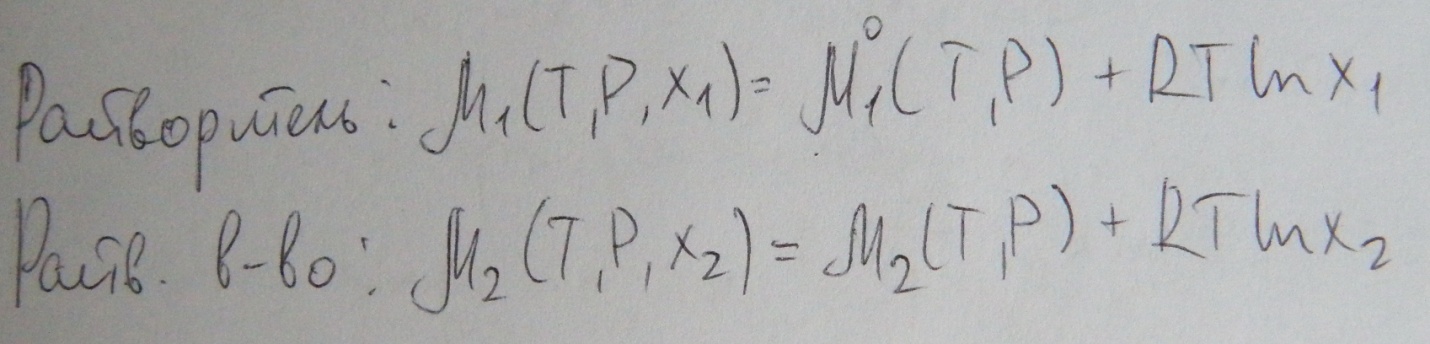
Таким образом в совершенных растворах для растворителя и растворенного вещества одинаковое, а именно первое
Совершенные растворы образуют вещества близкие по своим физико-химическим свойствам. Например смесь оптических изомеров или смесь веществ одного гомологического ряда
Термодинамические свойства совершенного раствора
Продиференцируем уравнение
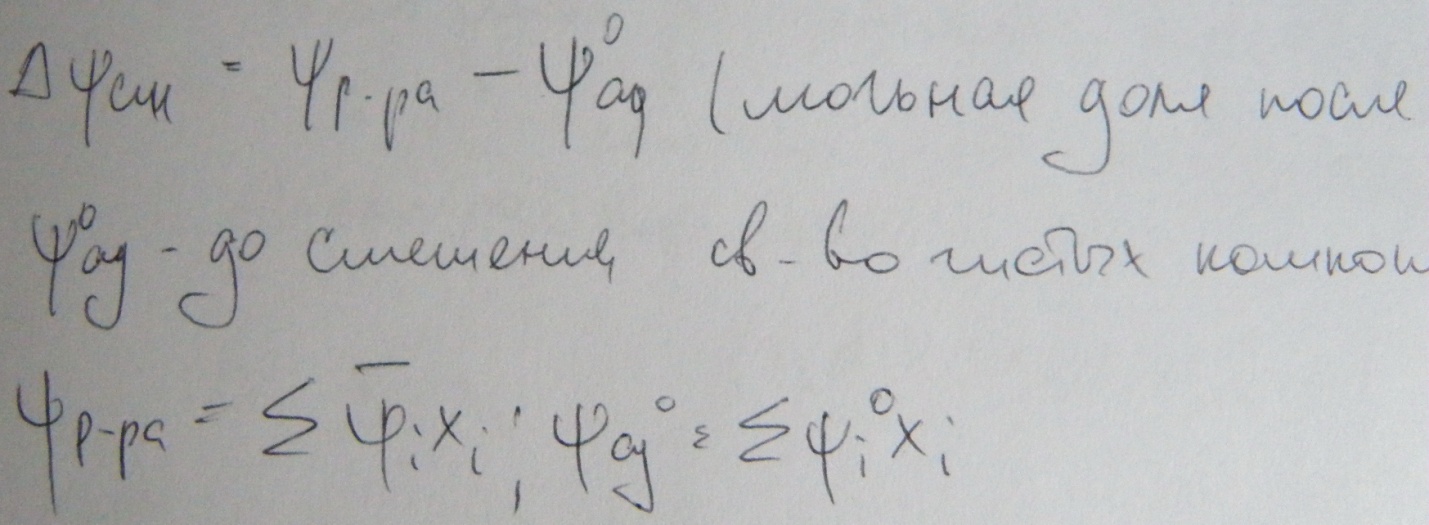
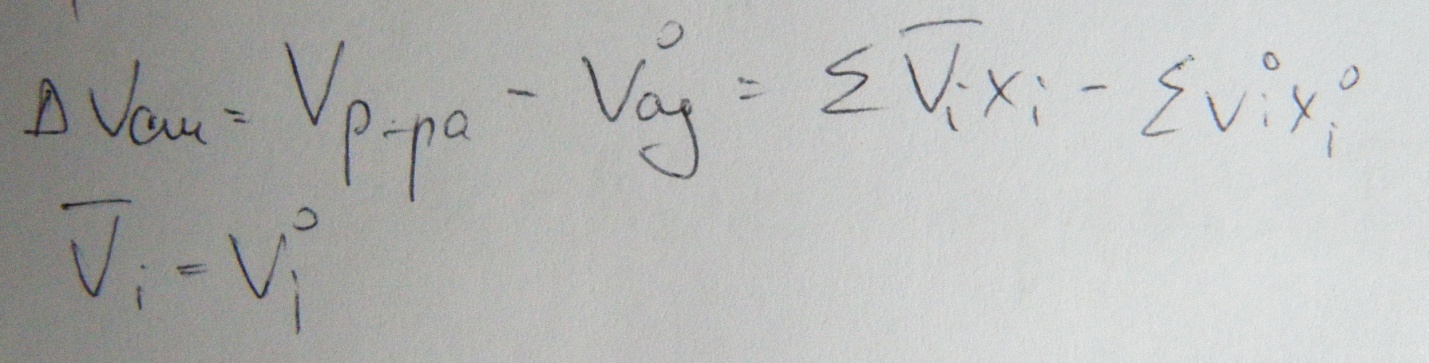
Таким образом получаем
(Образование совершенного раствора происходит без изменения обьема)
Разделим уравнение
(1) на Т и продиференцируем по Т при![]()

Образование совершенного раствора проходит без изменений теплового эффекта реакции
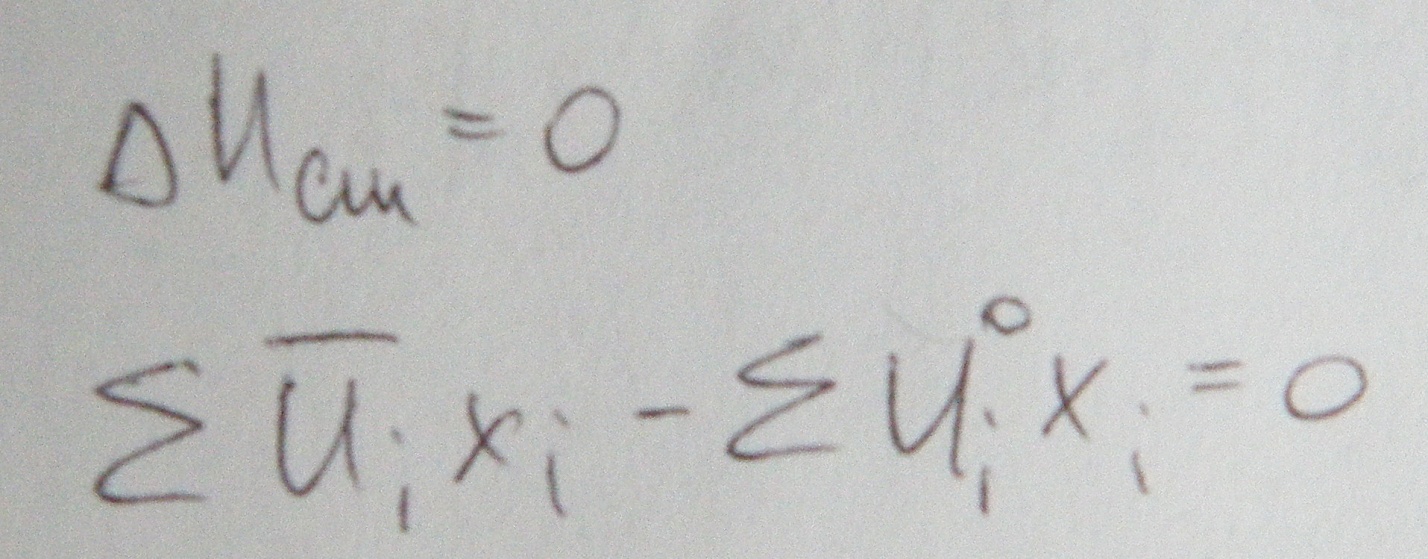
Образование совершенного раствора проходит без изменения внутренней энергии
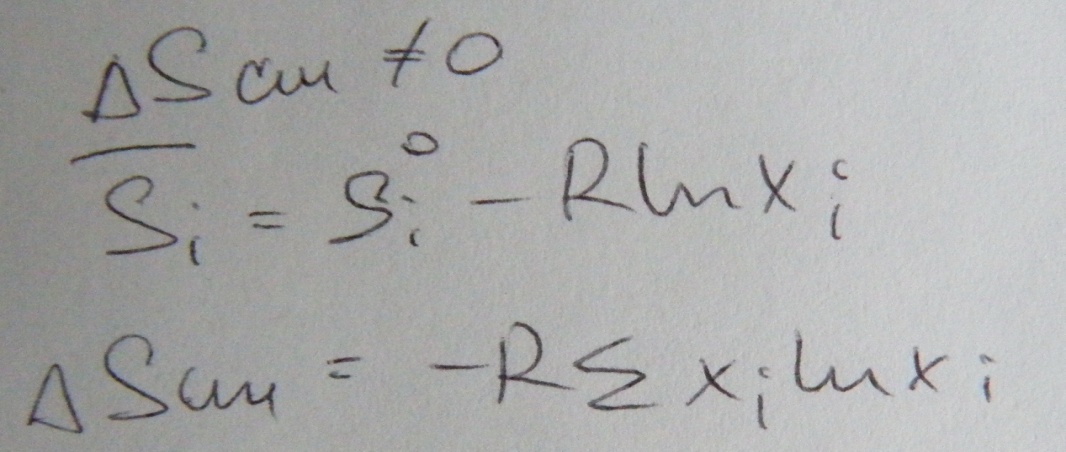
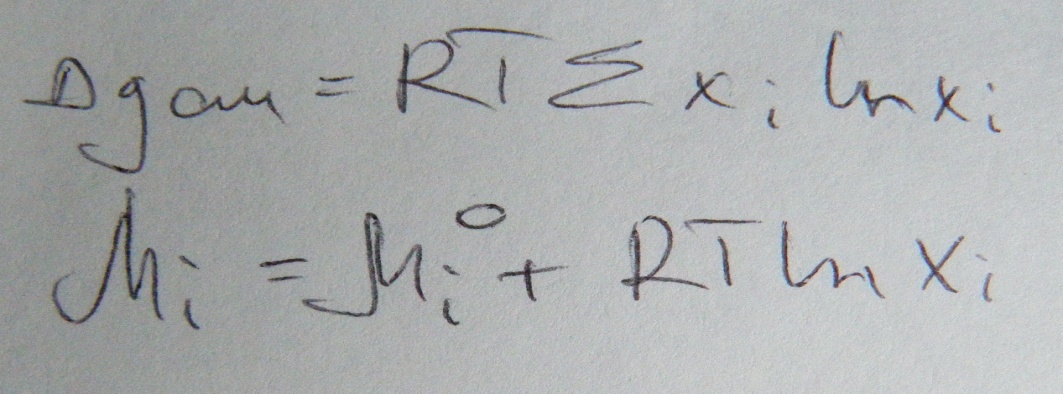
Если рассмотреть бинарный раствор то будет справедлив закон Рауля