
- •Лекции по физической химии
- •2 Лекция: Законы идеального газа.
- •Энергия. Теплота. Работа.
- •Первый закон термодинамики.
- •Первый принцип термодинамики
- •Теплоёмкость.
- •3 Лекция: Понятие внутренней энергии и энтальпии чистого вещества
- •Термохимия. Энтальпия химических реакций. Закон Гесса
- •Закон Гесса
- •Закон Киркхгоффа
- •Схемы зависимости энтальпий реакций от температуры
- •2Ой Закон термодинамики. Энтропия
- •4 Лекция: 2 закон термодинамики.
- •Постулат Томпсона.
- •Формулировка Оствальда.
- •5 Лекция:
- •Направление процессов открытых многокомпонентных
- •6 Лекция: Фазовое равновесие
- •7 Лекция:
- •8 Лекция:
- •Химическое равновесие
- •Критерий направленности и равновесия в химических реакциях
- •Критерий направленности
- •9 Лекция:
- •10 Лекция: Растворы неэлектролитов. Общие понятия и определения.
- •Межчастичные взаимодействия в растворах.
- •Экспериментальные методы определения парциально – мольных величин.
- •Графический метод.
- •11 Лекция:Основные классы растворов и их термодинамические свойства
- •Совершенные растворы
- •Бесконечно разбавленные растворы
- •Термодинамические свойства бесконечно разбавленного раствора
- •Неидеальные (реальные) растворы
- •Термодинамические условия образования реального раствора
- •1)Равновесие совершенный раствор (пар) Закон Рауля.
- •14 Лекция: Кинетика сложных реакций
2 Лекция: Законы идеального газа.
Идеальным называется газ, в котором отсутствует межмолекулярное взаимодействие.
Закон Бойля-Мариотта
VP=const m-постоянна
![]() =
=![]()
![]()
Закон Гей-Люсакка
P-const
Объём прямо пропорционален его постоянной температуре.
![]()
![]() коэффициент
объёмного расширения.
коэффициент
объёмного расширения.
![]()
![]()
T,
K=273,16+t,![]() C
C
Закон Шарля
При постоянном объёме давление прямо пропорционально температуре.
![]()
![]()
Закон Авогадро
При одинаковых Р и Т в равных объёмах различных идеальных газов, содержится равное количество молекул.
При одинаковых Р и Т, 1 моль идеальных газов занимает одинаковый объём. При нормальных условиях (Т0=0 С, Р=1 атм.) 1 моль всех идеальных газов занимает V=22,4, Vm=22,4 л/моль.
Закон Дальтона
Общее давление смеси идеального газа равно сумме давлений компонентов составляющих смесь.
Р
общ.= +
+![]() +
+…
+
+…
Общее число моль газов в смеси равно сумме молей отдельного газа.
n общ.=nA+nB+nC+…
На основе этих законов: уравнение Менделеева-Клаперона
P*V=R*T
P*V=n*R*T (для n моль)
R-универсальная газовая постоянная. R=8,312 Дж/моль*К
XA
Доля, которая составляет число молей для данного газа от общего числа смеси называется мольной долей.
Энергия. Теплота. Работа.
Неотъемлемым свойством материи является движение. Мерой движения при его переходе из одной формы в другую является энергия. Энергия- способность к совершению работы или переносу теплоты.
Энергия включает:
Кинетическую энергию движения системы
Потенциальную энергию положения системы во внешнем поле
Внутреннюю энергию
В термодинамике рассматривают неподвижные системы и в отсутствие внешнего поля, поэтому полная энергия будет равна внутренней. Внутренняя энергия- энергия всех микрочастиц, составляющих систему. Она включает в себя энергию поступательного, вращательного и колебательного движения молекул, энергию межмолекулярного взаимодействия, кинетическую энергию движения электронов вокруг ядра, потенциальную энергию взаимодействия электронов и ядер и внутреннюю энергию. Внутренняя энергия зависит от природы вещества, массы и параметра состояния, является экстенсивным свойством системы. Внутренняя энергия является функцией состояния(dU). Внутренняя энергия идеального газа не зависит от V,P.
![]()
![]()
Существует две формы передачи энергии:
1) Мерой энергии при её передаче за счёт хаотического столкновения частиц соприкосновения тел является теплота. Это микроскопическая форма передачи энергии, она не связана с переносом вещества.
2) Мерой энергии при её передаче за счёт направления перемещения масс под действием каких-либо сил является работа(макроскопическая форма передачи энергии).
![]()
В химических реакциях единственной работой является объёмная.
![]()
Выражение для работы в применение к различным процессам.
Изохорный V=const
![]()
Изобарный P=const
![]()
![]()
![]()
![]()
Изотермический Т=const
![]()

Адиабатный
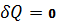
![]()
![]()
W=![]()
Первый закон термодинамики.
Закон сохранения энергии
Энергия не возникает из ничего и не исчезает бесследно, она переходит только из одной формы в другую в строго эквивалентных количествах.
Вечный двигатель первого рода не возможен. Не возможно создать периодически действительную тепловую машину, которая создавала бы работу без затраты теплоты из окружающей среды.
Если система совершает круговой процесс, то суммарная работа эквивалентна теплоте.
![]()
B
1

2
3
A
A1B2A
A1B3A
![]()
![]()
![]()
Аналогично
![]()
Q![]() W=const
W=const
Мы получили, что разница Q W=const не зависит от пути, то эта разность есть изменение некоторого свойства системы.
Q-W=![]() U
U
