
- •Раздел 2
- •Глава 11
- •11.1. Общая характеристика
- •11.2. Виды гравиметрических определений
- •11.3. Понятие о механизме образования осадка
- •11.4. Коллоидная стадия образования осадка
- •11.5. Причины загрязнения осадка и способы их устранения
- •11.6. Основные этапы методики гравиметрического определения методом осаждения
- •11.7. Гравиметрия в фармацевтическом анализе
- •Глава 12
- •12.1. Основные понятия титриметрии
- •12.2. Классификация титриметрических методов анализа и способов титрования
- •12.3. Стандартные растворы и стандартные вещества
- •12.4. Расчёты, связанные с приготовлением растворов титрантов и титрованием Расчёты, связанные с приготовлением растворов
- •Расчёты, связанные с титрованием
- •Глава 13
- •13.1. Титранты и стандартные вещества
- •13.2. Обнаружение конечной точки титрования. Кислотно-основные индикаторы
- •Метиловый красный
- •Тимолфталеин (бесцветный синий)
- •Феноловый красный
- •13.3. Кривые титрования
- •0,10 М раствором NaOh
- •Расчёты для построения кривой титрования
- •Расчёты для построения кривой титрования
- •0,10 М Na2co3 0,10 м раствором hCl
- •13.4. Факторы, влияющие на величину скачка титрования
- •13.5. Погрешности титрования
- •13.6. Некоторые случаи практического применения кислотно-основного титрования в водных растворах
- •Глава 14
- •14.1. Ограничения возможностей кислотно-основного основного титрования в водных растворах
- •14.2. Критерии выбора растворителя для кислотно-основного титрования
- •14.3. Применение в фармацевтическом анализе Титрование в кислотных растворителях
- •Глава 15
- •15.1. Общая характеристика
- •15.2. Меркуриметрическое титрование
- •15.3. Комплексонометрическое титрование
- •15.3.1. Понятие о комплексонах
- •15.3.2. Свойства этилендиаминтетрауксусной кислоты и её взаимодействие с катионами металлов
- •15.3.3. Кривые титрования
- •1,010-3 М раствором эдта при рН 9,50 в присутствии 510-2 м nh3
- •15.3.4. Способы обнаружения конечной точки титрования. Металлоиндикаторы
- •Пирокатехиновый фиолетовый – металлоиндикатор из группы сульфофталеиновых красителей. Представляет собой четырёхосновную кислоту. Комплексы с металлами обычно окрашены в синий цвет.
- •15.3.5. Индикаторные погрешности
- •15.3.6. Титранты и стандартные вещества
- •15.3.7. Способы комплексонометрического титрования и его применение
- •Глава 16
- •16.1. Общая характеристика
- •16.2. Аргентометрическое титрование
- •16.2.1. Кривые титрования
- •Расчёты для построения кривой титрования
- •16.2.2. Способы обнаружения конечной точки титрования
- •Метод Мора
- •Метод Фольгарда
- •Особенность определения хлоридов
- •Особенность определения иодидов
- •Метод Фаянса
- •16.2.3. Титранты и стандартные вещества
- •16.2.4. Применение в фармацевтическом анализе
- •16.3. Меркурометрическое титрование
- •Глава 17
- •17.1. Общая характеристика и классификация
- •17.2. Кривые титрования
- •17.3. Способы обнаружения конечной точки титрования. Окислительно-восстановительные индикаторы
- •Глава 18
- •18.1. Иодометрическое титрование
- •Титранты и стандартные вещества
- •Обнаружение конечной точки титрования
- •18.2. Хлориодометрическое титрование
- •18.3. Иодатометрическое титрование
- •18.4. Броматометрическое титрование
- •18.5. Нитритометрическое титрование
- •18.6. Перманганатометрическое титрование
- •18.8. Дихроматометрическое титрование
- •18.8. Цериметрическое титрование
Особенность определения хлоридов
Растворимость AgCl примерно на порядок больше, чем у AgSCN, поэтому осадок AgCl, образовавшийся на первом этапе титриметрического определения, может реагировать со вторым титрантом:
AgCl + SCN- AgSCN + Cl-
Для титрования расходуется большее, чем необходимо, количество NH4SCN, и окончательный результат содержит отрицательную погрешность, величина которой может достигать 5%. Для того чтобы такое не происходило, можно провести одну из следующих операций:
-
осадок AgCl отделяют от раствора фильтрованием;
-
уменьшают площадь поверхности осадка AgCl – при нагревании или сильном встряхивании осадок подвергается коагуляции;
-
отделяют осадок AgCl от раствора слоем более тяжёлого, чем вода органического растворителя, например, нитробензола.
Особенность определения иодидов
Иодид-ионы могут окисляться ионами Fe3+. Поэтому при определении I- методом Фольгарда к анализируемому раствору вначале добавляют избыток стандартного раствора AgNO3 и лишь затем железоаммонийные квасцы. Образовавшийся AgI не окисляется ионами Fe3+.
Метод Фаянса
В данном методе для обнаружения конечной точки титрования используют адсорбционные индикаторы.
Адсорбционными индикаторами называются вещества, адсорбция или десорбция которых осадком сопровождается изменением окраски в точке эквивалентности или вблизи неё.
В качестве адсорбционных индикаторов в аргентометрическом титровании чаще всего используют флуоресцеин и его галогенопроизводные (дихлорфлуоресцеин, эозин, флоксин, эритрозин), а также сульфофталеины (бромфеноловый синий), родамины (родамин 6G) и другие вещества. Большинство индикаторов имеют окрашенные анионы. Родамины являются катионными красителями.
Действие индикаторов в методе Фаянса связано с их адсорбцией в качестве противоионов на заряженной поверхности осадка.

В результате адсорбции изменяется электронная структура индикатора и его окраска. Например, флуоресцеин, находящийся в растворе, имеет жёлтую окраску, а адсорбированный на осадке – розовую; эозин, соответственно, оранжевую и красно-фиолетовую.
Сами индикаторы не должны выступать в качестве потенциалопределяющих ионов, так как при этом они будут адсорбироваться на осадке до точки эквивалентности. Способность различных анионов замещать друг друга на поверхности осадка галогенида серебра уменьшается в следующем порядке:
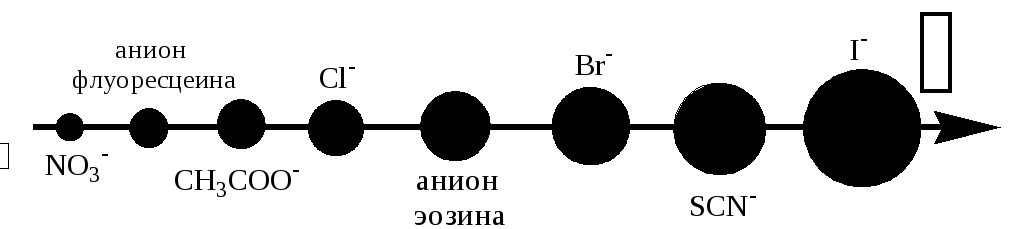
Анион флуоресцеина адсорбируется на осадке слабее всех галогенид-ионов и поэтому может быть использован в качестве индикатора при титровании хлоридов, бромидов и иодидов. Эозин адсорбируется лучше хлорид-ионов. Данный индикатор нельзя применять для обнаружения конечной точки титрования хлоридов, так как он будет адсорбироваться на осадке AgCl ещё до достижения точки эквивалентности.
Для того чтобы индикатор мог адсорбироваться на заряженной поверхности осадка, он должен находиться в растворе в ионизированном виде. Ионизация, а, следовательно, и способность индикатора к адсорбции зависят от рН.
Рассмотрим, как влияет рН на индикаторные свойства флуоресцеина и его тетрабромпроизводного – эозина. Данные соединения являются двухосновными кислотами, причём у флуоресцеина более сильными кислотными свойствами обладает карбоксильная группа, а у эозина, вследствие электроноакцепторного действия атомов брома – фенольный гидроксил.

На осадке адсорбируются анионные формы флуоресцеина и эозина, содержащие ионизированный фенольный гидроксил. У флуоресцеина – это дианион, у эозина – моно- и дианион. Исходя из значений pKa, достаточное количество дианиона флуоресцеина будет находиться в растворе лишь при рН > 6-7, поэтому титрование с данным индикатором проводят при рН 7 – 10 (верхняя граница связана с образованием осадка оксида серебра). Титрование с эозином можно проводить при рН 2,5-3 Для создания такой кислотности среды используют уксусную кислоту.
Чёткость обнаружения конечной точки с помощью адсорбционных индикаторов тем выше, чем больше индикатора адсорбируется на осадке. Количество адсорбированного индикатора, в свою очередь, зависит от площади поверхности осадка. Поэтому при титровании с адсорбционными индикаторами, в отличие от гравиметрических определений, стремятся получить осадок с как можно более мелкими частицами. Присутствие сильных электролитов, вызывающих коагуляцию коллоидных систем, затрудняет обнаружение конечной точки титрования.
