
- •Белки: строение, свойства и функции
- •1. Белки и их основные признаки
- •2. Биологические функции белков
- •3. Аминокислотный состав белков
- •4. Классификация белков
- •4.1. По растворимости
- •4.2. По форме молекул
- •5. Физические свойства белков
- •6. Структурная организация белковых молекул
- •6.1. Первичная структура белков
- •Пространственное расположение полипептидных цепей (Конформация пептидных цепей в белках)
- •6.2. Вторичная структура белков
- •6.3. Третичная структура белков
- •7. Способность к специфическим взаимодействиям как основа биологической активности белков
- •8. Ингибиторы функций белков
- •9.Связь структуры белков с их функциями на примере гемоглобина и миоглобина Четвертичная структура белка.
- •К инетика оксигенирования миоглобина и гемоглобина
- •Транспорт двуокиси углерода
- •Молекулярная основа эффекта Бора
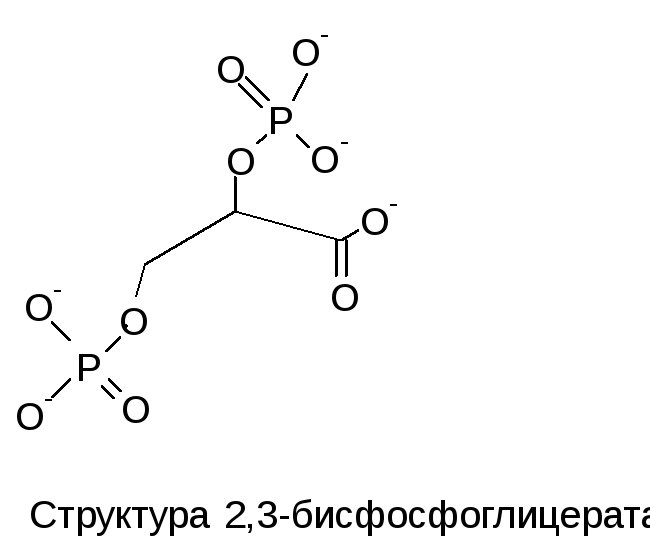
- •Регуляция 2,3-бисфосфоглицератом
- •10. Изофункциональные белки
- •11. Изменения белкового состава организма
Регуляция 2,3-бисфосфоглицератом
Недостаток О2 в тканях приводит к накоплению 2,3-бисфосфоглицерата. Это соединение образуется из 1,3-бисфосфоглицерата, промежуточного продукта гликолиза. Тетрамер гемоглобина связывает одну молекулу ДФГ, которая размещается в центральной области, выстланной остатками все 4-х субъединиц. Объем этой полости достаточен только в том случае, когда разрушены солевые мостики между тетрамерами. ДФГ стабилизирует неоксигенированную форму Hb. С фетальным гемоглобином ДФГ связывается менее прочно, поэтому HbF обладает большим сродством к О2, чем гемоглобин взрослого человека.
При увеличении концентрации ДФГ в эритроцитах (например, при снижении парциального давления кислорода), снижается сродство О2 к гемоглобину, этим и обуславливается регулирующее действие ДФГ.
Кооперативные изменения конформации олигомерных белков составляют основу механизма регуляции функциональной активности не только Hb, но и большого числа других белков, в том числе аллостерических ферментов.
10. Изофункциональные белки
Белок, выполняющий определенную функцию в клетке, может быть представлен несколькими формами - изофункциональными белками, или изоферментами. такие белки хоть и выполняют одинаковую функцию, но отличаются, константой связывания, что приводит к некоторым различиям в функциональном отношении. Например, в эритроцитах человека обнаружено несколько форм гемоглобина: HbA (96%), HbF (2%), HbA2(2%). Все гемоглобины представляют собой тетрамеры, построенные из протомеров , , , (HbA -22, HbF - 22, HbA2 - 22). Все протомеры сходны между собой по первичной структуре, и очень большое сходство наблюдается по вторичной и третичной структурам. Все формы гемоглобинов предназначены для переноса кислорода в клетки тканей, но HbF, например, имеет большее сродство к кислороду, чем HbA. HbF характерен для эмбриональной стадии развития человека. Он способен отнимать кислород у HbA, что обеспечивает нормальное снабжение кислородом плода.
Изобелки - это результат наличия более чем одного структурного гена в генофонде вида.
11. Изменения белкового состава организма
Белковый состав взрослого человека более или менее постоянен, однако возможны некоторые изменения содержания некоторых белков в зависимости от физиологической активности, состава пищи, циклические изменения (биоритмы). При болезнях белковый состав тканей изменяется. Эти проявления болезней называют протеинпатиями. Различают протеинпатии двух типов - наследственные и приобретенные. Наследственные - результат повреждения в генетическом аппарате организма (например, HbS). Приобретенные сопровождают любую болезнь. При приобретенных первичная структура белка не изменяется, изменяется количество белка и его распределение в тканях. Нарушение этих параметров в тканях и жидкостях организма позволяют поставить правильный диагноз.
