
- •Органическая химия
- •Оглавление
- •Введение
- •Общие методические указания по изучению учебной дисциплины
- •Унифицированные вопросы для самоконтроля
- •Методические указания по темам курса
- •Раздел 1.Основные теоретические положения органической химии.
- •Классификация органических соединений
- •Важнейшие классы органических соединений
- •Стабильность третичного иона карбония выше, т.К. Частичный положительный заряд на атоме углерода нейтрализуется индукционным эффектом наибольшего числа радикалов.
- •Раздел 2. Природные источники органических соединений и продукты их переработки
- •Раздел 3. Алифатические углеводороды ( алканы, алкены, алкадиены, алкины)
- •Раздел 4. Галогенпроизводные алифатического ряда
- •Раздел 5. Кислородсодержащие соединения алифатического ряда
- •Раздел 6. Азотсодержащие соединения алифатического ряда
- •Раздел 7.Серосодержащие органические соединения
- •Раздел 8. Соединения со смешанными функциями
- •Раздел 9. Карбоциклические соединения ( циклоалканы, циклоалкены, арены)
- •Раздел 10. Ароматические галогенпроизводные
- •Раздел 11. Кислородсодержащие соединения ароматического ряда
- •Раздел 12. Ароматические сульфокислоты
- •Раздел 13. Азотсодержащие соединения ароматического ряда
- •Раздел 14. Многоядерные ароматические соединения
- •Раздел 15. Гетероциклические соединения
- •Раздел 16. Высокомолекулярные соединения
- •Список рекомендуемой литературы
Раздел 8. Соединения со смешанными функциями
Если в молекуле углеводорода содержатся одновременно две (или более) различные функциональные группы, то такие соединения называют соединениями со смешанными функциями. К ним относятся гидроксикислоты, альдегидо- и кетокислоты, аминокислоты, углеводы и многие другие вещества, играющие важную в процессах , связанных с жизнедеятельностью живых организмов. Например, аминокислоты являются структурными единицами животных и растительных белков, а углеводы, входят в состав нуклеотидов, из которых построены нуклеиновые кислоты, осуществляющие биосинтез белка и передачу наследственных свойств. При изучении свойств соединений со смешанными функциями необходимо обратить внимание на взаимное влияние функциональных групп, строение и свойства моно-, ди- и полисахаридов, области применения.
Раздел 9. Карбоциклические соединения ( циклоалканы, циклоалкены, арены)
Алициклические соединения - это углеводороды, молекулы которых содержат один или несколько циклов (колец) неароматического характера. По своим свойствам они схожи с соответствующими соединениями алифатического ряда. Термин «алициклические» означает «алифатические циклические» углеводороды, но несмотря на большое сходство между алифатическими и алициклическими соединениями, имеются некоторые особенности в поведении последних, которые можно объяснить наличием в них циклической структуры.
Простейшими соединениями этого ряда являются:
I. Циклоалканы (циклопарафины)
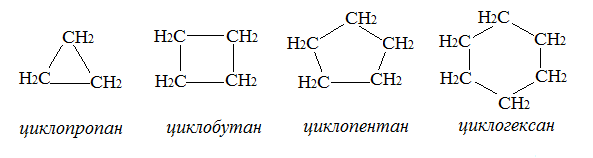
П. Циклоолефины, циклодиолефины, циклоацетилены и т.д.
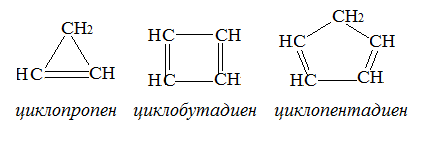
Алициклическим углеводородам соответствуют алициклические галогенопроизводные, спирты, карбонилсодержащие соединения, кислоты, амины и т.д. Между этими классами существуют взаимные переходы, аналогичные переходам между соединениями с открытой цепью.
Характер связи в циклопарафинах— насыщен, но, однако, малые, средние и высшие циклы ведут себя по разному в целом ряде реакций. Большие циклы, как и парафины, проявляют склонность к реакциям замещения. Малые циклы, подобно олефинам, вступают в реакции присоединения. Окисление и восстановление во всех случаях протекают с раскрытием цикла.
Экспериментальное определение угла в циклопропане показало, что оно составляет не 60°, а 106°, то есть отклонение от 109° 28/ очень мало. Это достигается образованием «банановых» связей, то есть перекрывание sр3 орбиталей происходит не вдоль прямой линии, а под некоторым углом к ней. «Банановая связь» менее прочная, чем σ - связь, но энергетический баланс молекулы выгоднее, чем при сильном искажении угла тетраэдра. Только в одном циклобутане, отклонение угла на 9,40 оказывается более энергетически выгодным, чем образование «банановых» связей.
Среди алициклических соединений широко распространено явление изомерии во всех её разновидностях, включая пространственные – геометрическую, оптическую, а также конформацион-
ную .
Ароматические углеводороды (арены) содержат в своей молекуле цикл, состоящий из шести атомов углерода, которые находятся в состоянии sp2 гибридизации (бензол). Электронная плотность π-связей распределена в кольце равномерно, т.е. все связи между атомами углерода равны по длине и прочности (эффект сопряжения). Ароматические соединения не дают реакций присоединения, характерных для этиленовых и ацетиленовых углеводородов. Для ароматических углеводородов наиболее характерны реакции замещения водорода в ароматическом кольце (реакция Фриделя -Крафтса, галогенирование, нитрование, сульфирование).
Положение, в которое вступает в ароматическое кольцо вторая группа, зависит от природы уже имеющегося в кольце заместителя (или ориентанта). Ориентанты I (-NH2, -NHR, - NR2, -Alк, Hal: -F, -Cl, -Br, -I) направляют вторую группу в орто- и пара-положения.
Ориентанты П рода
![]()
направляют вторую группу в мета-положение:
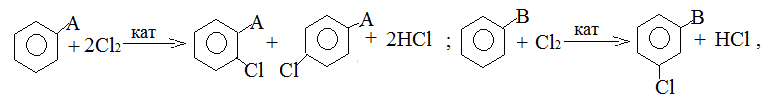
где А - ориентант I рода; В - ориентант П рода. Изучите механизм реакций замещения, образование π- и σ-комплексов, влияние ориентантов, их активирующее и дезактивирующее действие [1-4].
В реакции присоединения (по непредельным связям) они вступают труднее, чем олефины (гидрирование, озонирование, хлорирование). Также труднее протекает их окисление.
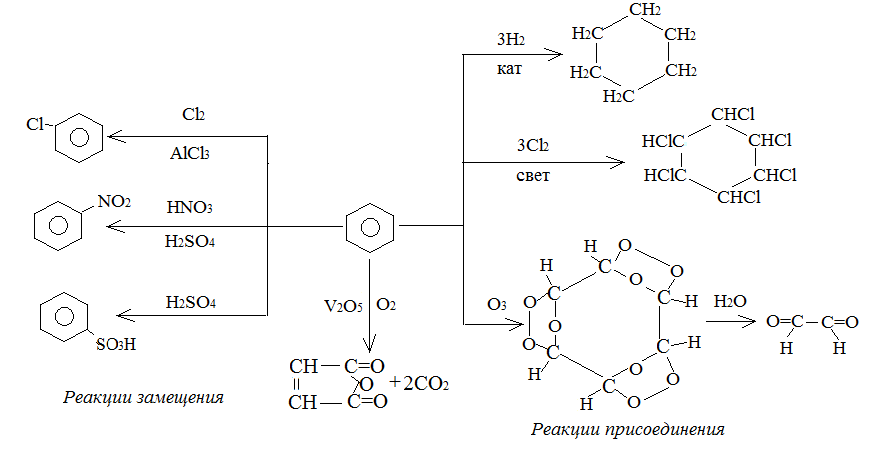
В промышленности ароматические углеводороды получают из продуктов коксования каменного угля и в результате ароматизации углеводородов нефти.
