
Лечение сахарного диабета 1 типа
.pdf30 |
Лечение сахарного диабета 1 типа |
Важным шагом в производстве препаратов инсулина стало получение инсулина человека.
В принципе, человеческий инсулин можно производить четырьмя способами:
1)полным химическим синтезом;
2)экстракцией из поджелудочных желез человека;
3)полусинтетическим;
4)биосинтетическим.
Первые 2 способа не используются из-за недостаточной разработанности первого способа и недостатка сырья (поджелудочных желез человека) для массового производства вторым способом.
Препараты инсулина человека, применяющиеся для лечения в настоящее время, получают либо полусинтетическим методом с помощью ферментнохимической замены В-30-аминокислоты аланина в свином инсулине на треонин, либо биосинтетическим способом по генноинженерной технологии.
Полусинтетический метод имеет лишь то преимущество, что для получения исходного вещества, то есть свиного инсулина, можно прибегнуть к давно и хорошо известным, усовершенствованным способам изготовления и очистки. Теоретически к "загрязнению" конечного продукта ведет попадание в него остатков ферментов или побочных продуктов полусинтеза, возникающих в процессе энзиматической замены одной аминокислоты на другие. Большинство развитых стран отказались от использования препаратов животного происхождения. Ведущие фирмы-производители инсулина сокращают производство свиного инсулина и полностью прекращают производство бычьих.
Для биосинтетического производства человеческого инсулина были предложены различные способы. Необходимый геномный материал переносят в микроогранизмы, которые начинают синтезировать предшественники инсулина. Чаще всего применяют один из двух следующих способов:
•раздельный синтез А- и В- цепи инсулина и последующее соединение двух цепей;
•синтез проинсулина или предшественников инсулина различного состава, из которых затем ферментным способом получают инсулин. В настоящее время все фирмы используют именно второй метод.
Современные технологии на фирмах Авентис, Эли Лилли, Ново-Нор- диск отличаются друг от друга, частично по патентно-правовым причинам. Эли Лилли – первая фирма, которая приступила к использованию генноинженерной технологии производства инсулина, с 1987 г. работает на челове-
Пособие для врачей |
31 |
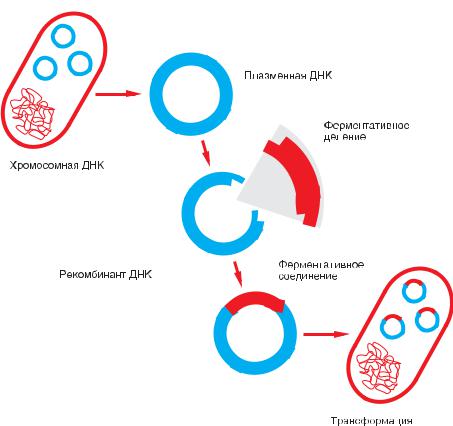
Рисунок 13. Введение генетической информации в E. Coli
ческом геноме. С его помощью бактерии кишечной палочки (E. coli) синтезируют проинсулин, который после ферментного отщепления С-пептида превращается в инсулин (рис. 13).
Фирма Ново-Нордиск применяет синтетически полученную ДНК для "ми- ни-проинсулина", то есть такого проинсулина, в котором С-пептид значительно короче, чем в проинсулине человека. Эту синтетическую ДНК вводят в
дрожжевые микроорганизмы, которые начинают синтезировать "мини-про- инсулин". На следующем этапе из него ферментным способом выделяют инсулин, по аминокислотной последовательности соответствующий человеческому. Сначала фирма Ново-Нордиск производила человеческий инсулин по-
32 |
Лечение сахарного диабета 1 типа |
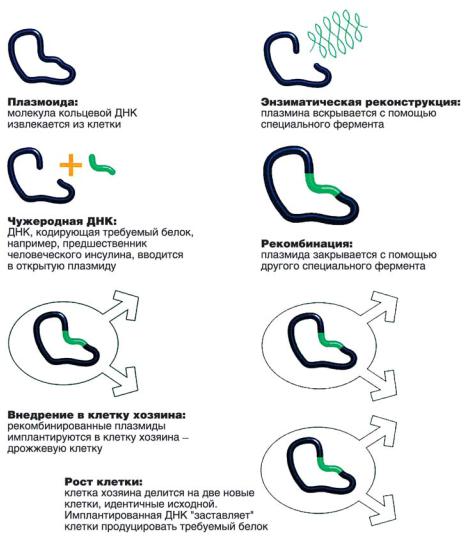
Рисунок 14. В 1981 г. компания Ново-Нордиск впервые в мире приступила к серийному выпуску человеческого инсулина. В 1985 г. с помощью метода генной инженерии второго поколения были "запрограммированы" пекарские дрожжи на естественную секрецию инсулина. Полученный инсулин НМ абсолютно идентичен инсулину, который синтезируется в человеческом организме.
Пособие для врачей |
33 |
лусинтетическим методом из свиного инсулина. Теперь человеческие инсулины Актрапид-НМ, Протафан-НМ и Актрафан-НМ (Ново) получают только биосинтетически (рис. 14).
Основной проблемой биосинтетического метода получения человеческого инсулина является абсолютное очищение конечного продукта от малейших примесей кишечной палочки или дрожжей, которые синтезировали инсулиновые цепочки. Был разработан новый метод контроля качества, на основании которого можно утверждать, что биосинтетически получаемый инсулин человека в настоящее время полностью свободен от каких-либо побочных примесей.
Таким образом, чистота современных препаратов инсулина человека, отвечает самым высоким требованиям. Каких-либо нежелательных побочных действий, зависящих от примесей, эти препараты инсулина не имеют.
Иммунологические исследования больных, которые либо с самого начала получали человеческий инсулин, либо были переведены на него в процессе лечения, показали, что при подкожном введении инсулина человека в организме образуются циркулирующие антитела к инсулину. Это явление, поначалу весьма удивившее медиков, связывают именно с тем, что препарат вводится подкожно, при этом происходит энзиматическое разрушение инсулина в месте инъекции. В любом случае, проявления и степень иммунной реакции при лечении человеческим инсулином весьма незначительны. Как при лечении впервые выявленных больных, так и при переводе с других препаратов инсулин человека выгодно отличается от инсулина животного происхождения. Важно отметить, что использование методов генной инженерии для получения препаратов инсулина человека позволило решить вопрос животного сырья, поскольку подсчитано, что 10 литров культуры E. coli производит столько же инсулина, сколько можно экстрагировать из поджелудочных желез миллионного стада свиней.
На сегодняшний день выпуск и применение инсулинов животного происхождения в развитых странах мира практически прекращены. Общественными разрешительными организациями и комитетами по биоэтике запрещены ксенотрансплантации, т. е. пересадка органов от животных к
человеку, равно как и приготовление лекарств из органов животных. Сейчас все больше накапливается фактов о том, что через субстанции из органов животных человеку передаются болезни, в частности вирусные. Поэтому препаратом выбора для больных диабетом, получающим инсулинотерапию, является рекомбинантный человеческий инсулин. Далее, говоря о человеческом инсулине, мы имеем в виду только рекомбинантный человеческий инсулин.

34 |
Лечение сахарного диабета 1 типа |
Вещества, добавляемые к инсулину
Добавки к инсулину вносят по следующим причинам:
•для удлинения действия инсулина;
•для дезинфекции;
•для кристаллизации и придания препарату буферных свойств.
Удлинение действия инсулина
Уже вскоре после введения инсулина в терапевтическую практику пробовали увеличить длительность его действия внесением различных добавок. Первые попытки, например с гуммиарабиком, лецитином, масляными суспензиями, холестерином, провалились. Лишь в 1936 г. Хагедорну удалось создать протамин-инсу- лин как вещество с щелочными свойствами. Протамин уменьшает растворимость инсулина при нейтральном pH. Инсулин продленного действия должен был помочь больным реже – по возможности, всего один раз в сутки – делать инъекции, чем это было при использовании только инсулина короткого действия.
Протамин как вещество, удлиняющее действие инсулина
Протамин – белок со щелочными свойствами, который получали из молок лососевых рыб во время нереста. Имеется всего несколько сообщений об аллергических реакциях на этот белок. Правда, считать протамин веществом, применение которого не составляет совсем никакой проблемы, нельзя. В отдельных редких случаях регулярное подкожное введение протамина (например, в составе НПХ-инсулина) может вызвать своего рода иммунизацию с образованием против него гуморальных антител типа IgE.
Протамин-цинк-инсулин (ПЦИ)
Первым препаратом инсулина продленного действия, стабильным в нейтральном растворе, был протамин-цинк-инсулин. Цинк, в небольшом количестве добавленный к протамин-инсулину, позволяет получить стабильный нейтральный препарат с длительностью действия до 72 часов. Его нельзя смешивать в одном шприце с инсулином короткого действия (который в этом случае связывается с избытком протамина). В настоящее время в России не выпускается.
НПХ – инсулин (НПХ – нейтральный протамин Хагедорна)
Этот инсулин (латинское обозначение – NPH) был создан в 1936 г. Хагедорном. В отличие от протамин-цинк-инсулина, НПХ-инсулин содержит инсулин и
Пособие для врачей |
35 |
протамин в изофанных, то есть в равных, количествах, при которых нет избытка ни инсулина, ни протамина (поэтому другое его название изофан-инсулин).
Чтобы при нейтральном pH протамин мог образовывать кристаллы инсулина, необходимо добавить небольшое количество цинка, фенола и/или крезола. Нейтральный pH препарата обеспечивается добавлением фосфатного буфера.
НПХ-инсулин можно стабильно смешивать с инсулином короткого действия. В соответствии с этим, существуют различные препараты, которые содержат смесь инсулина короткого действия и НПХ-инсулина. Постоянно создаются новые комбинации этих смесей в соотношениях от 10:90% до 50:50%; однако на самом деле нужными являются лишь очень немногие из них.
Не исключено, что для создания изофан-инсулина из инсулина различного происхождения необходимы неодинаковые пропорции инсулина и протамина. Так, при клиническом применении человеческого НПХ-инсулина была выявлена значительно меньшая продолжительность действия, чем при использовании свиного НПХ-инсулина.
Инсулин-цинк-суспензии
Первым препаратом, основанным на этом принципе замедления действия, был инсулин Ленте (Lente). Его разработка стала возможной после того, как было обнаружено, что добавление небольших количеств цинка при нейтральном pH удлиняет действие инсулина. Буферные свойства раствору придают не с помощью фосфатного (как в случае с протамин-инсулином), а с помощью других буферов, например, ацетатного.
Дезинфицирующие вещества и консерванты
В целом, добавлять дезинфицирующие вещества к инсулину необходимо. Дезинфицирующим действием обладают некоторые из субстанций, которые и без того необходимо вносить в препарат по фармако-технологическим соображениям. Так, например, в НПХ уже содержатся фенол и крезол. Оба вещества обладают неприятным запахом. Метилпарабен, напротив, не имеет никакого запаха. После того, как Актрапид-НМ и Протафан-НМ стали готовить с добавлением не метилпарабена, а крезола, никаких отличий между препаратами инсулина человека разных фирм не осталось.
Все дезинфицирующие вещества в тех концентрациях, в которых они присутствуют в препаратах инсулина, не оказывают на здоровье никакого вредного влияния. В инсулин-цинк-суспензии нельзя добавлять фенол, изменяющий физические свойства частиц инсулина, поэтому данные препараты содержат метилпарабен. Ионы цинка, содержащиеся в этих препаратах, оказывают также антимикробное действие.

36 |
Лечение сахарного диабета 1 типа |
Несмотря на многократное введение иглы во флакон с инсулином, такая многоступенчатая антибактериальная защита предотвращает осложнения, которые могли бы возникнуть из-за бактериального обсеменения.
Вещества, необходимые для кристаллизации и придания буферных свойств
Для перевода инсулина в кристаллическое состояние в инсулин-цинк-сус- пензии необходимо добавлять NaCI.
НПХ-инсулины содержат глицерин. В практическом отношении важно, что некоторые инсулины в качестве буферного вещества содержат фосфаты (например, инсулины фирмы Ново-Нордиск). Фосфатсодержащий инсулин никогда не смешивают с инсулин-цинк-суспензиями. Иначе выпадает осадок фосфата цинка, который непредсказуемым образом укорачивает продолжительность действия цинк-инсулина.
Концентрации инсулина
Первые препараты инсулина содержали лишь 1 единицу инсулина в миллилитре. Позже появились препараты с более высокой концентрацией.
Препараты инсулина, использующиеся в России содержат 40 единиц и (или) 100 единиц инсулина в миллилитре(U-40, U-100).
Вбольшинстве европейских стран применяется инсулин, содержащий 100 единиц в миллилитре (U-100). В Великобритании с 1983 г. имеется лишь U-100- инсулин; в 1988/1989 г. на такой инсулин полностью перешла и Швейцария.
Целесообразность перехода к U-100-инсулину у нас в стране диктуется тем, что часть больных стала пользоваться инъекторами инсулина ("шприцручками"), в которых применяются специальные патроны ("пенфиллы") с инсулином U-100.
Вразличных работах есть указания на то, что скорость всасывания подкожно введенного инсулина короткого действия в кровоток замедляется при повышении концентрации препарата. Однако похоже на то, что существенной разницы между U-40- и U-100-инсулином в этом отношении нет.
Препараты инсулина выпускаются в специальных флаконах, которые нельзя замораживать. Хранить их в течение длительного времени следует в холодильнике при температуре +2 - +8 °C. При поездках запас инсулина не следует класть в багаж, поскольку температура в багажной камере достигает минус 50 °С. Инсулин следует перевозить в ручной клади.

Пособие для врачей |
37 |
Флаконы, используемые больным в настоящее время, хранят при комнатной температуре. Инсулины, используемые в шприцах-ручках термостабильны и не теряют своих свойств при температуре до 37 °С. Срок годности препаратов инсулина обычно 2 года. Используемый в данный момент флакон инсулина может храниться при комнатной температуре в течение 30 дней.
Таблица препаратов инсулина, используемых в России
Инсулины |
Препараты |
Начало |
Пик |
Длительность |
|
|
действия |
действия, ч. |
действия, ч. |
|
|
|
|
|
Ультракорот- |
Хумалог |
через 15 мин. |
через 0,5-2 |
3-4 |
кого действия |
(ЛизПро) |
|
|
|
(аналоги |
Новорапид |
|
|
|
инсулина |
(Аспарт) |
|
|
|
человека) |
|
|
|
|
|
|
|
|
|
Короткого |
Актрапид НМ |
через 30 мин. |
через 1-3 |
6-8 |
действия |
Хумулин R |
|
|
|
|
Инсуман рапид |
|
|
|
|
|
|
|
|
Средней |
Монотард НМ |
через 2,5 ч. |
через 7-15 |
24 |
продолжи- |
Протафан НМ |
через 1,5 ч. |
через 4-12 |
24 |
тельности |
Хумулин НПХ |
через 1 ч. |
через 2-8 |
18-20 |
действия |
Инсуман базаль |
через 1 ч. |
через 3-4 |
11-20 |
|
|
|
|
|
Длительного |
Ультратард НМ через 4 ч. |
через 8-24 |
28 |
|
действия |
|
|
|
|
|
|
|
|
|
Препараты инсулина различной длительности действия
Многочисленные препарата инсулина различаются по длительности действия, степени очистки, источнику получения, концентрации, величине pН.
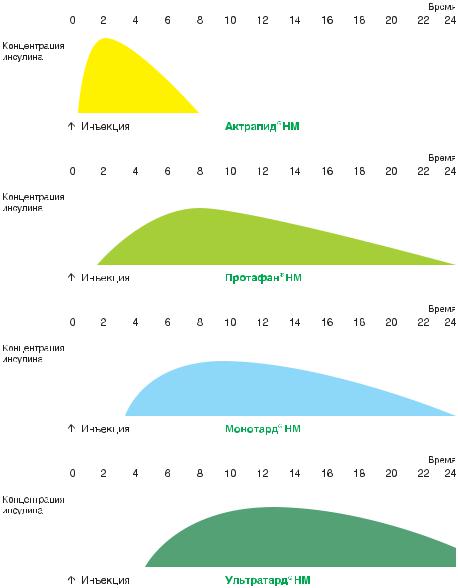
Препараты инсулина могут быть короткого действия, средней продолжительности и длительного действия (рис. 15). Начало действия препаратов первой группы через 15-25 минут после введения, пик – через 2-3 часа, продолжительность действия обычно не превышает 6 часов. К препаратам короткого действия относятся Актрапид и НМ (человеческий) (Ново-Нор-
38 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Лечение сахарного диабета 1 типа |
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Рисунок 15. Длительность действия инсулинов

Пособие для врачей |
39 |
диск), Хумулин R и S (Лилли), Инсуман рапид фирмы Авентис и другие. Препараты короткого действия – прозрачные, большинство препаратов
пролонгированного действия – мутные (суспензии).
Начало действия препаратов средней продолжительности через 2-4 часа после введения, максимум действия через 6-8 часов, продолжительность, как правило, 12-14 часов. К препаратам данной группы относятся Монотард НМ (Ново-Нордиск), Протафан НМ (Ново-Нордиск), Хумулин N (Лилли), Инсуман Базаль-Н (Авентис). Ранее к этой группе относили инсулин Семиленте и Семилонг, однако их истинная продолжительность действия слишком коротка – менее 10 часов. Они сняты с производства.
К препаратам длительного действия относятся Ультратард НМ (НовоНордиск), Хумулин ультраленте (Лилли). Начало их действия через 4-5 часов после введения, продолжительность 24-36 часов Так как разные фирмы применяют различные консерванты и другие обязательные компоненты в препаратах инсулина, рекомендуется одновременно использовать препараты короткого и длительного действия одной и той же фирмы.
СТРАТЕГИЯ ИНСУЛИНОТЕРАПИИ
Как уже было сказано выше, инсулин выделяется β-клетками как в голодном состоянии, так и по требованию, после приема пищи в количествах, зависящих от ее состава. У здорового человека секреция инсулина может быть измерена с помощью определения С-пептида, поскольку он выделяется β-клеткой эквимолярно к инсулину и не задерживается печенью. У здорового человека в сутки вырабатывается от 23 до 60 ед инсулина, что составляет от 0,6 до 1,0 Ед/кг массы тела. Эта секреция подразделяется на базальную (базисную) и пищевую (болюсную). Базисная секреция инсулина рассчитывается в пределах приблизительно до 1,0 ед/час, что составляет 24 ед в сутки. Стимулированная пищей секреция инсулина составляет от 1,0 до 1,5 ед инсулина на каждые 10-12 г углеводов (1ХЕ). Известно также, что потребность в инсулине выше утром и чувствительность к нему возрастает в вечернее время. Все эти моменты имеют существенное значение для врача, поскольку задача современной инсулинотерапии заключается в том, чтобы имитировать с помощью препаратов инсулина разной длительности собственную секрецию инсулина. Этот вид инсулинотерапии получил название базис-болюсного принципа инсулинотерапии. Он поло-
