- •Министерство образования и науки Российской Федерации
- •Термохимия. Закон Гесса
- •Зависимость теплового эффекта химической реакции от температуры
- •Вычисление изменения энергии Гиббса химической реакции по значениям стандартных энтальпий и энтропий
- •Фазовые равновесия. Уравнение Клапейрона-Клаузиуса
- •Химическое равновесие
- •Термодинамика растворов
- •Электропроводность электролитов
- •Электродвижущие силы и электродные потенциалы
- •II. Коллоидная химия Молекулярно-кинетические свойства коллоидных систем
- •Оптические свойства коллоидных систем
- •Поверхностные явления в коллоидных системах
- •Адсорбция
- •Седиментационная устойчивость коллоидных систем
- •Мицеллообразование
- •Агрегативная устойчивость коллоидных систем. Кинетика коагуляции Примеры решения типовых задач
- •Контрольные задания Вариант 1
- •Вопросы
- •Вариант 2
- •Вопросы
- •Вариант 3
- •Вопросы
- •Вариант 4
- •Вопросы
- •Вариант 5
- •Вопросы
- •Вариант 6
- •Вопросы
- •Вариант 7
- •Вопросы
- •Вариант 8
- •Вопросы
- •Вариант 9
- •Вопросы
- •Вариант 10
- •Вопросы
- •Вариант 11
- •Вопросы
- •Вариант 12
- •Вопросы
- •Вариант 13
- •Вопросы
- •Вариант 14
- •Вопросы
- •Вариант 15
- •Вопросы
- •Стандартные изменения энергии Гиббса образования веществ
- •Поверхностное натяжение воды на границе с воздухом
Контрольные задания Вариант 1
1. 63 г азота находятся при н.у. Определить количествотеплоты, работу, изменение энтальпии и внутренней энергии при изобарном расширении до объема 0,2 м3.
2. Вычислить тепловые эффекты химических реакций при стандартных условиях по стандартнымтеплотам образования (пользуясь данными приложения).
СН4(г) + 2H2S(г) = CS2(г) + 4Н2(г)
3. Вычислить стандартное изменение энергии Гиббса при 250С для реакции
HBr(г)= ½Br2(г)+ ½ Н2(г)
по стандартным значениям энтальпий образования и абсолютных энтропий химических соединений.
4. Определить величину приращения температуры плавления при изменении давления на 1 Па для алюминия, если его температура плавления составляет 660,1С, изменение объема 1,51 см3/моль, мольная теплота плавления равна 10,878 кДж/моль.
5. Выразить концентрацию водного раствора через молярность, нормальность, моляльность и мольные доли.
|
Растворенное вещество |
Заданная концентрация, (мас.) |
Плотность раствора, г/мл |
Объем раствора, л |
|
AgNO3 |
50 |
1,668 |
1 |
6. Вычислить абсолютные скорости движения анионов и катионов в растворе электролита по следующим данным:
|
Электролит |
t+ |
,
|
|
HNO3 |
0,842 |
364,6 |
7.
Рассчитать
ЭДС цепи, состоящей из кобальтового и
водородного электродов. Давление
водорода 0,3 МПа, активность ионов кобальта
1 моль/л, рН равен 1. Стандартный электродный
потенциал кобальта
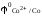 равен –0,277 В. Температура 25С.
равен –0,277 В. Температура 25С.
8. Вычислить величину осмотического давления в гидрозоле золота с массовой концентрацией 2 кг на единицу объема, плотностью 19,3 г/см3 и диаметром частиц 6 109 м при 250С.
9. Рассчитать скорость оседания в гравитационном поле капель водяного тумана с радиусом частиц 106 м и время, за которое капли, находящиеся в 2 м от земли осядут. Плотность воды 1 г/см3, вязкость среды 1,8 105 Пас. Плотностью среды пренебречь.
10. Вычислить удельную поверхность единицы объема и единицы массы угольной пыли с диаметром частиц 6 10-5 м и плотностью 1,8 г/см3.
11. Рассчитать константы в уравнении БЭТ и удельную поверхность катализатора, если адсорбция криптона при 77,5 К характеризуется следующими данными:
|
Р, Па |
19,86 |
26,66 |
41,05 |
65,44 |
|
V, см3 |
0,2762 |
0,3040 |
0,3523 |
0,4097 |
Площадь, занимаемая одной молекулой криптона 19,2 10-20 м2, плотность криптона 3,739 10-3 г/см3, давление насыщенного пара криптона 342,55 Па.
12. Золь йодида свинца PbI2получен смешением 49,8 г раствора йодида калия и 132,4 г раствора нитрата свинца. Написать формулу мицеллы золя и указать знак электрического заряда коллоидной частицы.
Вопросы
1. Дать несколько формулировок I закона термодинамики.
2. Какие процессы называются равновесными?
3. Значение коллоидной химии. Дисперсные системы в промышленности.
Вариант 2
1. 63 г азота находятся при н.у. Определить количествотеплоты, работу, изменение энтальпии и внутренней энергии при изохорном нагревании до достижения давления 2,026105 Па.
2. Вычислить тепловые эффекты химических реакций при стандартных условиях по стандартнымтеплотам образования (пользуясь данными приложения).
4СО(г)+ 2SO2(г)=S2(г)+ 4СО2(г)
3. Вычислить стандартное изменение энергии Гиббса при 250С для реакции
HС1(г)= ½ С12(г)+ ½ Н2(г)
по стандартным значениям энтальпий образования и абсолютных энтропий химических соединений.
4. Определить величину приращения температуры плавления при изменении давления на 1 Па для фосфинаPH3, если его температура плавления составляет –134,74С, изменение объема 2,25см3/моль, мольная теплота плавления равна 1,130 кДж/моль.
5. При 25С давление паров воды равно 32,3 гПа. Чему равно давление паров воды над раствором, содержащем 6 г мочевины в 180 г воды?
6. Удельная электропроводность 1 л 12%-го раствора хлорида алюминия равна 0,1041 Ом–1см–1, а его плотность 1,109 г/см3. Предельная подвижность иона Al3+ равна 63 см2/(Оммоль-экв), хлорид-иона 76,35 см2/(Оммоль-экв). Вычислить эквивалентную электропроводность и кажущуюся степень диссоциации.
7.
Стандартный электродный потенциал
медного электрода
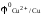 равен
0,337 В, стандартный электродный потенциал
никелевого электрода
равен
0,337 В, стандартный электродный потенциал
никелевого электрода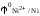 равен –0,250 В. Записать электрохимический
элемент, константу равновесия, ЭДС
элемента, убыль изобарно-изотермического
потенциала при 25С.
Активность ионов никеля 0,2 моль/л, ионов
меди 0,1 моль/л.
равен –0,250 В. Записать электрохимический
элемент, константу равновесия, ЭДС
элемента, убыль изобарно-изотермического
потенциала при 25С.
Активность ионов никеля 0,2 моль/л, ионов
меди 0,1 моль/л.
8. Вычислить коэффициент диффузии частиц в золе сульфида мышьяка As2S3, если радиус частиц 2 10-8 м, вязкость среды 10-3 Пас, температура 250С.
9. Определить число частиц, образовавшихся при раздроблении 1,15 г золота на правильные кубики с длиной ребра 2 10-9 м и плотностью 19,32 103 кг/м3.
10. Пользуясь экспериментальными данными спектрофотометрических измерений, подтвердить графически применимость закона Ламберта – Бера к гидрозолю конго красного и определить концентрацию при D= 0,25; 0,45 и 0,65.
|
Концентрация золя, С 102, кг/м3 |
1 |
3 |
5 |
7 |
9 |
11 |
|
Оптическая плотность D |
0,065 |
0,22 |
0,37 |
0,53 |
0,69 |
0,85 |
11. Написать формулы мицелл золей и указать знак электрического заряда коллоидной частицы:
а) SiO2 стабилизированного H2SiO3;
б) Au стабилизированного KAuO2.
12. Во сколько раз изменится величина порога коагуляции, если для коагуляции 105 м3 золя AgI вместо 1,5 103 л KNO3 концентрации 1 моль/л взять 4 104 л Ca(NO3)2 концентрации 0,1 моль/л.