- •Министерство образования и науки Российской Федерации
- •Термохимия. Закон Гесса
- •Зависимость теплового эффекта химической реакции от температуры
- •Вычисление изменения энергии Гиббса химической реакции по значениям стандартных энтальпий и энтропий
- •Фазовые равновесия. Уравнение Клапейрона-Клаузиуса
- •Химическое равновесие
- •Термодинамика растворов
- •Электропроводность электролитов
- •Электродвижущие силы и электродные потенциалы
- •II. Коллоидная химия Молекулярно-кинетические свойства коллоидных систем
- •Оптические свойства коллоидных систем
- •Поверхностные явления в коллоидных системах
- •Адсорбция
- •Седиментационная устойчивость коллоидных систем
- •Мицеллообразование
- •Агрегативная устойчивость коллоидных систем. Кинетика коагуляции Примеры решения типовых задач
- •Контрольные задания Вариант 1
- •Вопросы
- •Вариант 2
- •Вопросы
- •Вариант 3
- •Вопросы
- •Вариант 4
- •Вопросы
- •Вариант 5
- •Вопросы
- •Вариант 6
- •Вопросы
- •Вариант 7
- •Вопросы
- •Вариант 8
- •Вопросы
- •Вариант 9
- •Вопросы
- •Вариант 10
- •Вопросы
- •Вариант 11
- •Вопросы
- •Вариант 12
- •Вопросы
- •Вариант 13
- •Вопросы
- •Вариант 14
- •Вопросы
- •Вариант 15
- •Вопросы
- •Стандартные изменения энергии Гиббса образования веществ
- •Поверхностное натяжение воды на границе с воздухом
Адсорбция
Примеры решения типовых задач
Задача 1. Найти величину адсорбции органической кислоты на поверхности раздела водный раствор/воздух, степень заполнения поверхности и удельную поверхность адсорбента при 17 0С и концентрации 0,7 103 моль/м3 по константам уравнения Шишковскогоа = 12,5 10-3 и b = 7,73 10-3. Площадь, занимаемую одной молекулой кислоты принять равной 15,85 10-19 м2.
Р е ш е н и е. Величину адсорбции найдем по уравнению изотермы Ленгмюра. Для этого определим величину Г с учетом того, что Т = 17 0С = 290 К:
Г
=
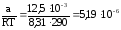 моль/м2.
моль/м2.
Рассчитываем величину адсорбции
Г
=
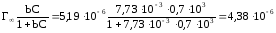 моль/м2.
моль/м2.
Степень заполнения вычисляют по формуле:
=
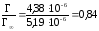 .
.
Удельную поверхность адсорбента находят с помощью выражения:
Sуд = ГNAS0= 5,19 106 6,02 1023 15,85 1019 = 4,95 м2.
Задача 2.Определить константы уравнения Ленгмюра и адсорбцию СО2 на слюде, а также степень заполнения при Р =8 Па, если при Т =155 К получены следующие результаты:
|
Р, Па |
0,48 |
1,19 |
2,06 |
9,8 |
|
Г, моль/см2 |
1,22 1010 |
1,95 1010 |
2,55 1010 |
3,62 1010 |
Р
е ш е н и е.
Согласно уравнению Ленгмюра,
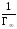 является
угловым коэффициентом прямой зависимости
между
является
угловым коэффициентом прямой зависимости
между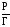 и
Р и, следовательно,
Г =ctg,
где
- угол наклона прямой. Вычисляем величины
и
Р и, следовательно,
Г =ctg,
где
- угол наклона прямой. Вычисляем величины
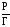 :
:
|
Р, Па |
0,48 |
1,19 |
2,06 |
9,8 |
|
|
0,39 1010 |
0,61 1010 |
0,81 1010 |
2,7 1010 |
По полученным данным строим график,
отложив на оси абсцисс Р, а на оси ординат
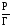 .
Как видно из графика,
Г =ctg=
.
Как видно из графика,
Г =ctg=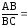
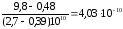 моль/см2.
моль/см2.
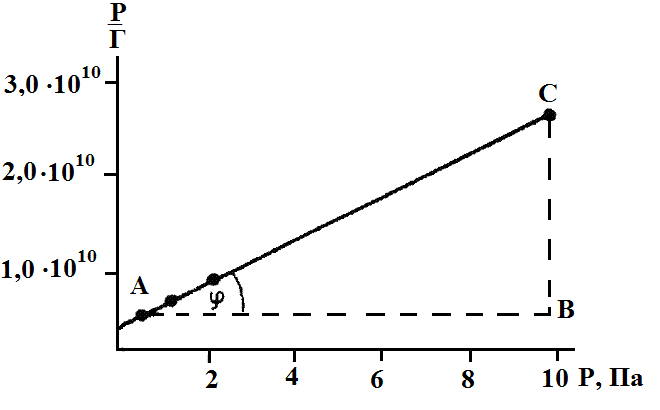
Зависимость
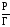 от Р.
от Р.
Отрезок,
отсекаемый на оси ординат, равен
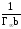 = 0,25
1010,
откуда
= 0,25
1010,
откуда
b=
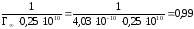 .
.
Вычислим величину Г при 8 Па по уравнению:
Г
=
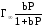 = 4,03
1010
= 4,03
1010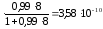 моль/см2.
моль/см2.
Степень заполнения поверхности определяем по формуле:
=
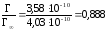 .
.
Задача 3. Найти константы уравнения Фрейндлиха, если при адсорбции уксусной кислоты на активированном угле получены следующие данные
|
С, моль/л |
0,0024 |
0,0073 |
0,0204 |
|
Г, моль/г |
2,9 104 |
4,6 104 |
8,5 104 |
Р е ш е н и е. Воспользуемся уравнением изотермы адсорбции Г = kС. Константы уравнения Фрейндлиха определяются графически после логарифмирования. Находим логарифмы концентрации кислоты и величин Г:
|
lgC |
2,62 |
2,14 |
1,69 |
|
lgГ |
3,54 |
3,34 |
3,07 |
Зависимость lgГlgC показана на рис. ниже
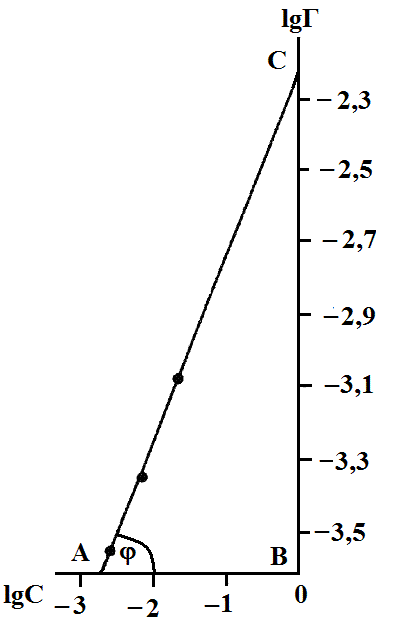
Зависимость lgГlgC.
Согласно графику, lgk = 2,22, следовательно, k = 102,22 = 6,02 103.
tg
=
 =
=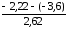 = 0,52, следовательно,
= 0,52.
= 0,52, следовательно,
= 0,52.
Задача 4. При адсорбции криптона на серебре при 77,5 К получены следующие результаты:
|
Р, мм.рт.ст. |
0,0992 |
0,1800 |
0,3686 |
0,5680 |
0,6843 |
|
V, см3/г |
0,0127 |
0,0150 |
0,0176 |
0,0190 |
0,0198 |
Рассчитать константы уравнения БЭТ Vmи с,удельную поверхность катализатора Syд,приняв площадь, занимаемую одной молекулой криптона, равной 19,5 1020 м2, плотность криптона при 0° С 3,739 103 г/см3, давление насыщенного пара криптона 2,57 мм.рт. ст.
Р
е ш е н и е.Согласно
уравнению изотермы адсорбции БЭТ,
прямолинейная зависимость получается
в координатах
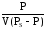
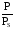 .
.
|
|
0,0385 |
0,0700 |
0,1430 |
0,2200 |
0,2660 |
|
|
3,16 |
5,02 |
9,50 |
14,93 |
18,33 |
На основании полученных данных строим график. Из графика находим тангенс угла наклона прямой:
tg
=
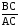 =
=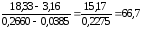 . (а)
. (а)
Отрезок,
отсекаемый на оси ординат, равен
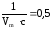 . (б)
. (б)
Решая совместно уравнения (а) и (б), получаем значения с = 134,4 и Vm = 0,0149 см3/г.
Для пересчета Vm на Г воспользуемся формулой:
Г
=
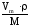 =
=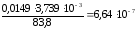 моль/г.
моль/г.
Удельную поверхность катализатора рассчитывают по уравнению:
Sуд = ГNAS0 = 6,64 107 6,02 102319,5 1020 = 0,078 м2
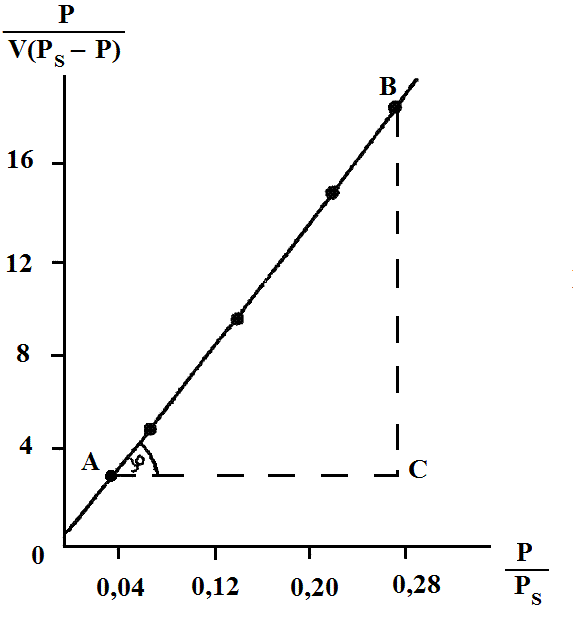
Зависимость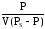 от
от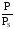 .
.