
- •Министерство образования и науки Российской Федерации
- •Термохимия. Закон Гесса
- •Зависимость теплового эффекта химической реакции от температуры
- •Вычисление изменения энергии Гиббса химической реакции по значениям стандартных энтальпий и энтропий
- •Фазовые равновесия. Уравнение Клапейрона-Клаузиуса
- •Химическое равновесие
- •Термодинамика растворов
- •Электропроводность электролитов
- •Электродвижущие силы и электродные потенциалы
- •II. Коллоидная химия Молекулярно-кинетические свойства коллоидных систем
- •Оптические свойства коллоидных систем
- •Поверхностные явления в коллоидных системах
- •Адсорбция
- •Седиментационная устойчивость коллоидных систем
- •Мицеллообразование
- •Агрегативная устойчивость коллоидных систем. Кинетика коагуляции Примеры решения типовых задач
- •Контрольные задания Вариант 1
- •Вопросы
- •Вариант 2
- •Вопросы
- •Вариант 3
- •Вопросы
- •Вариант 4
- •Вопросы
- •Вариант 5
- •Вопросы
- •Вариант 6
- •Вопросы
- •Вариант 7
- •Вопросы
- •Вариант 8
- •Вопросы
- •Вариант 9
- •Вопросы
- •Вариант 10
- •Вопросы
- •Вариант 11
- •Вопросы
- •Вариант 12
- •Вопросы
- •Вариант 13
- •Вопросы
- •Вариант 14
- •Вопросы
- •Вариант 15
- •Вопросы
- •Стандартные изменения энергии Гиббса образования веществ
- •Поверхностное натяжение воды на границе с воздухом
Вариант 15
1. При 27 С и давлении 1013000 Па 8 г кислорода расширяются адиабатно до давления 101300 Па. Вычислить конечную температуру и работу, совершенную кислородом.
2. Рассчитать тепловые эффекты реакции:
2СО + SO2 = 0,5S2(г) + 2СО2 при температурах 335 К и 486 К и найти их отношение.
Тепловой эффект реакции при стандартных условиях равен: 204,88 кДж.
Теплоемкости при этих условиях равны:
Ср(СО) = 29,14 Дж/(мольК); Ср(SO2) = 39,87 Дж/(мольК);
Ср(S2(г)) = 32,51 Дж/(мольК); Ср(СО2) = 37,11 Дж/(мольК).
3. Вычислить стандартное изменение энергии Гиббса при 250С для реакции
NO2(г) = O2(г) + ½ N2(г)
по стандартным значениям энтальпий образования и абсолютных энтропий химических соединений.
4. Давление диссоциации MgCO3 при 813 К равно 0,996 105 Па, а при 843 К равно 1,786 105 Па. Вычислить тепловой эффект реакции разложения магнезита
MgCO3(т) MgO(т) + СО2(г)
и рассчитать, при какой температуре давление диссоциации будет равно 1,013 105 Па.
5. Выразить концентрацию водного раствора через молярность, нормальность, моляльность и мольные доли.
|
Растворенное вещество |
Заданная концентрация, (мас.) |
Плотность раствора, г/мл |
Объем раствора, л |
|
CuSO4 |
8 |
1,084 |
1 |
6. При 18°С удельная электропроводность чистой воды равна 3,84·10-8Ом-1·см-1. Подвижности ионов Н+ и ОН– соответственно равны 315 и 174 Ом-1·моль-экв-1·см2. Вычислить степень диссоциации и константу диссоциации воды.
7.
Стандартные электродные потенциалы
медного и серебряного электродов равны
соответственно 0,337
В и 0,779 В. Записать электрохимический
элемент, в котором протекает реакция
Cu
+ 2Ag+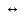 Cu2+
+ 2Ag,
определить ее направление, рассчитать
константу равновесия, ЭДС и изменение
изобарно-изотермического потенциала
при 25
С, если активность ионов серебра равна
0,1моль/л, ионов меди 0,2 моль/л.
Cu2+
+ 2Ag,
определить ее направление, рассчитать
константу равновесия, ЭДС и изменение
изобарно-изотермического потенциала
при 25
С, если активность ионов серебра равна
0,1моль/л, ионов меди 0,2 моль/л.
8. Рассчитать скорость оседания в гравитационном поле капель аэрозоля NH4Cl с радиусом частиц 5 107 м и время, за которое капли, находящиеся в 2 м от земли осядут. Плотность NH4Cl 1,5 г/см3, вязкость среды 1,76 105 Пас. Плотностью среды пренебречь.
9. Найти площадь, занимаемую одной молекулой пальмитиновой кислоты С15Н31СООН на единице поверхности водного раствора и толщину адсорбционного слоя, если величина предельной адсорбции составляет 7,9 106 моль/м2, а плотность кислоты равна 0,85 103 кг/м3.
10. Рассчитать константы в уравнении БЭТ и удельную поверхность катализатора, если адсорбция криптона при 77,5 К характеризуется следующими данными:
|
Р, мм рт.ст. |
0,149 |
0,200 |
0,308 |
0,491 |
|
V, см3/г |
0,2763 |
0,3040 |
0,3524 |
0,4098 |
Площадь, занимаемая одной молекулой криптона 19,2 10-20 м2, плотность криптона 3,739 10-3 г/см3, давление насыщенного пара криптона 2,57 мм рт. ст.
11. С помощью нефелометра определили, что мутность гидрозоля мастики в 8,3 раз больше мутности стандартного золя. Средний диаметр частиц стандартного золя 2 нм. Определить радиус частиц гидрозоля мастики, если концентрации золей одинаковы.
12. Написать формулы мицелл золей и указать знак электрического заряда коллоидной частицы:
а) BaSO4 стабилизированного K2SO4;
б) BaSO4 стабилизированного Ba(CH3COO)2.
