
практикум по кмвед
.pdf
микроскоп этот рельеф будет создавать сочетание света и тени (рис. 4.2). Свет будет больше рассеиваться теми участками, которые сильнее протравились. Такие участки будут выглядеть более тёмными. При травлении полированная поверхность протирается со слабым нажимом ватным тампоном, смоченным травителем, либо раствор наносится на поверхность шлифа тонким слоем и выдерживается до тех пор, пока поверхность не станет матовой. После этого микрошлиф тщательно промывается проточной водой, спиртом и сушится фильтровальной бумагой.
4.2. Порядок выполнения работы
1. Ознакомиться с устройством микроскопов МИМ-7 и ЕС МЕТАМ РВ-22. 2. Приготовить микрошлиф для исследования структуры.
3. Изучить и зарисовать исследуемую микроструктуру.
4.3. Содержание отчёта
1.Описание цели работы.
2.Схема металлографического микроскопа.
3.Схема микроструктуры образца
4.Описание микроструктуры исследуемого образца.
4.4. Контрольные вопросы
1.Каков порядок приготовления микрошлифа?
2.Для чего проводится травление?
3.От чего зависит выбор травителя?
4.Как определяется увеличение микроскопа?
5.Чем отличается шлифование от полирования?
6.Что называется микроанализом?
7.Почему при травлении структура образца протравливается неодина-
ково?
Рекомендуемая литература [1–3, 6, 19].
31
5. ИЗУЧЕНИЕ ПРОЦЕССА ПЕРВИЧНОЙ КРИСТАЛЛИЗАЦИИ
Цель работы: изучить процесс формирования кристаллов при переходе вещества из жидкого состояния в твёрдое.
Приборы и оборудование: водный раствор хлористого аммония, микроскоп типа МБС-9, предметное стекло, фрагменты слитка сурьмы с продольным и поперечным изломами.
5.1. Краткие теоретические сведения
Кристаллизацией называется переход металла при определенной температуре из жидкого состояния в твёрдое. Рассмотрим энергетические условия этого процесса.
Энергетическое состояние любой системы характеризуется определенным запасом внутренней энергии. Та часть энергии, которая в изотермических условиях может быть превращена в работу, называется свободной: Е = U – T S, где U – полная внутренняя энергия системы; Т – температура; S – энтропия. Чем меньше свободная энергия системы, тем она более устойчива.
Согласно второму закону термодинамики, всякая система стремится к более устойчивому состоянию, т. е. к минимальному значению свободной энергии. Любой самопроизвольно текущий процесс идет только в том случае, если новое состояние более устойчиво. Переход вещества в жидкое состояние и наоборот также подчиняется этому закону: если меньшей свободной энергией обладает твёрдое тело, то идет процесс кристаллизации и, наоборот, при меньшей свободной энергии жидкого состояния – плавление.
Зависимость изменения свободной энергии металла в жидком и твёрдом состояниях от температуры приведена на рис. 5.1. С увеличением температуры величина свободной энергии как жидкой, так и твёрдой фаз уменьшается, но законы изменения различны.
При температуре Тs свободная энергия твёрдой и жидкой фаз равны, что даёт возможность их одновременного существования. Такая температура называется равновесной. Чтобы начался процесс кристаллизации необходима разность свободных энергий Е1 твёрдой и жидкой фаз. В соответствии с этим температура Ткр соответствует температуре кристаллиза-
32
ции. Разность по абсолютной величине между равновесной и температурой кристаллизации называется степенью переохлаждения: Т1 = | Тs – Ткр |. Чем больше степень переохлаждения Т, тем больше разность свободных энергий Е1 , тем интенсивней будет идти процесс кристаллизации.
|
Е |
|
|
|
|
жидкое состояние |
|
||
энергия |
E1 |
|
|
|
|
|
|
твердое состояние |
|
Свободная |
E2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
Т1 |
|
Т2 |
|
|
Ткр |
Ts |
Тпл |
T, о С |
Рис. 5.1. Схема изменения свободной энергии жидкой и твердой фаз металла в зависимости от температуры
Для развития процесса плавления необходима разность свободных энергий Е2, которая возникает при некоторой степени перегрева:
Т2 = | Тs – Тпл |, где Тпл – температура плавления.
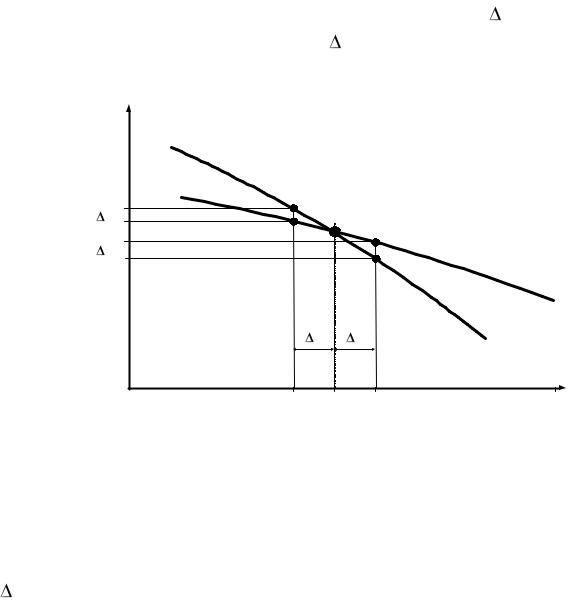
Впервые глубокие исследования процесса кристаллизации были проведены русским инженером-металлургом Д.К. Черновым. Он показал, что процесс кристаллизации складывается из двух этапов: образования центров и роста кристаллов из этих центров. Скорость процесса кристаллизации количественно характеризуется скоростью зарождения центров и скоростью роста кристаллов. Число зарождающихся в единицу времени центров (Ч.Ц.) имеет размерность 1/мм3 (число центров, возникающих в 1 мм3 объёма металла за секунду). Скорость роста кристаллов (С.Р.) – это увеличение линейных размеров кристалла в единицу времени (м/ч). Зависимость числа центров кристаллизации и скорости роста кристаллов от степени переохлаждения приведены на рис. 5.2.
33
При равновесной температуре ( Т = 0) |
значения С.Р. и Ч.Ц. равны |
||||||||
нулю. Поэтому процесс кристаллизации идти не может. При увеличении |
|||||||||
степени переохлаждения увеличивается разность свободных энергий |
|||||||||
твёрдой и жидкой фаз, что ведет к увеличению Ч.Ц. и С.Р. Если жидкость |
|||||||||
переохладить до температуры, соответствующей точке «а», то образуются |
|||||||||
|
|
|
крупные зёрна (рис. 5.2), так |
||||||
|
|
|
как С.Р. будет большая при |
||||||
|
а |
|
малом значении Ч.Ц., а при |
||||||
|
|
малых |
значениях |
С.Р. |
и |
||||
|
|
|
|||||||
. |
в |
c |
больших Ч.Ц. (точка «в») |
||||||
Ч.Ц |
С.Р. |
||||||||
|
образуется |
большое |
число |
||||||
Р. , |
|
Ч.Ц. |
мелких кристаллов. |
|
|
|
|||
С. |
|
|
Если очень сильно пе- |
||||||
|
|
|
|||||||
|
|
|
реохладить |
жидкость, |
то |
||||
|
|
Т |
образование |
кристаллитов |
|||||
|
|
не происходит, так как при |
|||||||
|
|
|
|||||||
Рис. 5.2 Влияние степени переохлаждения на |
низких |
температурах |
под- |
||||||
число |
центров кристаллизации |
и скорость |
|||||||
вижность атомов (диффузия) |
|||||||||
роста кристаллов |
|
||||||||
|
уменьшается, и они из хао- |
||||||||
|
|
|
|||||||
тичного расположения в жидкости не успевают образовывать кристалли- |
|||||||||
ческие решётки. Следовательно, в этом случае образуется аморфное тело. |
|||||||||
У металлов и сплавов тоже возможно аморфное состояние, если ско- |
|||||||||
рости охлаждения будут в пределах 106…1010 оС/с. Такие сплавы называют |
|||||||||
«металлическими стёклами». Они обладают высокой твёрдостью, пла- |
|||||||||
стичностью, прочностью. При больших толщинах аморфные сплавы по- |
|||||||||
лучить не удаётся, так как решающую роль начинает играть теплоотвод из |
|||||||||
средних слоёв. Поэтому аморфные сплавы выпускают в виде ленты, |
|||||||||
фольги. |
|
|
|
|
|
|
|
|
|
На процесс кристаллизации, размер и форму кристаллов оказывают |
|||||||||
влияние (кроме степени переохлаждения) и другие факторы: посторонние |
|||||||||
неметаллические примеси, механические воздействия, теплоёмкость и те- |
|||||||||
плопроводность самого металла (сплава), температура заливаемого ме- |
|||||||||
талла и формы, состояние поверхности и др. |
|
|
|
|
|
|
|||
Размер зерна металла сильно влияет на его механические свойства. Эти |
|||||||||
свойства (особенно вязкость и пластичность) выше, если металл имеет |
|||||||||
мелкое зерно. |
|
|
|
|
|
|
|
||
34
Очень часто искусственно регулируют размер зерна в отливках путем |
||||||||||
введения в расплавленный металл нерастворимых веществ. Нераствори- |
||||||||||
мые включения играют роль центров кристаллизации, от количества ко- |
||||||||||
торых зависит получение того или иного размера зерна. Чем больше при- |
||||||||||
месей, тем больше центров кристаллизации, тем мельче получается зерно. |
||||||||||
Этот процесс называется модифицированием, а вещества, которые для этой |
||||||||||
цели используются, – модификаторами. |
|
|||||||||
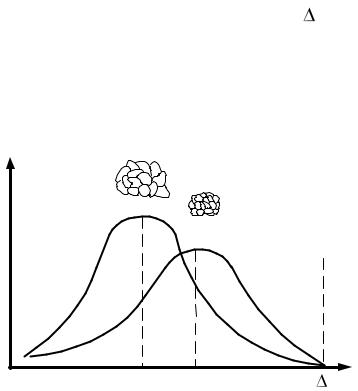
В процессе кристаллизации |
|
|
||||||||
структура |
слитка |
состоит |
из |
|
4 |
|||||
|
|
|||||||||
трёх зон, каждая из которых |
|
|
||||||||
характеризуется |
особым |
|
рас- |
|
|
|||||
положением зёрен |
(рис. |
5.3), |
|
1 |
||||||
образовавшихся при различных |
|
2 |
||||||||
условиях |
охлаждения. |
Первая |
|
|||||||
|
|
|||||||||
зона 1 – наружная мелкозерни- |
|
3 |
||||||||
|
|
|||||||||
стая корка. Она образуется при |
|
|
||||||||
соприкосновении |
расплавлен- |
|
|
|||||||
ного |
металла |
с |
холодными |
|
|
|||||
стенками |
изложницы. |
Металл |
|
|
||||||
сильно переохлаждается и воз- |
|
|
||||||||
никает |
|
значительное |
число |
Рис. 5.3. Схема строения стального слит- |
||||||
центров |
кристаллизации, |
|
тем |
ка: |
1 – наружная мелкозернистая корка; |
|||||
|
2 |
– крупные столбчатые кристаллы; |
||||||||
более, что посторонние твердые |
||||||||||
3 – равноосные кристаллы; 4 – усадочная |
||||||||||
частицы и выступы на поверх- |
||||||||||
раковина |
||||||||||
ности изложницы создают до- |
||||||||||
|
|
|||||||||
полнительные центры кристаллизации. Эта зона имеет небольшую глубину. |
||||||||||
Вторая зона 2 характеризуется образованием крупных столбчатых |
||||||||||
кристаллов (дендритов), которые растут перпендикулярно стенкам и дну |
||||||||||
изложницы в сторону, обратную направлению отвода тепла от жидкости. |
||||||||||
Третья зона 3 состоит из различно ориентированных равноосных кри- |
||||||||||
сталлов различного размера, которые всегда больше, чем кристаллы первой |
||||||||||
зоны. |
|
|
|
|
|
|
|
|
|
|
Столбчатые кристаллы для малопластичных металлов с точки зрения |
||||||||||
механической прочности нежелательны. Особенно непрочными являются |
||||||||||
места встречи дендритов, растущих от разных стенок изложницы. Они |
||||||||||
35
являются местами образования различных дефектов – пустот, неметаллических включений и т. д.
Четвёртая зона 4 – усадочная раковина. Жидкий металл имеет больший объём, чем закристаллизовавшийся, поэтому залитый в изложницу металл в процессе кристаллизации сокращается в объеме, что приводит к образованию пустот, называемых усадочными раковинами, которые могут быть сконцентрированы в одном месте, либо рассеяны по всему объёму слитка или его части.
5.2. Порядок выполнения работы
Исследовать процесс кристаллизации реального стального сплава визуально в условиях учебной лаборатории практически невозможно. Поэтому процесс образования кристаллов в настоящей работе изучается на примере кристаллизации водного раствора соли хлористого аммония (NH3CL) с помощью бинокулярного микроскопа МБС-9.
После нанесения капли раствора на предметное стекло начинается процесс испарения воды, приводящий к кристаллизации раствора и выпадению кристаллов. Раствор хлористого аммония позволяет наблюдать процесс роста дендритных кристаллов. При этом нужно обратить внимание на последовательность развития кристаллов, направление их роста, искажение формы при взаимном их соприкосновении.
Исследуя продольный и поперечный излом сурьмы, нужно выявить все зоны кристаллизации, которые образуются при кристаллизации металлического слитка.
5.3. Содержание отчёта
1.Описание цели работы.
2.Рисунок затвердевшей капли хлористого аммония.
3.Рисунки продольного и поперечного сечения слитка сурьмы с указанием зон кристаллизации.
4.Выводы.
36
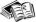
5.4. Контрольные вопросы
1.Что называется первичной кристаллизацией?
2.Что называется степенью переохлаждения?
3.От чего зависит степень переохлаждения?
4.Что называется свободной энергией?
5.Как влияет Ч.Ц. и С.К. на размер зерна?
6.Можно ли искусственно изменять размер зерна?
7.Каковы зоны кристаллизации стального слитка?
8.Что называется модифицированием?
9.Как влияет размер зерна на механические свойства сплава?
Рекомендуемая литература [1–3, 6].
6. ИССЛЕДОВАНИЕ ВЛИЯНИЯ СКОРОСТИ ОХЛАЖДЕНИЯ НА СВОЙСТВА СТАЛИ
Цель работы: исследовать влияние скорости охлаждения на твердость углеродистой стали, нагретой до температуры закалки.
Приборы и оборудование: комплект лабораторных образцов, твердомер Роквелла ТК-2.
6.1. Краткие теоретические сведения
Способом, позволяющим изменять структуру и свойства сплавов, является термическая обработка. Термическая обработка сплавов, в частности стали, в большинстве случаев состоит в нагреве до определённой температуры, выдержке при этой температуре и охлаждении с разными скоростями в зависимости от требуемой конечной структуры и физи- ко-механических свойств.
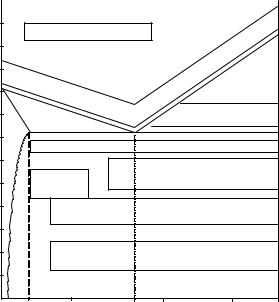
Диаграмма состояния сплавов железа с углеродом даёт представление о структурных превращениях, протекающих в железоуглеродистых сплавах при очень медленном нагреве или охлаждении. При увеличении скорости охлаждения превращения аустенита смещаются в область низких температур, что используется при термической обработке стали.
37
Термическая обработка применяется для выравнивания химического |
||||||||||||
состава сплавов, снятия внутренних напряжений, устранения наклёпа, |
||||||||||||
улучшения обрабатываемости, повышения стойкости режущего инстру- |
||||||||||||
мента, прочности, твёрдости и износостойкости деталей и ряда других |
||||||||||||
свойств. |
|
|
|
|
|
|
|
|
|
|
||
Т, оС |
|
|
|
|
Интервалы температур на- |
|||||||
1200 |
|
|
|
|
грева |
для |
различных |
видов |
||||
|
|
1 |
|
термической |
обработки |
при- |
||||||
1100 |
|
|
|
|||||||||
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
|
|
|
||
1000 |
|
|
|
|
ведены на рис. 6.1. |
|
|
|
||||
900 |
|
|
2 |
|
Охлаждение |
стали |
произ- |
|||||
800 |
|
|
3 |
водится с различными скоро- |
||||||||
|
|
|
||||||||||
700 |
|
|
4 |
|
стями |
в зависимости от |
того, |
|||||
600 |
|
|
|
|
|
|
|
|
|
|
||
|
|
6 |
|
какие |
свойства |
необходимо |
||||||
500 |
|
5 |
|
получить. Различные скорости |
||||||||
|
|
|
||||||||||
400 |
|
|
|
|||||||||
|
|
7 |
|
охлаждения |
стали |
приводят к |
||||||
300 |
|
|
|
|||||||||
|
|
|
|
получению |
различных |
струк- |
||||||
200 |
|
|
8 |
|
||||||||
|
|
|
тур. |
|
|
|
|
|
|
|||
100 |
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
Скорости охлаждения |
для |
|||||||
|
|
|
|
|
||||||||
|
0,02 |
0,5 |
0,8 1,0 |
1,5 С,% |
разнообразных |
видов |
терми- |
|||||
|
|
|
|
|
||||||||
Рис. 6.1. Температура нагрева при раз- |
ческой |
обработки |
опреде- |
|||||||||
|
|
|
|
|
|
|
||||||
личных видах |
термической |
обработки: |
ляются по диаграмме изотер- |
|||||||||
1 – диффузионный отжиг; 2 – нормализа- |
мического |
превращения |
ау- |
|||||||||
ция, |
полный |
отжиг и полная закалка; |
стенита. На рис. 6.2 представ- |
|||||||||
3 – неполный отжиг и неполная закалка; |
лена такая диаграмма для эв- |
|||||||||||
4 – рекристаллизационный отжиг; 5 – от- |
||||||||||||
тектоидной стали. |
|
|
|
|||||||||
жиг для снятия внутренних напряжений; |
|
|
|
|||||||||
При малых |
скоростях ох- |
|||||||||||
6 – высокий отпуск; 7 – средний отпуск; |
||||||||||||
|
|
|
|
|
|
|
||||||
8 – низкий отпуск |
|
лаждения V1 аустенит превра- |
||||||||||
|
|
|
|
|
щается в перлит с твердостью |
|||||||
HRC 15–20. При скоростях V2 образуется сорбит (HRC 20–30), при V3 – |
||||||||||||
троостит (HRC 35–40). При скорости охлаждения выше V3 |
произойдет |
|||||||||||
лишь частичный распад аустенита с образованием троостита. Не распав- |
||||||||||||
шаяся |
часть |
аустенита |
претерпит |
бездиффузионное |
аустени- |
|||||||
то-мартенситное превращение. В результате образуется троосто-мартен- |
||||||||||||
ситная структура, которая чаще всего является нежелательной. При ско- |
||||||||||||
ростях выше Vкр в стали образуется только мартенсит. |
|
|
|
|
|
|||||||
38
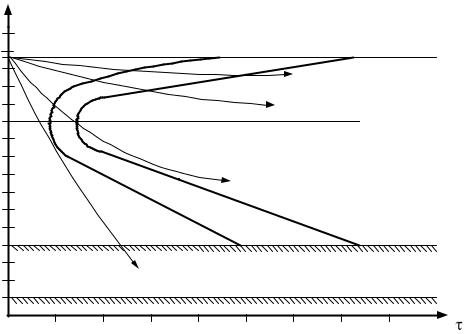
Наименьшая скорость охлаждения Vкр, при которой из аустенита образуется только мартенсит, называется критической скоростью закалки.
Различают следующие (основные) виды термической обработки:
–отжиг 1-го рода (диффузионный, рекристаллизационный и отжиг для снятия внутренних напряжений);
–отжиг 2-го рода (полный, неполный, циклический);
–закалка;
–отпуск.
Т, оС |
|
|
|
|
А1 |
|
|
|
|
|
|
V2 |
V1 |
П |
|
|
С |
Т |
|
550 |
|
|
|
|
|
|
|
|
|
А |
|
V3 |
Б |
|
|
|
|
||
|
|
|
|
|
Mн |
|
|
|
|
250 |
|
|
|
|
Мк |
Vкр |
М+А |
|
|
|
|
|
||
|
|
|
|
|
- 50 |
|
|
|
|
0 |
|
|
|
log |
|
|
|
|
|
Рис. 6.2. Схема диаграммы изотермического превращения |
||||
переохлаждённого аустенита эвтектоидной стали: П – перлит; |
||||
С – сорбит; Т – троостит; Б – бейнит |
|
|
||
Диффузионный отжиг применяется для крупногабаритных отливок с целью устранения ликвации. Иногда этот процесс называют гомогенизацией (от слова «гомогенный» – (однородный). При гомогенизации сталь нагревают до температуры 1050…1200 оС, время выдержки 8…20 часов и медленное охлаждение.
Диффузионный отжиг приводит к росту зерна. Этот дефект может быть устранён дополнительным отжигом на мелкое зерно или нормализацией. В результате гомогенизации у стали повышаются такие механические свойства, как ударная вязкость и усталостные характеристики.
39
Рекристаллизационный отжиг проводится при температуре 650…700 оС.
Время выдержки зависит от габаритов заготовки. Цель такого отжига – устранение наклёпа и повышение пластичности. Используется перед холодной обработкой давлением и как промежуточная операция для снятия наклёпа в деталях, прошедших холодную обработку давлением.
Отжиг для снятия остаточных напряжений необходим для изделий, в
которых после предшествующих технологических операций (обработка резанием, сварка и др.) возникли остаточные напряжения. При этом виде отжига производится нагрев до 160…700 оС с выдержкой 2,5…3 мин на 1 мм толщины сечения.
Полный отжиг заключается в нагреве доэвтектоидной стали на 30…50 оС выше температуры, соответствующей точке Ас3, выдержке для полного завершения фазовых превращений и последующем медленном охлаждении. В результате полного отжига получается мелкозернистая структура, обеспечивающая вязкость и пластичность.
Неполный отжиг отличается от полного тем, что нагрев производится до температуры на 10…30 оС выше точки Ас1. Неполный отжиг для доэвтектодных сталей применяется тогда, когда требуется только снижение твёрдости. Заэвтектоидные стали подвергаются только неполному отжигу.
Нормализация заключается в нагреве стали до температуры Ас3 + (30…50) оС или Аст + (30…50) оС, выдержке для прогрева и завершения фазовых превращений и охлаждения на воздухе. Нормализация вызывает полную фазовую перекристаллизацию и устраняет крупнозернистую структуру, полученную при литье, прокате, ковке или штамповке. Нормализация широко используется для улучшения свойств стальных отливок вместо закалки и отпуска.
Закалка заключается в нагреве доэвтектодных сталей до температур на 30…50 оС выше Ас3 (полная закалка), а заэвтектоидных – на 30…50 оС выше Ас1 (неполная закалка). Неполная закалка доэвтектоидных сталей Ас1 + (30…50) оС и полная заэвтектоидных Аст + (30…50) оС, как правило, не производится. После нагрева и выдержки сталь охлаждается со скоростью не ниже критической.
Для получения различных структур при закалке изделия охлаждают с различной скоростью, которая зависит от охлаждающей среды, формы изделия и теплопроводности стали. Охлаждающая способность различных сред представлена в табл. 6.1.
40
