- •Практическая значимость результатов исследований.
- •Основная часть
- •1.1.1 Результаты анализа модифицированных металлами форм шунгита и аморфного SiO2
- •1.2 Исследование физико – химических свойств нанокомпозитов с Ni
- •1.3 Исследование физико – химических свойств нанокомпозитов с Fe и Co
- •1.4 Исследование физико-химических свойств нанокомпозитов с Cu
- •1.4.1 Исследования электрохимического поведения композитов на основе модифицированного медью шунгита
- •Список использованных источников
1.1.1 Результаты анализа модифицированных металлами форм шунгита и аморфного SiO2
Исследование структуры образцов шунгита выполняли с помощью дифрактометра ДРОН-4-07 в режиме 25 кВ, 25 мА. С использованием трубки с кобальтовым (Со) анодом. Съемку рентгенограмм проводили со скоростью 1 град/мин в диапазоне углов от 8 до 70 оΘ, в режиме непрерывного сканирования, с записью на диаграмную ленту. Скорость диаграммной ленты составляло 720 мм/ч.
Фазовый состав исследуемых образцов определяли методом сравнения найденных по экспериментальным данным межплоскостных расстояний и относительных интенсивностей соответствующих линий рентгенограммы с табличными данными этих величин, приведенными в американской рентгенографической картотеке стандартов JCPDS. Величины межплоскостных расстояний d, набор которых характерен для вещества определенного состава и строения, находили по уравнению Брегга-Вульфа:
SinΘ=nλ/2d (1)
где Θ – измеренный угол; n – порядок отражения рефлексов; λ – длина волны Å; d – межплоскостное расстояние, Å.
На рисунке 1 показаны результаты рентгенофазового анализа силикатного шунгита.
Рефлексы на рентгенограммах относятся в Å относятся к фазам: 3,34; 4,27 и др. – α кварц SiO2; 10,0; 2,56 и др. – мусковит KAl2[OH]2{AlSi3O10}; 3,03; 1,91 и др. – кальцит СaCO3; 2,98; 1,42 и др. – диоксид CaMgSi2O6.
Следует отметить, что самый интенсивный рефлекс углерода (С) совпадает с рефлексом SiO2 – 3,35 Å.
Таким образом, образец шунгита состоят из фаз: углерода, кварца, мусковита, кальцита и диоксида. Надписи над сигналами соответствуют наличию следующих фаз: SiO2 – кварц; СaCO3 – кальцит; CaMgSi2O6 – диоксид; KAl2[OH]2{AlSi3O10} – мусковит.

Рисунок 1 – Рентгенограмма образца силикатного шунгита
Полученные результаты элементного анализа Коксуйских шунгитов, показали, что входящие в состав шунгита соединения оксида алюминия и кварца составляя 70% по массе тела, шунгитовых пород и могут стать объектом выщелачивания для дальнейшего увеличения удельной поверхности.
Нами было апробирована методика определения удельной поверхности шунгитов по низкотемпературной адсорбции жидкого азота (метод БЭТ-а). Было установлена, что удельная поверхность силикатного и карбонатного шунгитов равны 7,54 и 12,24 м2/г, соответственно.
На основе проведенного рентгенофазового анализа установлено, что силикатная форма шунгита состоит из пяти фаз: углерод, кварц, кальцит, диоксид и мусковит.
С помощью Мессбауэровской спектроскопии исследовался процесс термической обработки Коксуйского шунгита. Спектры снимались на спектрометре СМ 2201 и приведены на рисунке 2-1 и 2-1а. Источником служил Со-57 в Cr активностью 100 мКи.
Во всех спектрах образцов присутствуют мелкие частицы с железом в 2-х и 3-х валентном состоянии (Fe3+, Fe2+) в разных количествах.
У крупных частиц металлического железа поле на ядре составляет 330 кЭ. Компонента 1 в образцах 1 и 1а имеет поле не намного больше, чем у чистого железа, возможно из-за присутствия внутри частиц железа атомов Ni. А во 2-м компоненте возможно в решётке железа присутствуют более лёгкие элементы (возможно Al).
Во всех остальных образцах вероятно в решетке железа присутствуют в разных количествах атомы Co и Ni.

Рисунок 2 – Результаты Мессбауэровской спектроскопии
Анализ полученных результатов показывает, что процесс восстановления железа в шунгите протекает последовательно, через стадию Fe2+. Замена водородной атмосферы на кислородсодержащую при комнатной температуре не приводит к полному окислению металлического состояния железа, происходит лишь некоторое уменьшение количества последнего (до 61%), и увеличения содержания форм Fe3+ и Fe2+ (до 19 – 20%). Возможность широкого модифицирования фазового состава Коксуйского шунгита делает его весьма перспективным сырьем для получения новых материалов.
На основании исследовании с помощью Мессбауэровской спектроскопии установлена возможность восстановления окисленных форм железа в шунгите, которое происходит при термической обработке в токе водорода. Коксуйский шунгит может быть модифицирован ионом любого металла, который в восстановительной среде переходит в его восстановленные формы.
Это позволит варьировать количество металла в носителе, что имеет перспективу в получении новых электродных материалов для осуществления электрокаталитических процессов с участием органических соединений.
Шунгитовый углерод – элементарный углерод со специфичной структурой. Основу её представляет многослойная глобула размером около 10 нм. Такая структура очень активная в окислительно-восстановительных реакциях, обладающая сорбционными и каталитическими свойствами.
Углерод в породе образует матрицу, в которой распределены высокодисперсные силикаты с размером частиц 0,5 – мкм, что хорошо видно из фотографии, приведенной на рисунках 3 и 4, где показана структура исходного Коксуйского шунгита. Характерным для данного минерала является большое содержание SiO2, что и определяет особенность поведения в электрохимических условиях исследования модифицированных форм композитов, полученных на его основе.
Был дополнительно произведен физико-химический анализ, как исходного минерала, так и его модифицированных форм с помощью современных приборов физико-химического анализа – рентгеновского дифрактометра X'Pert MPD PRO (PAN analytical) и низковакуумного растрового электронного микроскопа в комплекте с системой энергодисперсионного рентгеновского микроанализа Jeol JSM-6490 LA.
Элементный анализ каждой пробы, проводимый на низковакуумном растровом электронном микроскопе в комплекте с системой энергодисперсионного рентгеновского микроанализа, выполняли не менее чем в трех точках образца, результаты затем усредняли, одновременно получали снимки поверхности. Поскольку шунгит был и модифицирован солями металлов, то картину поверхностей модифицированных образцов обязательно сравнивали с поверхностью исходного материала.
Анализ фазового состава образцов показал, что основными фазами в нем являются кварц, графит, широкий перечень алюмосиликатных структур, в том числе – мусковит, биотит, флогопит и др. Из элементов представлены все перечисленные выше, в том числе кальций, фосфор, натрий и сера. Результаты рентгенофазового анализа приведены в таблицах 1 и 2.
Образцы модифицированного шунгита с различным содержанием ионов железа и кобальта, получены методом пропитки из их уксуснокислых солей. Наличие восстановленных форм ионов металлов подверглись рентгеновскому микроанализу. Массовые содержания модифицирующих металлов в шунгите находятся в пределах ошибки экспериментов. На основании данных, приведенных в таблицах 1 и 2 можно судить об образовании новых материалов с мелкодисперсными частицами железа и кобальта в шунгите. Наличие металлов и их восстановленных форм могут быть подтверждены и с помощью РФА и электрохимическим методом.
Таблица 1 - Результаты элементного рентгенофазового анализа шунгита модифицированного железом
|
Элемент |
Шунгит модиф. Fe (5 %) при 200 0С, масс. % |
Шунгит модиф. Fe (15 %) при 200 0С, масс. % |
Шунгит модиф. Fe (5 %) при 400 0С, масс. % |
Шунгит модиф. Fe (10 %) при 400 0С, масс. % |
Шунгит модиф. Fe (15 % ) при 400 0С, масс. % |
|
С |
13,4 |
21,4 |
24,78 |
21,4 |
14,86 |
|
О |
43,3 |
32,9 |
44,81 |
36,0 |
19,67 |
|
Al |
14,28 |
5,4 |
4,95 |
5,1 |
4,09 |
|
Si |
18,64 |
20,2 |
18,75 |
22,0 |
29,27 |
|
Na |
- |
- |
0.8 |
- |
- |
|
К |
6,34 |
2,0 |
1,41 |
1,2 |
3,76 |
|
Fe |
4,3 |
15,2 |
4,56 |
4,8 |
28,34 |
|
Ва |
- |
2,64 |
- |
- |
- |
|
Mg |
- |
- |
0,74 |
- |
- |
Таблица 2 - Результаты элементного рентгенофазового анализа шунгита модифицированного кобальтом
|
Элемент |
Шунгит модиф. Со (10 %) при 200 0С, масс. % |
Шунгит модиф. Со (15 %) при 200 0С, масс. % |
Шунгит модиф. Со (10 %) при 400 0С, масс. % |
Шунгит модиф. Со (15 %) при 400 0С, масс. % |
|
1 |
2 |
3 |
4 |
5 |
|
С |
19,13 |
17,61 |
25,95 |
18,7 |
|
О |
41,68 |
29,94 |
34,96 |
37,8 |
|
Al |
5,37 |
5,09 |
5,31 |
4,8 |
|
Продолжение таблицы 2 |
||||
|
1 |
2 |
3 |
4 |
5 |
|
Si |
19,40 |
30,42 |
19,91 |
22,7 |
|
К |
2,31 |
1,94 |
1,47 |
1,4 |
|
Fe |
4,23 |
6,39 |
7,86 |
3,4 |
|
Сo |
7,87 |
8,61 |
4,54 |
10,9 |
Методом рентгенофазового анализа были проведены исследования образцов модифицированных шунгитов, полученных в токе аргона и водорода при 4000С. На рисунке 3 представлена диаграмма РФА для шунгита с 10 % железом.
Обнаружено, что на рентгенограммах присутствуют рефлексы характерные для α-кварца и мусковита, которые присутствуют в исходном образце шунгита, также имеется рефлекс при 2,02 для α-Fe (ASTM 6 – 696), что указывает на наличие дисперсных частиц железа в полученном нами образце.
По результатам рентгеноспектрального анализа было установлено, что во взятых для исследования образцах шунгита содержится более 60 % оксида кремния, и около 10 % оксида алюминия. Кроме того, в шунгите найдены оксиды различных металлов, обладающих адсорбционными свойствами к некоторым органическим веществам (фенол и его производные).

Рисунок 3 – Фотография шунгита, снятый на низковакуумном растровом микроскопе
Jeol JSM – 6490 LA
Элементный анализ каждой пробы, проводимый на низковакуумном растровом электронном микроскопе в комплекте с системой энергодисперсионного рентгеновского микроанализа, выполняли не менее чем в трех точках образца. Результаты трех анализов усредняли, одновременно получали снимки поверхности. Поскольку шунгит был модифицирован различными солями металлов, то картину поверхностей сравнивали с поверхностью исходного материала.
На рисунке 4 приведено распределение частиц по поверхности силиката, содержащегося в исходном материале, взятое из двух точек. Идентичность состава показали относительную равномерность поверхности, что позволяет ожидать возможность осуществления синтеза новых материалов с одинаковой структурой, путем его модифицирования.
|
|
|
Рисунок 4– Распределение фаз по составу в шунгите
Образцы модифицированного шунгита с различным содержанием ионов железа, кобальта и никеля, получены методом пропитки из их уксуснокислых солей. Наличие восстановленных форм ионов металлов подтверждаются результатами рентгенофазового анализа. На представленном ниже рисунке – 5 обнаружены частицы металлического кобальта, которые были введены в виде его карбоксилат ионов, с последующим их восстановлением в токе водорода, в инертной среде (Ar).

Рисунок 5 – Фотография, снятая на низковакуумном растровом микроскопе Jeol JSM – 6490 LA шунгита модифицированного кобальтом
|
|
|
Рисунок 6 – Распределение фаз по составу шунгита модифицированного кобальтом
Зерно риса находится в оболочке, которую учёные называют цветковой чешуёй, а производственники – лузгой или шелухой. Осенью зерно с полей свозится на крупозаводы, где оно очищается от оболочки, а солома остаётся в поле. Очищенное от лузги зерно имеет жёлтый цвет, а для получения привычного потребителю белого цвета рис шлифуют, удаляя верхний слой. Таким образом, в процессе получения крупы белого шлифованного риса образуется три вида отходов: солома, цветковая чешуя (лузга, шелуха) и отруби (мучка). Количество отходов на предприятии при получении крупы риса составляет до 30 процентов от массы сухого зерна.

Рисунок 7 - Вид под микроскопом поверхности частиц аморфного кремнезёма, полученного из рисовой шелухи
Основываясь на анализе научной литературы: отходы от производства риса отличаются по своему химическому составу от всех других злаковых культур прежде всего большим содержанием в соломе и шелухе аморфного диоксида кремния. Поэтому теплотворная способность соломы и лузги ниже, чем у древесины или соломы и шелухи других зерновых (например, овса, гречихи), а при сжигании образуется много мелкодисперсной золы, которая имеет ограниченный диапазон возможного использования (хотя и она может приносить доход производителям шелухи). Качество корма или удобрения из шелухи и соломы очень низкое также из-за высокого содержания кремнезёма. Дробление рисовых отходов быстро приводит к износу оборудования в силу их высокой абразивности. Химический состав всех отходов риса (соломы, шелухи и мучки) указывает на наличие ряда полезных человеку веществ.
Исследования морфологии поверхности рисовой шелухи и её модифицированных форм проводились применением методов, как сканирующая электронная и атомно-силовая микроскопия, которые дает возможность оценить размеры пор и частиц в них. Однако использование этих методов для характеристики частиц, находящихся внутри пор аморфного силиката (SiO2), связано с большими экспериментальными затруднениями.
На следующем рис. 8 приведено АСМ - изображение поверхности исходного материала для получения аморфного силиката – рисовая шелуха.

Рисунок 8 – АСМ - изображение рисовой шелухи
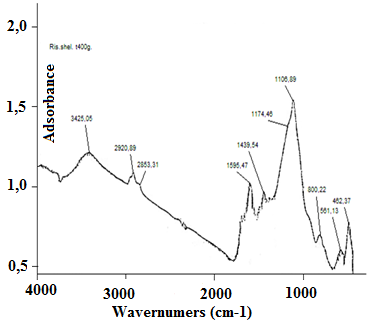
Данные ИК-спектроскопии продуктов пиролиза рисовой шелухи, полученные на приборe Specord-M80 при температурах 4000С, 5000С, и 6000С в токе аргон показаны на рисунках 9а, 9б, и 9в, соответственно.
Для продукта пиролиза рисовой шелухи, полученные при 4000С имеются характерные импульсы сдвоенных полос поглощения, отвечающих за валентные колебания групп Si – О; Si – O – Si - 1174 и 1106; а ν 2920, 2853; δ1439 см-1 – ν-С-Н (гр-СН2); ν ОН-3425 см-1, ν ОН-1596 см-1 за свободные ОН- - группы отвечает полоса поглощения 3634-3635 см-1, а за связанные водородной связью ОН – группы область поглощения – 3417-3428 см-1. Широкая полоса поглощения в области 3100-3500 см-1 характеризует колебания ОН - группы. В области 2900-3000 см-1 проявляются полосы поглощения колебания метильной группы (СН3)-группы. При 2600-2900 см-1 наблюдаются полосы поглощения метиленовых групп (СН2).
Особенностями ИК-спектров продуктов пиролиза рисовой шелухи, полученных при температурах 5000С, и 6000С, которые показаны на рисунках 9б и 9в, соответстенно является исчезновение полос валентных колебании при 2600-2900 см-1 характерных для поглощения метиленовых групп (СН2).
|
|
|
|
а б в
Обозначение: а – 400 ºС; б - 500 ºС; в - 600 ºС; инертный газ Ar.
Рисунок 9 - ИК- спектры продуктов пиролиза рисовой шелухи
На рисунок 10 представлены АСМ - изображение поверхности аморфного силиката, полученного термическим восстановительным (Н2) разложением рисовой шелухи при температуре 5000С, в инертной среде аргона.
Из рисунок 10 видно, что SiO2 имеет пористую структуру, причем поры можно разделить на крупные (глубина 50—60 нм, диаметр 0,7—1,0 мкм) и мелкие (глубина 30—40 нм, диаметр 100—120 нм). Образование пор, вероятно, обусловлено температурным воздействием на органическую часть шелухи, что приводит к образованию аморфной структуры продукта пиролиза. Важно отметить, что крупные поры образуются из-за скопления в одном месте мелких пор, т.е. представляют собой впадины с неравномерной поверхностью дна, глубина которых на 10—20 нм больше, чем глубина мелких пор. На основании этого можно предположить, что основную функциональную нагрузку несут мелкие поры, возможно, именно в них при электроосаждении будет размещаться металл.
Как видно, из рисунков 10 и 11, где изображена поверхность аморфного силиката, которая отличается наличием равномерных расщелин с характерными впадинами, представляющим заметным скоплением мелких пор. Можно предположить, что размеры частиц, которые могут осаждаться при модифицировании в матрице будут соизмеримы с размерами её пор (глубина 30 - 40 нм, диаметр 100 -120 нм).

Рисунок 10 - АСМ-изображения поверхности аморфного силиката

Рисунок 11 – АСМ - изображение поверхности продукта пиролиза рисовой шелухи и распределение пор