
Органическая химия.Казань
.pdf
160
Биологически активные соединения – химические соединения различной природы и происхождения, которые будучи введенными в организм, оказывают воздействие на биологические процессы и характеризуются высокой специфичностью и активностью.
Биполярный ион (цвиттер-ион) – нейтральные молекулы, в которых одновременно присутствуют пространственно разделенные противоположные заряды. Такие ионы образуют, например, аминокислоты.
|
O |
|
|
|
O |
CH3- |
CH-C |
CH3- |
|
CH-C |
|
|
OH |
|
|
+ |
O- |
|
|
||||
NH2 |
NH3 |
||||
Биурет – соединение, отвечающее структуре H2N-CO-NH-CO-NH2. Получают разложением мочевины. Качественной реакцией на биурет (биуретовая реакция) является его взаимодействие с катионом Cu2+ в щелочной среде и появление фиолетовой окраски. В реакцию типа биуретовой вступают амиды и имиды аминокислот.
В
Вагнера реакция – окисление алкенов в гликоли (диолы) действием перманганата калия в щелочной среде:
CH2=CH2 KMnO4 CH2 CH2 OH OH
Вальденовское обращение – обращение конфигурации хирального центра при протекании реакции по SN2-механизму. Если в исходной молекуле имеется только один хиральный центр, то в результате вальденовского обращения образуется соединение с противоположной относительной конфигурацией по отношению к исходной.
|
COOH |
PCl5 |
|
COOH |
|
|
HO |
* |
H |
H |
* |
|
|
C |
|
C Cl |
|
|||
|
CH2COOH |
|
|
CH2COOH |
|
|
gOH L-яблочная кислота |
D-хлорянтарная кисл |
+AgOH |
||||
|
COOH |
|
|
COOH |
|
|
Cl |
* |
H |
PCl5 |
H |
* |
|
C |
|
C OH |
|
|||
|
CH2COOH |
|
|
CH2COOH |
|
|
161
Вицинальный (соседний) – термин, используемый для обозначения положения двух атомов или атомных групп, связанных с двумя соседними атомами. Сокращенно виц.
|
|
H |
|
OH |
|
|
Br |
H |
|||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
C |
|
C |
|
H |
H |
|
C |
|
C |
|
H |
||||
|
|
|
|||||||||||||||
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
OH H |
|
|
H |
Br |
|||||||||||
вицинальные ОН-группы |
|
|
|
|
вицинальные атомы Br |
||||||||||||
Возгонка – (сублимация), переход вещества из твердого состояния в газообразное, минуя жидкое; является фазовым переходом первого рода.
Вымораживание – концентрирование растворов путем перевода растворителя в твердую фазу за счет охлаждения раствора.
Выпаривание – концентрирование растворов нелетучих соединений частичным испарением растворителя при кипении.
Высшие жирные кислоты – природные или синтетические карбоновые кислоты алифатического ряда, содержащие не менее 6 углеродных атомов. Кислоты природного происхождения получают из растительных жиров, синтетические – из нефтехимического сырья.
Вюрца реакция – получение углеводородов взаимодействием алкилгалогенидов с металлическим натрием. При использовании разных алкилгалогенидов образуется смесь углеводородов.
2 R-I + 2Na R-R + 2NaI
Г
Гетеролитический разрыв связи – расщепление ковалентной связи, в результате которого связующая пара электронов остается у более электроотрицательного атома, что приводит к образованию заряженных частиц: H|:X H+ + X- Гибридизация – комбинация («смешение») атомных орбиталей разных типов, принадлежащих одному атому, в результате чего образуется набор эквива-
лентных гибридных орбиталей.
Гидразиды – функциональные производные карбоновых кислот, в карбоксильной группе которых -ОН замещен на остаток гидразина:
O
R C
NH-NH2
Гидразоны – продукты взаимодействия альдегидов и кетонов с гидрази-
ном:
|
|
|
O |
|
|
|
N-NH2 |
R |
|
C |
+ NH2-NH2 |
R |
|
C |
+ H2O |
|
|
||||||
|
|
|
R' |
|
|
|
R' |
Гидратация – взаимодействие веществ с водой, характеризующееся тем, что молекула воды присоединяется к исходной молекуле полностью.
Гидридный сдвиг – процесс переноса гидрид-иона Н- от одной частицы к другой.

162
Гидрирование (гидрогенизация) – присоединение водорода к органическим соединениям. Процесс может осуществляться при различных условиях (давление, температура) и катализируется, как правило, металлами VII группы или оксидами и сульфидами металлов.
Гидрогалогенирование – присоединение галогеноводородов к непредельным соединениям. В ряду HHal легче присоединяется HI, труд
нее HCl (HI > HBr > HCl). Процесс Г. алкенов и алкинов осуществляется в соответствии с правилом Марковникова.
Гидрогенизация жира – гидрирование жиров путем присоединения водорода к непредельным остаткам высших жирных кислот, входящих в состав жира. Используется для снижения ненасыщенности жиров и изменения их вязкости.
Гидроксикислоты – производные карбоновых кислот, в углеводородном радикале которых содержится гидроксигруппа.
Гидроксилирование – введение гидроксигруппы в молекулы органических соединений. Процесс реализуется в реакциях замещения (R-Cl + HOH R-OH + HCl), присоединения (CH2=CH2 + HOH CH3-CH2OH), окисления и т.д.
Гидролиз – взаимодействие ионов соли с водой, приводящее к образованию слабого электролита и, следовательно, изменению рН среды.
Гликозиды – группа природных соединений, молекулы которых состоят из неуглеводного компонента (агликона) и остатка углевода, связанных между собой гликозидной связью. Различают С-гликозиды (С-С-связь между углеводным остатком и агликоном), N-гликозиды (С-N-связь между углеводным остатком и агликоном), О-гликозиды (С-О-связь между углеводным остатком и агликоном), S-гликозиды (С-S-связь между углеводным остатком и агликоном).
Гликозиды сердечные – группа природных соединений, оказывающих кардиотоническое действие. Агликоны имеют стероидную природу.
Гликоли – диолы, в которых гидроксигруппы находятся в вицинальном положении, т.е. связаны с соседними атомами углерода.
Гомолитический разрыв связи – расщепление ковалентной связи, в результате которого у каждой из образующихся частиц остается по одному неспа-
ренному электрону: |
|
|||
. |
|
A. + B. |
||
A |
|
. |
B |
|
Гриньяра реакция – методы синтеза органических соединений, основанные на присоединении реактивов Гриньяра к поляризованным кратным связям
H-CH=O |
1) CH3MgI (эфир) |
CH3CH2OH + MgOHI |
|
2) H2O |
|||
|
|
Д
Дегидрирующие реагенты – вещества, в присутствии которых осуществляется процесс дегидрирования; они являются акцепторами водорода.
Дегидрогалогенирование – отщепление галогеноводорода от молекулы органического соединения с образованием кратных связей в продукте реакции
163
или формированием циклических структур. Реакцию Д. широко используют для получения соединений, содержащих двойные или тройные связи.
CH3 - CH - CH3 NaOH, сп. р-р CH3-CH=CH2 + NaCl + H2O
Cl
Дегидратация – отщепление воды под влиянием химического или термического воздействия. Различают внутримолекулярную (отщепление воды в пределах одной молекулы) и межмолекулярную (отщепление воды при взаимодействии двух одинаковых или разных молекул) дегидратацию.
Дезаминирование – удаление, отщепление аминогруппы от молекулы ор-
ганического соединения. |
|
|
|
|
H2N- CH2-COOH + HNO2 |
HO-CH2-COOH + N2 + H2O |
|||
Дезоксисахара – моносахариды, в которых одна из спиртовых групп заме- |
||||
нена на атом водорода. |
|
|
|
|
Декарбоксилирование – отщепление CO2 |
из карбоксируппы карбоновых |
|||
кислот. |
|
|
|
|
CH -COONa + NaOH (тв.) |
to |
СH |
+ Na CO |
|
3 |
|
4 |
2 |
3 |
Депсипептиды – пептиды, в молекулах которых |
помимо амидной груп- |
|||
пы –CO-NH- содержатся и сложноэфирные группы –COO-CH2-. Деструкция – расщепление, разрушение структуры.
Диазотирование – формирование диазогруппы взаимодействием первичного амина с азотистой кислотой.
+ -
Ar-NH2 + HNO2 + HX [Ar-N N]X + 2 H2O
Диастереомерия – вид пространственной изомерии, обусловленный наличием в молекуле двух или более хиральных центров. Например, винная и мезовинная кислоты.
|
|
|
COOH |
|
|
|
|
COOH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
C |
|
|
OH |
H |
|
|
|
C |
|
|
OH |
||
|
|
|
|
|
|
|
|
|||||||||
|
|
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
HO |
|
C |
|
|
H |
|
|
C |
|
|
OH |
|||||
|
|
|
|
|
|
|||||||||||
|
|
|||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
COOH |
|
|
|
|
COOH |
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|||||
Диеновый синтез (реакция Дильса-Альдера) – 1,4-присоединение к сопряженным диенам соединений с активированной кратной связью, в результате чего образуются циклические структуры.
CH2 |
CH2 |
|
+ |
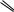 CH2 CH2
CH2 CH2
164
Дикетопиперазины – дикарбонильные производные пиперазина, различающиеся между собой положением карбонильных групп.
H |
|
|
H |
|
|
H |
|||||||
N |
|
|
N |
|
|
|
|
|
|
||||
|
|
|
|
N |
|||||||||
|
|
O |
O |
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
O |
|
|
|
|
O |
O |
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
N |
|
|
N |
|
|
N |
|||||||
H |
|
|
H |
|
|
H |
|||||||
Диоксаны – насыщенные шестичленные циклические соединения, содержащие два атома кислорода и различающиеся их взаимным расположением.
O O |
O |
O |
|
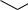 O
O  O
O
Дипольный момент – векторная величина, характеризующая меру смещения положительных и отрицательных зарядов в полярных молекулах. Определяется произведением величины заряда на расстояние между центрами зарядов.
Дисахариды – представители олигосахаридов, молекулы которых состоят из двух моносахаридных остатков (например, мальтоза).
|
CH2O H |
|
|
CH2O H |
|||||||||
|
|
|
O |
|
|
|
|
|
O |
|
|||
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|||||||||
|
OH |
|
O |
|
|
OH |
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||
HO |
|
|
|
|
|
|
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
OH |
|
|
|
|
OH |
|||||
Диспропорционирование (дисмутация) – это реакция самоокисления – самовосстановления органических соединений в щелочной среде.
2 H-CH=O OH- H-COOH + CH3OH
Е
Енол – соединение, в котором ОН-группа связана с одним из атомов углерода двойной связи. Енолы неустойчивы и изомеризуются в соответствующие карбонильные соединения.
R |
|
C |
|
CH2 |
R |
|
C |
|
CH3 |
||
|
|
|
|
||||||||
|
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||
|
OH |
|
|
O |
|||||||
Ж
Жиры – вещества животного и растительного происхождения, представляющие собой сложные эфиры глицерина и высших жирных кислот.
CH2OCOC17H33
CHOCOC17H31
CH2OCOC17H33
165
Живица – продукт жизнедеятельности растений, преимущественно представителей хвойных (сосна, ель, пихта и др.). Содержится в смоляных ходах и выполняет защитную функцию от проникновения патогенных грибов и вредителей через поверхность поврежденных участков коры. В состав живицы входят 40-65% дитерпеновых (смоляных) кислот; 20-35% монотерпеновых углеводородов, 5-20% сескви- и дитерпеновых углеводородов.
З
Зайцева правило – в реакциях дегидратации и дегидрогалогенирования под действием оснований протон отщепляется преимущественно от наименее гидрогенизированного атома углерода.
|
|
|
CH3 |
|
CH3 |
|
|
|
CH3 |
|
CH3 |
||||||||||||||
|
|
|
|
|
|||||||||||||||||||||
CH3 |
|
CH2 |
|
C |
|
C |
|
CH3 |
CH3 |
|
CH2 |
|
C |
|
|
|
C |
|
CH3 |
||||||
|
|
|
|
|
|
|
|
|
|
||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
-HX |
||||||||||||
|
|
|
|
X |
|
H |
|||||||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||
Защитные группы – группы, которые временно вводятся в молекулу органических соединений с целью сохранения отдельных реакционных центров при химических реакциях.
Зинина реакция – восстановление ароматических нитросоединений в соответствующие амины.
C6H5-NO2 [H] C6H5-NH2
И
Идентификация – установление тождества (идентичности) анализируемого вещества с уже известным соединениям на основании сопоставления физикохимических параметров (температура плавления, УФ-, ИК-, ПМР-спектроскопия, характерные реакции и т.д.) обоих веществ.
Изомеризация – превращение молекулы органического соединения в его изомер. При этом может изменяться строение углеродного скелета, положение функциональных групп или пространственное расположение атомов и групп атомов.
Изомерия – явление, обусловленное существованием молекул, имеющих одинаковый качественный и количественный состав, но различающихся по химическим и физическим свойствам вследствие неодинакового расположения атомов (или атомных группировок) в молекуле или их ориентации в пространстве.
Геометрическая И. – 1) стереоизомерия, обусловленная различным расположением заместителей вокруг двойных связей; 2) изомерия комплексных соединений, обусловленная различным расположением лигандов во внутренней сфере комплекса.
Зеркальная И. (оптическая изомерия) – пространственная изомерия, обусловленная способностью энантиомеров вращать плоскость поляризованного света в противоположные стороны.
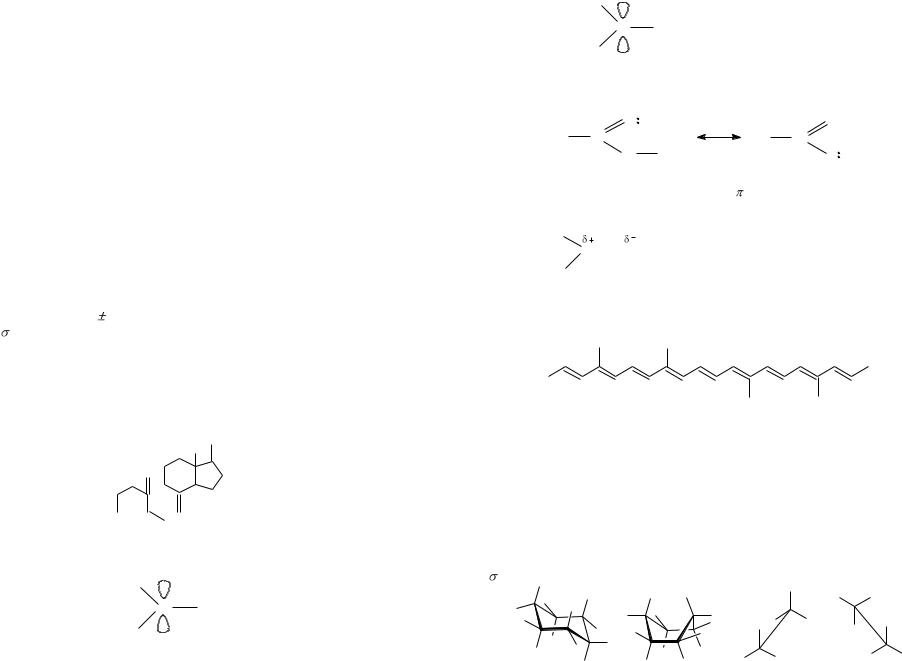
Конформационная И. – явление существования различных конформеров.
166
Пространственная И. – изомерия, обусловленная наличием химических соединений, построенных из одинаковых атомов с одинаковым порядком связей, но отличающихся расположением атомов (или атомных групп) в пространстве.
Структурная И. – разновидность изомерии, проявляемая двумя (и более) соединениями, отвечающими одной молекулярной формуле, но различающимися между собой: 1) строением углеродного скелета (например, бутан и изобутан); 2) различным расположением одинаковых функциональных групп (или кратных связей при одинаковом углеродном скелете), например, октанолы; α-,β-, γ- аминомасляные кислоты и т.д.; 3) различным порядком связи структурных элементов (например, диэтиловый эфир и бутанолы).
Цис-транс-декалиновая И. – изомерия, обусловленная различным расположением атомов водорода, связанных с двумя общими атомами углерода в молекуле декалина, относительно плоскости соединенных участков циклогексановых колец.
Изопрен – CH2=C(CH3)-CH=CH2
Изопреноиды – группа природных соединений, построенных из остатков изопрена (терпены и их производные, смоляные кислоты, стероиды).
Имины – N-производные карбонильных соединений: R1R2C=N-R Инверсия – изменение свойств системы на противоположные. Индуктивный эффект ( I) – перераспределение электронной плотности
вдоль линии -связи. Причиной этого является различная электроотрицательность атомов, между которыми осуществляется связь.
Инфракрасная спектроскопия (ИК-спектроскопия) – раздел молекулярной оптической спектроскопии, охватывающий диапазон длин волн 10-6-10-3м и изучающий спектры характеристических колебаний функциональных групп.
К
Кальциферолы – витамины группы D (D1-D7)
R
HO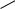


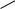
Карбанионы – органические анионы, характеризующиеся четным числом электронов и преимущественной локализацией отрицательного заряда на атоме углерода.
:
C-
Карбкатионы – органические катионы, положительный заряд преимущественно локализован на атоме углерода, находящегося в sp2-гибридном состоянии. Такой атом углерода имеет три связи и вакантную р-орбиталь.
167
C+
Карбоксильная группа – функциональная группа –COOH, определяющая свойства карбоновых кислот, имеет строение, промежуточное между двумя предельными структурами:
|
.. |
|
|
+ |
|
|
O |
|
|
|
|
|
|
|
O H |
||
C |
|
|
|
.. |
|
.. |
|
C |
.. |
- |
|
|
|
|
|||
|
O |
H |
|
O |
|
|
.. |
|
|
|
|
|
|
|
|
.. |
|
Карбонильная группа – функциональная группа С=О, в которой атомы углерода и кислорода связаны между собой ζ- и -связями. Валентный угол равен 1200. Вследствие большей электроотрицательности атома кислорода связь в карбонильной группе сильно поляризована:
C  O
O
Каротиноиды - полиненасыщенные соединения терпенового ряда, построенные по единому признаку: полиеновая цепь, состоящая из четырех изопреноидных фрагментов, по обоим концам связана либо с циклогексановыми циклами, либо с алифатическими фрагментами, состоящими из изопреноидных остатков.
CH3 |
CH |
|
|
|
3 |
|
|
|
|
|
R1 |
R |
|
|
|
|
CH |
3 |
CH3 |
|
|
|
Комплементарность – термин, обозначающий структурное соответствие любых молекул или участков молекул, благодаря чему формируется комплекс. В нуклеиновых кислотах комплементарными парами являются пары оснований (аденин – тимин, гуанин – цитозин) по одному от каждой полинуклеотидной цепи.
Конфигурация – пространственное расположение атомов или атомных групп относительно хирального центра, двойной связи или плоскости цикла.
Конформация – определенная геометрия молекулы, обусловленная внутренним вращением атомов или групп атомов вокруг простых связей. Конформации одного соединения отличаю тся степенью поворота вокруг одной (или более) -связи.
«кресло» «ванна» «заслоненная» «заторможенная»

168
Л
Лакриматоры – вещества, характеризующиеся слезоточивым действием. Лактамы – внутренние амиды аминокислот, в которых амидная связь явля-
ется частью циклической структуры.
O H2C C 
NH
H2C CH2
Лактаты – соли и сложные эфиры молочной кислоты.
Лактиды – циклические сложные эфиры, образованные двумя молекулами α-гидроксикислот:
O |
O |
R |
|
|
|
R1 |
O |
O |
|
||
|
|
Лактоны – 1) внутренние циклические сложные эфиры гидроксикислот; 2) соединения, содержащие сложноэфирную группу в цикле. В зависимости от числа атомов в цикле различают - (4 атома), - (5 атомов), δ- (6 атомов) лактоны.
|
|
O |
|
|
O |
|
O |
O |
O |
|
O |
|||
|
|
|||
|
|
|
|
Липиды – группа природных соединений, содержащихся в растительных и животных тканях. Жироподобные вещества, главным образом производные высших жирных кислот, спиртов или альдегидов (например, глицеролипиды, фосфолипиды –лецитин, кефалин, сфинголипиды).
М
Марковникова правило – в реакциях присоединения молекул типа НХ к несимметричным алкенам, водород присоединяется к более гидрированному атому углерода двойной связи.
R-CH=CH2 + HX R-CHX-CH3
Масс-спектрометрия – метод исследования вещества, основанный на регистрации спектра ионов, образовавшихся при ионизации атомов и молекул. Распад молекул на отдельные фрагменты зависит от стабильности образующихся частиц.
Мезомерный эффект ( М) – это смещение -электронов сопряженных связей в сторону атомов с не достроенной до октета электронной оболочкой.
Моносахариды – углеводы, которые не способны гидролизоваться с образованием еще более простых углеводов. Моносахариды следует рассматривать как циклические полуацетали многоатомных альдегидо- и кетоноспиртов, связанные в растворе взаимными превращениями со своими таутомерными ациклическими формами.
169
Мутаротация – изменение оптической активности растворов сахаров во времени до установления таутомерного равновесия между ациклическими и циклическими формами.
Мыла – натриевые или калиевые соли высших жирных кислот.
Н
Надкислоты – органические кислоты, содержащие группы –CO-O-O-H. Например, надуксусная кислота CH3COOOH.
Нитрилы – органические соединения, содержащие группу -C N, называемую нитрильной. При гидролизе нитрилов образуются соответствующие карбоновые кислоты.
R-C N + 3HOH R-COOH + NH3
Нитрозосоединения – органические соединения, содержащие в своей молекуле нитрозогруппу –N=O, связанную с атомом углерода.
Нуклеофил – любой атом или группа атомов, которые могут быть донорами электронной пары, т.е. являются основаниями Льюиса. Нуклеофилы могут быть как электронейтральными (:NH3), так и отрицательно заряженными части-
цами (OH-, Hal-).
О
Озазоны – соединения общей формулы R-NH-N=C(R1)-C(R2)=N-NH-R3.
Озониды – органические соединения, образующиеся при взаимодействии органических соединений с озоном и содержащие фрагмент:
C O C
O O
Оксалаты – соли и эфиры щавелевой кислоты.
Оксимы – органические соединения, содержащие группировку R2C=N-OH. Олигосахариды – углеводы, в построении молекул которых участвуют 2- 10 моносахаридных остатков, связанных О-гликозидной связью. Различают: 1)
восстанавливающие, содержащие по крайней мере один гликозидный гидроксил мальтоза, лактоза и др.); 2) невосстанавливающие, не имеющие гликозидных гидроксилов (сахароза и др.).
Омыление – щелочной гидролиз сложных эфиров.
Оптическая активность – способность хиральных молекул вращать плоскость поляризации света.
Орто, мета, пара-положения (сокращенно о-, м-, п-) обозначение положения заместителей в бензольном кольце.
OH |
OH |
OH |
|
|
|
CH3 |
|
|
|
CH3 |
|
|
|
CH3 |
о-метилфенол |
м-метилфенол |
п-метилфенол |

170
П
Пектины – полисахариды растительного происхождения, построенные из остатков замещенных α-D-галактуроновых кислот, связанных между собой α-1-4 гликозидными связями.
Полисахариды – углеводы, молекулы которых содержат более десяти моносахаридных остатков, соединенных О-гликозидными связями и образующих линейные или разветвленные цепи (крахмал, целлюлоза,гликоген и др.).
Р
Резонанс – изображение строения молекул с помощью гипотетических резонансных структур. Этот способ используют, когда для объяснения свойств данной молекулы не может быть использовано однозначное описание распределения электронов при помощи только одной структуры.
Резонансный гибрид – атомное и электронное распределение, соответствующее «реальной молекуле». Примером может служить бензол.
Ректификация – разделение гомогенных жидких смесей на чистые компоненты или фракции, отличающиеся температурами кипения.
С
Сопряжение – тип электронного взаимодействия в молекулах, ионах, радикалах, в структуре которых имеет место чередование простых и кратных связей ( , -сопряжение), или совокупности этих связей с атомами или группами атомов, содержащих неподеленные электронные пары, вакантные или частично заселенные валентные орбитали (р, -сопряжение).
Спектр действия лекарственного средства – характеристика лекарствен-
ного средства, отражающая все многообразие фармакологических эффектов, которые оно оказывает.
Спектрофотометрия – метод исследования, основанный на измерении спектров поглощения в УФ (200-400 нм), видимой (400-700 нм) и ИК ( 760 см-1) областях спектра. Используется для качественной идентификации и количественного анализа веществ.
Стереоизомерия – изомерия, обусловленная различным пространственным расположением атомов в молекуле. Различают два вида стереоизомерии: опти-
ческую и геометрическую.
Стереоизомеры – соединения, отвечающие одной общей формуле и характеризующиеся одинаковой направленностью связей, но отличающиеся друг от друга пространственным расположением атомов и атомных групп.
Стерический фактор – фактор, учитывающий необходимость определения взаимной ориентации реагирующих частиц при их столкновении для осуществления химической реакции.
171
Структурные изомеры – см. Изомерия структурная.
Сублимация – фазовый переход вещества из твердого состояния в газообразное минуя жидкое состояние.
Т
Тартраты – соли винной кислоты.
Таутомерия – явление самопроизвольного взаимного превращения структурных изомеров, находящихся в состоянии подвижного равновесия. Например, кето-енольная (взаимное превращение кетонной и енольной форм химического соединения, осуществляемое миграцией протона):
CH3-C-CH2-C |
O |
CH3- C=CH-C |
O |
|||
|
|
|||||
|
|
|
|
|
|
OC2H5 |
O |
OC2H5 |
OH |
||||
кольчато-цепная (переход циклических и ациклических форм углеводов):
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
|
C H |
|
|
|
|
|
|
||||||
|
|
|
|
|
|
|
|
|
|
|
|
C |
|
|
OH |
|
|
|
|
|
|
|||
|
|
|
|
CH2OH |
H |
|
|
|
|
CH2OH |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
O |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
O |
|
||||
|
|
HO |
|
|
C |
|
|
H |
|
|
|
OH |
||||||||||||
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
H |
|
C |
|
|
|
|
OH |
|
|
|
OH |
|
|
|||||||||
HO |
|
|
|
|
OH |
H |
|
|
|
|
|
|
|
|
|
|
HO |
|
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||||
|
|
|
|
|
OH |
|
|
|
C |
|
|
|
OH |
|
|
|
|
OH |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
||||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
CH2OH
лактим-лактамная (превращения лактимной и лактамной форм):
|
O |
|
OH |
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
H |
N |
N |
|
|
N |
|
|
|
|
||
|
|
|
|
|
|
O |
N |
|
N |
|
N |
|
O |
|
|
HO |
|
|
|
|
|
|
|
|
H |
|
H |
|
|
Терпеноиды – общее название производных углеводородов, относящихся к терпенам.
Терпены – группа природных соединений, отвечающих общей формуле (C5H8)n, где n 2. Терпены построены из изопреновых остатков, которые, согласно изопреновому правилу Ружички, связаны между собой по типу «голова к хвосту». По числу изопреновых остатков терпены делят на монотерпены C10H16, сесквитерпены C15H24, дитерпены C20H32, тритерпены C30H48, политерпены. Терпены являются составной частью эфирных масел, обладают душистым запахом, перегоняются с водяным паром.
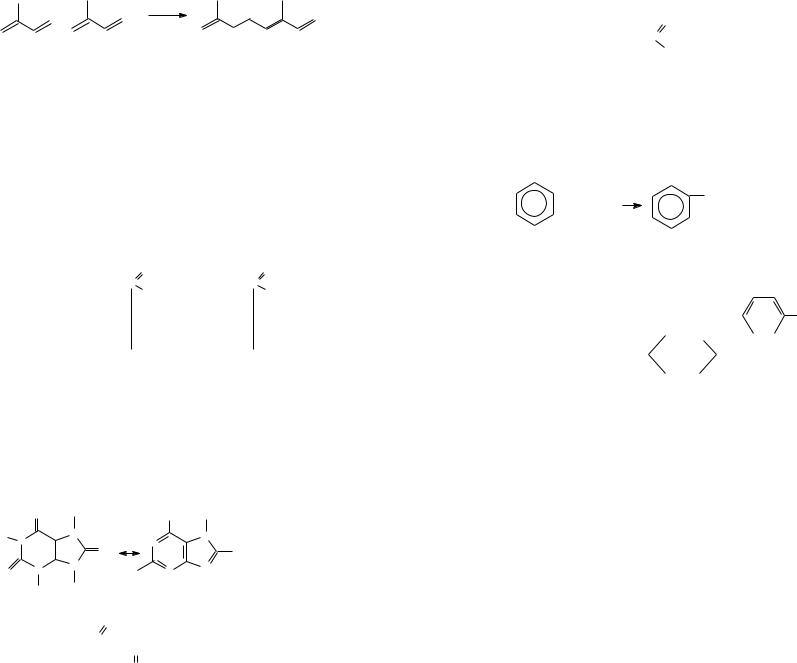
|
172 |
|
хвост |
голова |
оцимен |
Тиолы (тиоспирты, меркаптаны) – являются аналогами соответствующих спиртов, поскольку с углеводородным радикалом вместо ОН группы связана группа SH, называемая меркаптоили тиольной группой.
Токоферолы – витамины группы Е, представляющие собой высокомолекулярные соединения.
Токсичность – свойство биологически активного соединения или лекарственного средства вызывать нежелательные биологические эффекты в дозах больших, чем лечебные.
Толерантность – способность организма переносить воздействие определенного соединения без развития токсического эффекта.
Трео-форма – термин, используемый для указания различного расположения двух одинаковых заместителей у соединения с двумя хиральными центрами. Одинаковые заместители располагаются на разных сторонах проекционной формулы.
|
|
O |
|
|
O |
||||
H |
C H |
|
|
C H |
|||||
|
|
OH |
HO |
|
|
H |
|||
|
|
|
|
||||||
HO |
|
|
|
H |
H |
|
|
OH |
|
|
|
|
|
|
|||||
|
|
CH2OH |
|
|
CH2OH |
||||
Тривиальные названия – названия, которые использовались для химических соединений на ранней стадии становления химии.
У
Угол валентный – угол между направлениями химических связей в молекулах и кристаллах.
Угол оптического вращения (символ – α, единица – град) – угол, на который отклоняется (вправо или влево) плоскополяризованный свет при прохождении через раствор оптически активного вещества.
Ураты – соли мочевой кислоты.
|
O |
H |
|
|
|
OH H |
|
H |
N |
N |
|
|
N |
|
N |
|
|
O |
|
|
|
||
|
|
|
|
|
|
OH |
|
|
|
|
|
|
|
|
|
O N |
N |
|
|
|
N |
N |
|
|
|
HO |
|
|
|||
|
|
H |
|
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уреиды – N-ацилпроизводные мочевины, отвечающие общей формуле:
O
R-C
 NH-C-NH2
NH-C-NH2
O
173
Уретаны – эфиры карбаминовой кислоты, отвечающие общей формуле:
O
RNH-C
OR'
Ф
Фриделя-Крафтса реакция – алкилирование или ацилирование ароматических соединений алкилили ацилгалогенидами в присутствии AlCl3 (FeCl3; ZnCl2). В качестве ацилирующих агентов используют также ангидриды кислот или нитрилы. Реакция протекает по механизму SЕ.
+ RCOCl |
COR |
|
+ HCl |
||
|
Фенольные гликозиды – природные гликозиды, агликоны которых относятся к фенольным соединениям. Примером фенольных гликозидов является арбутин (гидрохинон-О-β-D-глюкопиранозид).
|
|
CH2OH |
O |
|
|
|
|
|
OH |
||||
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
|
||||
H |
|
|
O |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
OH |
H |
|
|
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
||||
HO |
|
|
|
|
|
|
|
|
|||||
|
|
|
|
|
|
|
|
|
|
|
|
||
|
|
|
|
H |
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|||
|
|
|
H |
OH |
|
|
|
|
|
|
|
|
|
Фенольные соединения – обширная группа природных соединений вторичного происхождения, представляющих собой фенолы и их производные. Согласно современным представлениям о биосинтезе фенольных соединений, их можно разделить на следующие типы:
1)соединения С6-ряда – простые фенолы (I),
2)соединения С6-С1-ряда – производные бензойной кислоты (фенольные кислоты) (II),
3)соединения С6-С2-ряда – фенолоспирты и фенилуксусные кислоты (III),
4)соединения С6-С3-ряда – производные фенилпропана (гидроксикоричные спирты, кислоты и кумарины) (IV),
5)соединения, относящиеся к дифенилпропану С6-С3-С6 (флавоноиды и изофлавоноиды) (V),
6)соединения, содержащие фрагмент С6-С3-С3-С6 – лигнаны (VI),
7)производные антрацена (VII),
8)полимерные соединения –лигнин, танниды, меланины:

174
OH |
OH |
OH |
OH |
|
|
|
|
||
OH |
COOH |
CH2-CH2OH |
CH=CH-COOH |
|
|
||||
(I) |
(II) |
(III) |
(IV) |
|
|
|
|
||
двухатомные |
гидроксибен- |
гидроксифенил |
гидроксикоричные |
|
фенолы |
зойные кислоты |
этиловый спирт |
кислоты |
|
O |
|
|
OH O |
OH |
|
|
|
||
|
H3CO |
CH2OH |
H3C |
OH |
|
|
|
||
O |
H3CO |
CH2OH |
|
|
|
|
|
|
|
(V) |
|
|
O |
|
флавон |
|
OCH3 |
(VII) |
|
|
|
кладофульфин |
||
|
|
|
||
OH (VI)
секо-изоларицирезинол
Фенолы – гидроксипроизводные ароматического ряда, где ОН-группа связана с ароматическим ядром. По числу гидроксигрупп различают одно- двух-, трех- и многоатомные фенолы.
Фишера формулы – способ изображения на плоскости пространственных структур молекул, имеющих хиральные центры. Проекции Фишера применимы для соединений с несколькими хиральными центрами, в том числе и для молекул, изображение которых в трехмерном пространстве затруднено.
Для построения проекционных формул тетраэдрическую модель располагают так, чтобы рассматриваемый асимметрический атом углерода находился в плоскости чертежа. Связи, направленные за плоскость чертежа, проецируются в вертикальные связи, а направленные перед плоскостью – в горизонтальные связи. Точка пересечения вертикальных и горизонтальных линий соответствует асимметрическому атому углерода.
175
|
1 |
|
1 |
|
1 |
|
|
|
|
|
|
|
2 |
3 |
4 |
3 |
4 |
|
C |
||||
|
|
|
|
|
|
3 |
4 |
|
2 |
|
2 |
|
|
|
|||
|
|
|
|
|
|
|
|
|
|
проекция Фишера |
|
|
|
O |
|
O |
|
|
|
С H |
|
С H |
|
|
HO |
H |
HO |
H |
|
|
|
CH2OH |
|
CH2OH |
|
L-глицериновый альдегид
Функциональная группа - атом или группа атомов, определяющие характерные химические свойства данного класса химических соединений. Например, ОН-группа в спиртах и фенолах; С=О (оксогруппа) в карбонильных соединениях; -СООН-группа в кислотах и т.д.
Х
Хелатные комплексы – комплексы, лиганды которых способны к образованию циклов.
Хеуорса формулы – изображение на плоскости циклической структуры, приближенное к пространственному строению. Цикл условно считают плоским. Это циклические формулы углеводов.
|
CH2OH |
|
|
|
|
|
|
|
|
||||
H |
|
|
O |
|
H |
HOCH2 O |
|
OH |
|||||
|
|
|
|
|
|
|
|
|
|||||
|
H |
H |
|
|
|
H |
H |
|
|||||
|
|
|
OH |
|
|
|
|
|
|
|
|
||
|
|
H |
|
|
H |
||||||||
|
|
|
|
|
|
|
|||||||
HO |
|
|
|
|
OH |
|
|
||||||
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
OH |
OH |
|||
|
H |
OH |
|
|
|
||||||||
|
|
|
|
|
|
|
|
|
|||||
-D-глюкопираноза -D-рибофураноза
Хиральность – основное понятие стереохимии, обозначающее свойство объекта быть несовместимым со своим зеркальным отображением. Хиральные молекулы характеризуются отсутствием центра и плоскости симметрии.
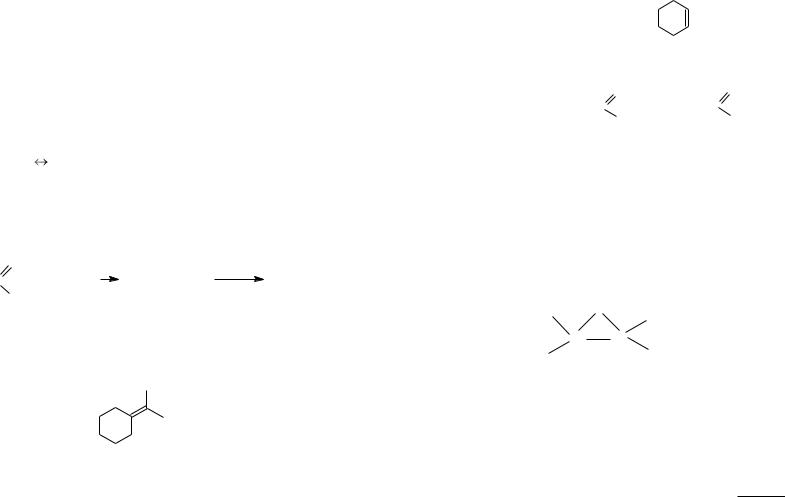
Хиральный центр – атом, связанный с четырьмя различными атомами или группами атомов.
хиральный
центр COOH
CH3
C
H OH
176
Хроматография – совокупность методов разделения, анализа и физикохимических исследований смесей растворенных веществ, где используется разделяющая среда (неподвижная фаза) и какой-либо растворитель (подвижная фаза).
Хюккеля правило – один из признаков, определяющих ароматичность: плоская циклическая структура является ароматической, если она содержит (4n + 2)π-электронов, участвующих в формировании единой делокализованной π- электронной системы.
Ц
Цвиттер-ион – нейтральные молекулы, в которых одновременно присутствуют разделенные противоположные заряды. Такие ионы образуют аминокислоты.
NH2-CH2-COOH |
+NH3-CH2-COO- |
|
|
||||
Цитраты - соли и эфиры лимонной кислоты. |
|
|
|||||
Ш |
|
|
|
|
|
|
|
Шиффовы основания (азометины) – соединения |
общей формулы |
||||||
RR1C=NR2, получаемые реакцией Шиффа. |
|
|
|
|
|
|
|
O |
|
|
H |
|
|
|
|
|
|
|
|
|
|||
|
|
|
|
|
|
|
|
R- C |
+ H2N-R' |
R-C-NH-R' |
|
R-CH=N-R' |
|||
H |
|
|
|
|
|
- H2O |
|
|
|
OH |
|
||||
|
|
|
|
||||
Э
Экзоциклическая двойная связь – связь, в которой один из двух sp2гибридных атомов углерода, участвующих в образовании двойной связи, участвует и в построении цикла.
Экстракция - извлечение и разделение компонентов раствора путем перевода их из одной фазы в другую. Второй жидкой фазой является растворитель – экстрагент, который добавляется к исходному раствору и не смешивается с исходной жидкой фазой.
Электрофил – любая частица или фрагмент молекулы, характеризующийся наличием свободной орбитали (например, катионы) или пониженной электронной плотностью и способные принимать электронную пару атома-партнера для образования ковалентной связи.
Элиминирование – процесс, в ходе которого от исходной молекулы отщепляется группа атомов.
177
Энантиомеры – пара оптических изомеров, относящихся друг к другу как предмет и его зеркальное отражение.
Эндоциклическая двойная связь – оба sp2гибридных атома углерода, об-
разующих двойную связь, участвуют в построении цикла:
Эпимеры – пара диастереомеров, содержащие несколько хиральных центров, но различающиеся между собой конфигурацией только одного хирального центра. Например, глюкоза и галактоза.
1 |
|
|
|
O |
|
1 |
|
|
|
O |
||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
||||
С |
|
|
H |
|
|
С |
|
H |
||||||||
2 |
|
|
|
|
|
2 |
|
|
|
|
||||||
|
|
|
|
|
OH |
H |
С |
|
OH |
|||||||
H |
|
|
С |
|
|
|
|
|
||||||||
3 |
|
|
|
|
|
|||||||||||
HO |
|
|
|
|
|
|
H |
HO |
3 |
|
|
|
|
H |
||
|
С |
|
|
|
С |
|
|
|||||||||
|
|
|
|
4 |
|
|
||||||||||
4 |
|
|
|
|
|
|
OH |
HO |
|
|
|
|
|
H |
||
|
|
|
|
|
|
|
|
|
|
|
||||||
H |
|
|
С |
|
|
|
|
С |
|
|
||||||
5 |
|
|
||||||||||||||
5 |
|
|
|
|
|
|||||||||||
H |
|
|
|
|
|
|
OH |
H |
|
|
|
|
|
OH |
||
|
|
|
|
|
|
|
|
|
|
|
||||||
С |
|
С |
|
|
||||||||||||
|
|
|
|
|
|
|||||||||||
6 |
|
|
|
|
|
|
|
6 |
|
|
|
|
|
|
||
СH OH |
|
СH2OH |
||||||||||||||
|
|
|
|
|
||||||||||||
|
|
|
|
|
2 |
|
|
|
|
|
|
|
|
|
|
|
|
глюкоза |
|
галактоза |
|||||||||||||
Эпоксид – соединение, образующееся при окислении алкенов и содержащее группу:
O
C C
Эритро-форма – термин, используемый для указания различного расположения двух одинаковых заместителей у соединения с двумя хиральными центрами. Одинаковые заместители располагаются по одну сторону проекционной формулы.
|
H |
|
|
H |
|||||
HO |
|
|
|
CH2CH3 |
CH3CH2 |
|
|
|
OH |
|
|
|
|
|
|
||||
HO |
|
|
|
CH3 |
CH3 |
|
|
OH |
|
|
|
|
|||||||
|
|
|
|
|
|
|
|
|
|
|
H |
|
|
H |
|||||
Этерификация – получение сложных эфиров взаимодействием карбоновых кислот и спиртов по обратимой реакции:
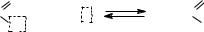
|
|
178 |
|
R-C |
O |
H+ |
O |
+ R'-OH |
R-C |
+ H2O |
|
|
OH |
|
OR' |
Эффекты заместителей – влияния, оказываемые атомами или группами атомов (заместителями) на атомы углерода, с которыми они связаны. Это влияние обусловлено либо различием в электроотрицательности заместителя и связанного с ним атома С, либо участием центрального атома заместителя в сопряженной системе связей.
Ядерный магнитный резонанс (ЯМР) - физический метод исследования,
основанный на избирательном взаимодействии магнитной компоненты радиочастотного электромагнитного излучения с системой ядерных магнитных моментов атомов вещества.
Список формул для запоминания
Алканы
Метан, этан, пропан ……. додекан.
Циклоалканы
Циклопропан, циклобутан, циклопентан, циклогексан.
Алкены
Этилен, пропен, бутен ………..
Диены
Бутадиен-1,3, изопрен (2-метилбутадиен-1,3), ……………..
Алкины
Ацетилен,……………
Ароматические углеводороды
Бензол, толуол, ксилолы (орто-, мета- и пара-), нафталины, антрацен, фенантрен.
Спирты
Метанол, этанол, пропанол, изопропиловый спирт, бутанолы. Бензиловый спирт, циклогексанол.
Этиленгликоль, глицерин.
Фенолы
Фенол, крезолы (орто-, мета-, пара-), гидрохинон, резорцин, пирокатехин, пирогаллол.
Альдегиды и кетоны
Альдегиды называют в соответствии с названиями карбоновых кислот, заменив слово кислота на альдегид.
Формальдегид (муравьиный альдегид), этаналь (уксусный альдегид), пропеналь (акриловый альдегид, акролеин), бензальдегид (бензойный альдегид). Ацетон, ацетофенон (метилфенилкетон), пара-хинон.
Карбоновые кислоты
Предельные одноосновные кислоты
179
Муравьиная кислота, уксусная кислота, пропионовая кислота, масляная кислота, валериановая кислота, капроновая кислота.
Непредельные одноосновные кислоты Акриловая кислота, метакриловая кислота, кротоновая кислота.
Ароматические кислоты Бензойная кислота, фталевая кислота, тере-фталевая кислота.
Предельные двухосновные кислоты Щавелевая кислота, малоновая кислота, янтарная кислота, глутаровая кислота.
Непредельные двухосновные кислоты Малеиновая кислота, фумаровая кислота.
Оксикислоты Гликолевая кислота, молочная кислота, винная кислота, яблочная кислота, ли-
монная кислота, салициловая кислота. Оксокислоты
Глиоксалевая кислота, пировиноградная кислота, ацетоуксусная кислота. Угольная кислота и ее производные
Карбамид, мочевина, уреид кислоты, уреидокислоты.
Высшие жирные карбоновые кислоты, входящие в состав жиров Пальмитиновая кислота, стеариновая кислота, олеиновая кислота, линолевая кислота, линоленовая кислота.
Амины и азотсодержащие соединения
Первичные, вторичные, третичные амины алифатического и ароматического ряда: метиламин, пропиламин, метилэтиламин, анилин, дифениламин, этилфениламин.
Аминоспирты: коламин, холин, ацетилхолин.
Гидразин, фенилгидразин, гидроксиламин, синильная кислота.
Аминокислоты
22 аминокислоты (см. учебник «Биоорганическая химия» Н.А.Тюкавкиной), цистин.
Фосфолипиды
Фосфатидная кислота, кефалин, лецитин, фосфатидилсерины., сфингозин, сфингомиелин.
Углеводы
Рибоза, дезоксирибоза, ксилоза, глюкоза, фруктоза, галактоза, манноза. Мальтоза, лактоза, сахароза, целлобиоза. Глюкуроновая кислота. Крахмал, клетчатка, целлюлоза.
Гетероциклические соединения
Фуран, тиофен, пиррол, пиразол, имидазол, пиридин, никотиновая кислота, пиримидин, пиридазин, пурин, урацил, цитозин, тимин, аденин, гуанин, барбиту-
ровая кислота, мочевая кислота, гипоксантин. Пиридоксальфосфат. НАДН, НАД+.
Неомыляемые липиды
Терпены: 3-карен, α- и β-пинены, лимонен, ментол, камфора. Каротиноиды: ретинол, ретиналь, β-каротин.
